四川省乐山市2023年中考化学真题
试卷更新日期:2023-08-16 类型:中考真卷
一、单选题
-
1. 下列与乐山有关的生产生活场景中涉及化学变化的是( )A、
 沐川船伐漂流
B、
沐川船伐漂流
B、 夹江烧制瓷砖
C、
夹江烧制瓷砖
C、 峨眉山冰雪融化
D、
峨眉山冰雪融化
D、 马边采摘绿茶
2. 规范的实验操作是实验成功和安全的保证,下列实验操作中正确的是( )A、
马边采摘绿茶
2. 规范的实验操作是实验成功和安全的保证,下列实验操作中正确的是( )A、 熄灭酒精灯
B、
熄灭酒精灯
B、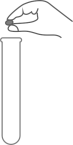 取用块状固体
C、
取用块状固体
C、 闻气体气味
D、
闻气体气味
D、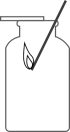 验满
3. 在探究燃烧的条件时,某同学点燃装有半杯水的纸杯,发现纸杯盛水部分没有燃烧,其主要原因是( )A、纸杯着火点变高 B、纸杯不是可燃物 C、纸杯未与氧气接触 D、温度低于纸杯着火点4. 物质的性质决定了用途,下列物质的用途主要由化学性质决定的是( )A、氦气用于充灌气球 B、盐酸用于除铁锈 C、干冰用于人工降雨 D、铜用于制作导线5. 农业上用质量分数为16%的溶液选种,实验室配制100 g该溶液的过程中不需要用到的仪器是( )A、
验满
3. 在探究燃烧的条件时,某同学点燃装有半杯水的纸杯,发现纸杯盛水部分没有燃烧,其主要原因是( )A、纸杯着火点变高 B、纸杯不是可燃物 C、纸杯未与氧气接触 D、温度低于纸杯着火点4. 物质的性质决定了用途,下列物质的用途主要由化学性质决定的是( )A、氦气用于充灌气球 B、盐酸用于除铁锈 C、干冰用于人工降雨 D、铜用于制作导线5. 农业上用质量分数为16%的溶液选种,实验室配制100 g该溶液的过程中不需要用到的仪器是( )A、 B、
B、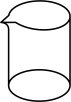 C、
C、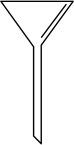 D、
D、 6. 山药中含有碱性皂角素,有些人皮肤沾上会发痒,涂抹下列家中常见物质能明显缓解该不适的是( )
6. 山药中含有碱性皂角素,有些人皮肤沾上会发痒,涂抹下列家中常见物质能明显缓解该不适的是( ) A、食醋 B、花生油 C、牙膏 D、肥皂水7. 碱性锌锰电池性能优越,其组成物质包括锌粉、氢氧化钾、二氧化锰、石墨等,这些物质的类别不包括( )A、酸 B、碱 C、单质 D、氧化物8. 碳是组成物质最多的元素,碳元素的相关信息和碳原子的结构示意图如图所示,下列说法正确的是( )
A、食醋 B、花生油 C、牙膏 D、肥皂水7. 碱性锌锰电池性能优越,其组成物质包括锌粉、氢氧化钾、二氧化锰、石墨等,这些物质的类别不包括( )A、酸 B、碱 C、单质 D、氧化物8. 碳是组成物质最多的元素,碳元素的相关信息和碳原子的结构示意图如图所示,下列说法正确的是( )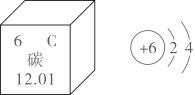 A、碳原子核外有4个电子 B、碳是一种金属元素 C、碳原子核内有12个质子 D、碳元素能组成多种单质9. 科学家通过“祝融号”火星车探测器测得火星表面大气成分(体积分数)如图所示,下列说法正确的是( )
A、碳原子核外有4个电子 B、碳是一种金属元素 C、碳原子核内有12个质子 D、碳元素能组成多种单质9. 科学家通过“祝融号”火星车探测器测得火星表面大气成分(体积分数)如图所示,下列说法正确的是( )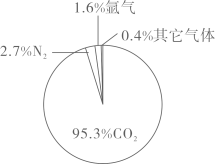 A、火星大气中的含量最高 B、火星大气中的含量高于空气 C、火星大气不含稀有气体 D、火星大气能使带火星的木条复燃10. 氯乙烯(丙)是生产环保PVC材料的重要原料,如图是一种合成氯乙烯的反应的微观示意图,下列说法正确的是( )
A、火星大气中的含量最高 B、火星大气中的含量高于空气 C、火星大气不含稀有气体 D、火星大气能使带火星的木条复燃10. 氯乙烯(丙)是生产环保PVC材料的重要原料,如图是一种合成氯乙烯的反应的微观示意图,下列说法正确的是( )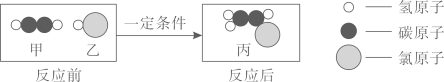 A、甲的化学式为 B、乙的相对分子质量为36.5 g C、丙中氢元素的质量分数最高 D、丙由三种元素组成11. 气体的溶解度通常指压强为101 kPa和一定温度时,在1体积水里溶解达到饱和状态时的气体体积。如图是甲、乙两种气体在101 kPa时的溶解度曲线,下列说法正确的是( )
A、甲的化学式为 B、乙的相对分子质量为36.5 g C、丙中氢元素的质量分数最高 D、丙由三种元素组成11. 气体的溶解度通常指压强为101 kPa和一定温度时,在1体积水里溶解达到饱和状态时的气体体积。如图是甲、乙两种气体在101 kPa时的溶解度曲线,下列说法正确的是( )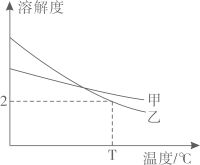 A、甲的溶解度大于乙的溶解度 B、两种气体的溶解度都随温度升高而增大 C、甲气体的溶解度受温度的影响小于乙 D、T℃时,气体乙的溶解度为2 g12. 目前许多学校安装了直饮水机,只要将它与自来水连接,便可以除去水中的部分杂质得到直饮水。某品牌直饮水机的工作原理如图所示,下列说法正确的是( )
A、甲的溶解度大于乙的溶解度 B、两种气体的溶解度都随温度升高而增大 C、甲气体的溶解度受温度的影响小于乙 D、T℃时,气体乙的溶解度为2 g12. 目前许多学校安装了直饮水机,只要将它与自来水连接,便可以除去水中的部分杂质得到直饮水。某品牌直饮水机的工作原理如图所示,下列说法正确的是( )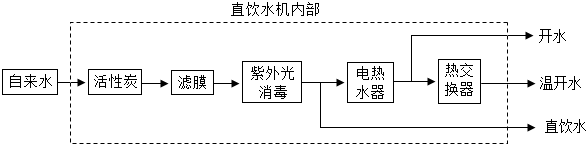 A、活性炭的作用是吸附 B、滤膜可除去水中的可溶性杂质 C、紫外光照射的作用是加热 D、直饮水一定是软水13. 已知20℃时,氢氧化钠易溶于酒精,碳酸钠在酒精中几乎不溶解。20℃时,某同学利用如图所示微型实验验证能与NaOH发生反应。打开止水夹,轻轻挤压软塑料瓶,观察实验现象,下列说法不正确的是( )
A、活性炭的作用是吸附 B、滤膜可除去水中的可溶性杂质 C、紫外光照射的作用是加热 D、直饮水一定是软水13. 已知20℃时,氢氧化钠易溶于酒精,碳酸钠在酒精中几乎不溶解。20℃时,某同学利用如图所示微型实验验证能与NaOH发生反应。打开止水夹,轻轻挤压软塑料瓶,观察实验现象,下列说法不正确的是( )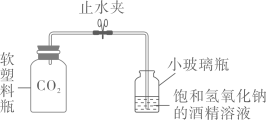 A、小玻璃瓶中导管口有气泡冒出 B、小玻璃瓶中有固体析出 C、应及时关闭止水夹防止小玻璃瓶中的液体倒吸 D、实验结束后,将小玻璃瓶中的物质倒入足量水中,无固体剩余14. 已知物质R由一种或多种物质组成。取一定质量的R在足量的氧气中完全燃烧,生成4.4 g二氧化碳和3.6 g水,下列分析不正确的是( )A、参加反应的R和氧气的质量总和一定等于8.0 g B、所取R质量的最小值为1.6 g C、R可能是酒精() D、若R为和的混合物,则和的分子个数比为
A、小玻璃瓶中导管口有气泡冒出 B、小玻璃瓶中有固体析出 C、应及时关闭止水夹防止小玻璃瓶中的液体倒吸 D、实验结束后,将小玻璃瓶中的物质倒入足量水中,无固体剩余14. 已知物质R由一种或多种物质组成。取一定质量的R在足量的氧气中完全燃烧,生成4.4 g二氧化碳和3.6 g水,下列分析不正确的是( )A、参加反应的R和氧气的质量总和一定等于8.0 g B、所取R质量的最小值为1.6 g C、R可能是酒精() D、若R为和的混合物,则和的分子个数比为二、填空题
-
15. 2023年5月28日,国产大型客机C919圆满完成首次商业飞行,制造飞机使用了大量的钢(铁和碳的合金)、铝合金、合成橡胶等材料。回答下列问题:(1)、以上材料属于有机合成材料的是。(2)、用化学符号表示以下微粒:
①3个铁原子;
②2个铝离子。
(3)、飞机的机身大量采用铝合金材料,其优点是(任写一条)。16. 氢能源是最理想的“绿色能源”之一,有规划地开发和使用氢能源是优化能源结构,实现“碳中和”的重要措施。我国氢能源的发展规划分为“灰氢”、“蓝氢”和“绿氢”三个阶段,具体如图所示。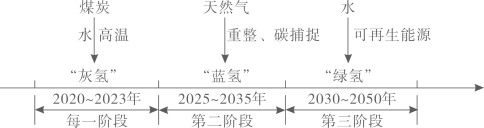
回答下列问题:
(1)、煤炭生成“灰氢”属于(选填“物理变化”或“化学变化”)。(2)、通过反应制备的氢气属于(选填“灰氢”、“蓝氢”或“绿氢”)。(3)、水分解生成“绿氢”时的另一种生成物为;写出一种用于制备“绿氢”的可再生能源。17. 化学学习要善于构建物质间的联系,形成“结构化”知识。某同学总结的部分铜及其化合物的转化关系如图所示。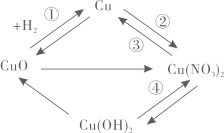
回答下列问题:
(1)、反应①中体现还原性的反应物是。(2)、Cu可以与浓硝酸发生反应②,该反应的化学方程为: , 反应中R的化学式为。(3)、将一根洁净的铝丝浸入硝酸铜溶液中能发生反应③。下列关于该反应的说法不正确的是。a.铝丝表面附着一层红色的物质
b.溶液的颜色由无色变为蓝色
c.此实验证明铝的金属活动性比铜强
d.该反应为置换反应
(4)、能与发生中和反应④,写出该反应的化学方程式。三、流程题
-
18. 保护环境,实现“绿水青山”目标,要对工厂尾气进行无害化处理。某氮肥厂和炼铁厂联合处理尾气的工艺流程如图所示。
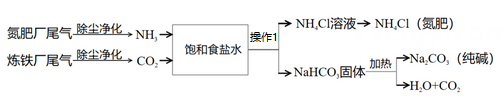
已知饱和食盐水处发生的反应为:。
回答下列问题:
(1)、饱和食盐水是(选填“纯净物”或“混合物”)。(2)、流程中“操作1”的名称为。(3)、根据信息写出加热固体发生反应的化学方程式。(4)、流程中,可循环使用的物质是。四、实验题
-
19. A-E是化学实验时常见的实验装置,组合不同装置可以实现、等气体的制备、干燥、收集等。
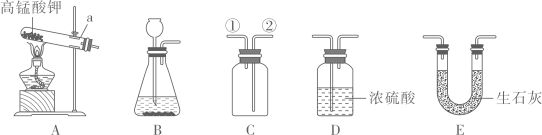
回答下列问题:
(1)、图中仪器a的名称为(2)、用装置A制备氧气时发生反应的化学方程式为 , 实验时应在试管口放一团(3)、利用装置C收集时,气体应从(选填“①”或“②”)导管口进入。(4)、欲制备并收集干燥的 , 应选用的装置为:B→→C(填装置序号)。五、科学探究题
-
20. 碳酸钠是生活中常用的盐,其水溶液呈碱性。某同学在完成教材十一单元“碳酸钠溶液与稀盐酸反应”的实验后(如图),对所得溶液溶质的成分进行如下探究。
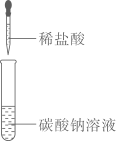
【反思讨论】
(1)、猜想Ⅰ:溶质只有;猜想Ⅱ:溶质有和;
猜想Ⅲ:溶质有和。
(2)、【实验探究】实验操作
实验现象
实验结论
实验1:取少量溶液于试管中,并向试管中加入一小段镁条。
猜想Ⅱ不正确
实验2:取少量溶液于试管中,滴加溶液。
有白色沉淀产生
猜想正确
(3)、【反思讨论】实验2中发生反应的化学方程式为。
(4)、某同学认为只要实验2中有白色沉淀产生,不需要实验1就可以判断猜想Ⅱ不正确,其理由是。(5)、向碳酸钠与稀硫酸反应后的溶液中进行下列操作,其现象一定能证明碳酸钠过量的是(填序号)。a.加入少量酚酞溶液后,溶液呈红色
b.继续加入稀硫酸,产生气泡
c.加入氢氧化钡溶液产生白色沉淀
d.加入少量铁屑后无气泡产生
六、计算题
-
21. 某一长期暴露在空气中的样品部分变质为并含少量水。取13.2 g该样品于烧杯中,加入39 g水使其完全溶解,向所得溶液中逐渐加入50 g溶质质量分数为14.6%的稀盐酸恰好完全反应。反应过程中产生气体的质量随时间的变化关系如图所示。(已知:)
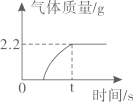
回答下列问题:
(1)、产生的的质量为g。(2)、计算13.2 g样品中碳酸钾的质量。(写出计算过程)(3)、计算反应后所得溶液中溶质的质量分数。(写出计算过程)
-
-
-