“高效课堂”1.3.1 盐酸的性质(提升版)--2023-2024学年浙教版科学九年级上册
试卷更新日期:2023-08-16 类型:同步测试
一、单选题
-
1. 下列各组物质相互接触,能发生化学反应却无明显现象的是( )A、氢氧化钠溶液与盐酸 B、氢氧化钡溶液与硫酸铜溶液 C、氧化铁与盐酸 D、石灰石与盐酸2. 某校九年级甲、乙两班同学进行常见酸和碱与指示剂反应的实验,使用的试剂如下图所示。实验后废液分别集中到废液缸中。某研究小组对此废液进行了检测,结果如下:
废液来源
检测方法和结果
甲班
观察废液呈无色
乙班
观察废液呈红色

请你根据实验现象判断,对该废液的溶质的说法错误的是( )
A、甲班废液中可能含有盐酸 B、甲班废液中只有氯化钠和氯化钙 C、乙班废液的成分中肯定没有盐酸 D、乙班废液中可能含有氢氧化钠3. 下列关于科学实验中的描述正确的是( )A、在某固体物质中加入稀盐酸,产生大量气泡,该物质一定是碳酸盐 B、在某溶液中加入氯化钡溶液和足量稀硝酸,产生白色沉淀,该溶液中一定含有硫酸根离子 C、在某溶液中加入硝酸银溶液和足量稀硝酸,产生白色沉淀,该溶液中一定含有氯离子 D、在稀盐酸与氢氧化钠反应后的溶液中滴加无色酚酞试液不变色,则两者恰好完全反应4. “类推”是科学学习过程中常用的思维方法。下列类推结果中,正确的是( )A、因为浓盐酸具有挥发性,所以浓硫酸也具有挥发性 B、因为金属铝与盐酸反应生成AlCl3和H2 , 所以金属铁与盐酸反应生成FeCl3和H2 C、因为离子是带电荷的粒子,所以带电荷的粒子一定是离子 D、因为蜡烛燃烧生成二氧化碳和水,所以蜡烛中一定含有碳元素和氢元素5. 能用金属与稀盐酸直接反应制取的是( )A、CuCl2 B、AgCl C、MgCl2 D、FeCl36. 取稀盐酸与氢氧化钠反应后的溶液进行实验下列能说明稀盐酸、氢氧化钠恰好都完全反应的是( )A、加硝酸银溶液,有白色沉淀生成 B、加氢氧化镁固体,固体全部溶解 C、加酚酞试液,溶液显红色 D、测定溶液的pH,刚好显中性7. 某同学在学习酸的化学性质后,做了甲、乙二个实验,实验结束后,把甲乙试管中的废液依次缓慢倒入同一洁净的废液缸中,下列对废液缸中废液成分的分析正确的是( ) A、废液中除氯化钠外,一定有氯化钙 B、如果废液呈酸性,则一定有氯化钙、氯化钠 C、如果废液呈碱性,则一定有氢氧化钙 D、废液中一定有氯化钠,还有氢氧化钙或碳酸钠或盐酸中的一种物质8. 兴趣小组按如图流程进行实验(每步均充分反应)。反应结束后,将烧杯内物质进行过滤,向滤渣中加入少量稀盐酸,无明显现象。下列说法不正确的是( )
A、废液中除氯化钠外,一定有氯化钙 B、如果废液呈酸性,则一定有氯化钙、氯化钠 C、如果废液呈碱性,则一定有氢氧化钙 D、废液中一定有氯化钠,还有氢氧化钙或碳酸钠或盐酸中的一种物质8. 兴趣小组按如图流程进行实验(每步均充分反应)。反应结束后,将烧杯内物质进行过滤,向滤渣中加入少量稀盐酸,无明显现象。下列说法不正确的是( ) A、滤渣中一定有Cu,一定没有Fe和Mg B、滤液中的溶质一定有FeCl2、MgCl2和CuCl2 C、本实验可判断出铁、铜、镁的活动性顺序 D、两支试管混合后,固体总质量一定增加9. 某同学在实验室做酸、碱性质的实验,所用试剂如图所示,实验后把三只试管的液体集中倒入一个废液缸中,废液呈蓝色。以下说法不正确的是( )
A、滤渣中一定有Cu,一定没有Fe和Mg B、滤液中的溶质一定有FeCl2、MgCl2和CuCl2 C、本实验可判断出铁、铜、镁的活动性顺序 D、两支试管混合后,固体总质量一定增加9. 某同学在实验室做酸、碱性质的实验,所用试剂如图所示,实验后把三只试管的液体集中倒入一个废液缸中,废液呈蓝色。以下说法不正确的是( ) A、废液呈碱性 B、废液中只存在2种溶质 C、废液中不存在盐酸和硫酸 D、废液中含有硫酸钠、氯化钠和氢氧化钠10. 实验小组按如图流程进行实验(每步均充分反应)。反应结束后,将烧杯内物质进行过滤,向滤渣中加入稀盐酸,无明显现象。下列说法正确的是( )
A、废液呈碱性 B、废液中只存在2种溶质 C、废液中不存在盐酸和硫酸 D、废液中含有硫酸钠、氯化钠和氢氧化钠10. 实验小组按如图流程进行实验(每步均充分反应)。反应结束后,将烧杯内物质进行过滤,向滤渣中加入稀盐酸,无明显现象。下列说法正确的是( ) A、本实验不可判断铁、铜、镁的金属活动性顺序 B、两支试管内的物质混合前后,固体总质量一定增加 C、滤渣中一定有Cu,一定没有Mg,可能有Fe D、滤液中的溶质一定有FeCl2、MgCl2、CuCl2
A、本实验不可判断铁、铜、镁的金属活动性顺序 B、两支试管内的物质混合前后,固体总质量一定增加 C、滤渣中一定有Cu,一定没有Mg,可能有Fe D、滤液中的溶质一定有FeCl2、MgCl2、CuCl2二、实验探究题
-
11. 兴趣小组的同学在做镁条和盐酸反应实验时发现, 试管外壁很烫,试管口出现白雾。白雾是什么呢? Ⅰ.同学们作出猜想
猜想一:是小水滴。因为盐酸溶液中的水受热会汽化上升,在试管口液化成小水滴。
猜想二:是盐酸小液滴。因为浓盐酸具有性,可能实验中使用的盐酸浓度过高,试管口就会形 成盐酸小液滴。
同学们将干燥的蓝色石蕊试纸放在内有正在反应的镁条和盐酸的试管口,试纸 , 证明猜想二是 合理的。
Ⅱ. 小柯提出质疑:为什么刚才打开盛放实验所用盐酸的试剂瓶,瓶口没有白雾,却在反应过程中出现白 雾?
小柯联系反应时试管外壁很烫, 于是猜想:白雾的形成可能与温度有关。
他用试管取少量盐酸,将干燥的蓝色石蕊试纸放在试管口,试纸不变红;然后 (填操作), 将(选填“干燥的”、“湿润的”) 蓝色石蕊试纸放在试管口,试纸变红。
得出结论: 这种盐酸浓度并不高,是镁和盐酸反应放热促使盐酸形成白雾。
12. 小乐做了“铝与酸反应”的系列实验,回答问题:实验1:小乐在试管中放入一枚未打磨的铝片,然后注入适量pH=4的稀盐酸。铝片与稀盐酸反应产生氢气的速率随时间变化的图线如图甲所示。
 (1)、铝片和稀盐酸在开始阶段不产生氢气的原因:(用相关化学反应方程式解释)。(2)、从a点到b点曲线上升的原因可能是
(1)、铝片和稀盐酸在开始阶段不产生氢气的原因:(用相关化学反应方程式解释)。(2)、从a点到b点曲线上升的原因可能是实验2:小乐将另一枚打磨过的铝片与适量pH=4的稀硫酸反应,结果生成氢气速率很慢。
针对铝片与稀盐酸和稀硫酸反应速率不同的现象,小乐提出了如下猜想:
猜想1:盐酸中的氯离子对反应起促进作用;
猜想2:硫酸中的硫酸根离子对反应起阻碍作用。
为了验证猜想,小乐设计了如图乙所示实验。
(3)、加入的两种固体物质A和B分别是。三、填空题
-
13. 盐酸在实验室有较多的使用,也呈现出不同的性质。(1)、打开浓盐酸时,瓶口出现白雾,说明浓盐酸具有性;(2)、实验室常用金属锌与稀盐酸来制取氢气,该反应的微观示意图如图甲、乙所示,其中“
 ”表示的离子是。
”表示的离子是。  (3)、实验室选用溶质质量分数为22%的盐酸与足量的大理石制取二氧化碳时,产生二氧化碳的快慢与时间关系如图丙所示,在实验过程中发现,发生装置中的锥形瓶外壁发烫。推测图中第5~10分钟时反应快速变慢的主要原因是。
(3)、实验室选用溶质质量分数为22%的盐酸与足量的大理石制取二氧化碳时,产生二氧化碳的快慢与时间关系如图丙所示,在实验过程中发现,发生装置中的锥形瓶外壁发烫。推测图中第5~10分钟时反应快速变慢的主要原因是。 14. 稀盐酸是实验室中一种重要的试剂,用途广泛。
14. 稀盐酸是实验室中一种重要的试剂,用途广泛。 (1)、在稀盐酸的下列用途中,无法用稀硫酸代替的是(选填序号)。
(1)、在稀盐酸的下列用途中,无法用稀硫酸代替的是(选填序号)。①金属表面除锈 ②除去氯化钠中少量的氢氧化钠 ③实验室制二氧化碳
(2)、向盛有稀盐酸的烧杯中加入适量的某种固体与之反应,反应前后烧杯内溶液中主要离子种类及个数比例变化如图所示,则加入的固体可能是下列中的(选填序号)。①铁 ②碳酸钠 ③氧化铁 ④氢氧化镁
15. 下图验证二氧化碳性质的实验:已知稀盐酸和石灰石反应生成二氧化碳,CO2表示二氧化碳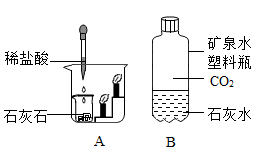 (1)、在A处能观察到两支蜡烛____(填序号)熄灭.A、从下而上 B、从上而下 C、同时(2)、根据实验A的现象可得出二氧化碳的什么物理性质:;
(1)、在A处能观察到两支蜡烛____(填序号)熄灭.A、从下而上 B、从上而下 C、同时(2)、根据实验A的现象可得出二氧化碳的什么物理性质:;还可得出的化学性质.因此可利用二氧化碳来.
(3)、在B处能观察到塑料瓶变瘪的同时,还能观察到现象,请写出该反应的文字表示式:16. 在宏观、微观和符号之间建立联系是科学学科的特点,如图是氢氧化钠与盐酸反应的示意图。 (1)、从微观粒子的变化过程可知,该反应的实质是 ;(2)、该反应属于反应(填基本反应类型)。
(1)、从微观粒子的变化过程可知,该反应的实质是 ;(2)、该反应属于反应(填基本反应类型)。四、解答题
-
17. 小科同学去柯岩风景区游玩时,捡回了若干块石灰岩,他想知道这些石灰岩中碳酸钙的含量,采用了以下的方法进行检测:取这种石灰岩样品6克,把40克稀盐酸分四次加入,测量过程所得数据见下表(已知石灰岩样品中含有的杂质不溶于水,不与盐酸反应)。
求:
加入稀盐酸的次序
1
2
3
4
加入稀盐酸的质量(克)
10
10
10
10
剩余固体的质量(克)
4.0
m
1.2
1.2
(1)、m=。(2)、样品中碳酸钙的质量是。(3)、所用稀盐酸的质量分数是多少?