上海市重点中学2022-2023学年高一下学期化学期末考试试题(等级考)
试卷更新日期:2023-08-15 类型:期末考试
一、单选题
-
1. 某Ba-Ti-O晶体具有良好的电学性能,其晶胞为立方晶胞(如图),晶胞边长为a pm。设阿伏加德罗常数的值为 , 下列说法错误的是
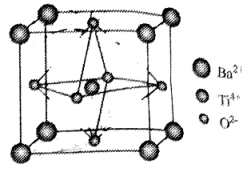 A、化学式为 B、和间的最短距离为 C、该晶胞中与等距离且最近的有4个 D、晶体的密度为
A、化学式为 B、和间的最短距离为 C、该晶胞中与等距离且最近的有4个 D、晶体的密度为二、填空题
-
2. 工业生产中涉及某些气态化合物是重要的化工原料,如、等有害气体,不能直接排放到大气中,但可以根据它们的性质避害趋利,用来制备多种重要的化学试剂。(1)、为了测定空气中的含量,将空气样品通入盛有400mL 0.1mol/L酸性溶液的密闭容器中,发生的离子反应方程式为。(2)、若管道中空气流量为a L/min,经过8min溶液恰好褪色,假定样品中被充分吸收,该空气样品中的含量为g/L。(假设空气中其他气体不与酸性溶液反应)3. 若用碱液吸收工业尾气中的后,得到等物质的量浓度的和溶液。继续向溶液中滴入几滴溶液变浑浊,请写出发生反应的离子方程式。4. 高效储氢材料被公认为氢能产业化进程中的关键,近年来,富氢含硼材料日渐成为储氢材料领域突出的研究热点。两种硼氢化物的熔点如下表所示:
硼氢化物
熔点/℃
400
-64.5
判断是晶体;是晶体。
5.向的含硫废水中加入适量溶液,产生黑色沉淀且溶液的pH降低。、、在水溶液中的物质的量含物分数随pH的分布曲线如图
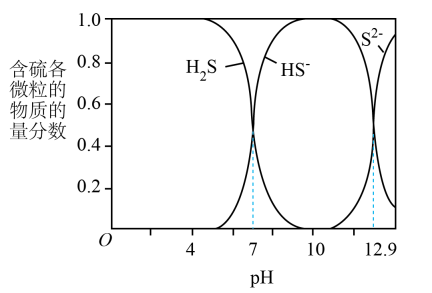 (1)、水溶液中存在电离平衡和。下列关于溶液的说法正确的是_____A、滴加新制氯水,平衡向左移动,溶液pH减小 B、加水,平衡向右移动,溶液中氢离子浓度增大 C、通入过量气体,平衡向左移动,溶液pH增大 D、加入少量硫酸铜固体(忽略体积变化),溶液中所有离子的浓度都减小(2)、pH≈10时,溶液中硫元素的主要存在形态为。(3)、用化学平衡移动原理解释向pH≈10的含硫废水中加入溶液后pH降低的原因:。(4)、
(1)、水溶液中存在电离平衡和。下列关于溶液的说法正确的是_____A、滴加新制氯水,平衡向左移动,溶液pH减小 B、加水,平衡向右移动,溶液中氢离子浓度增大 C、通入过量气体,平衡向左移动,溶液pH增大 D、加入少量硫酸铜固体(忽略体积变化),溶液中所有离子的浓度都减小(2)、pH≈10时,溶液中硫元素的主要存在形态为。(3)、用化学平衡移动原理解释向pH≈10的含硫废水中加入溶液后pH降低的原因:。(4)、某温度下,CuS和饱和溶液中pS和pM的关系如图所示,其中 , , 为或 , 下列说法错误的是____
 A、曲线Ⅱ代表的是 B、 C、此温度下CuS的 D、此温度下的饱和溶液中
A、曲线Ⅱ代表的是 B、 C、此温度下CuS的 D、此温度下的饱和溶液中三、实验题
-
6. 如图所示装置,将、通入中制备氯化亚砜()。
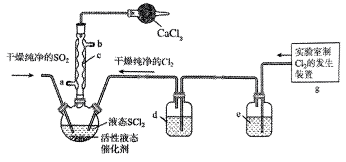
已知:①是一种液态化合物,沸点为77℃;②遇水剧烈反应,液面上产生白雾,并有刺激性气味的气体产生。请回答以下问题:
(1)、下列固体药品均可与反应制备 , 最不适合的是____。A、 B、 C、(2)、装置e中的试剂为。(3)、写出制备的化学方程式。(4)、若反应中向过量中共计通入的体积为925mL(STP),的体积为896mL(STP),最后得到产品4.76g , 则的产率(实际产量与理论产量之比)为。7. 完成下列问题。(1)、I.食醋的有效成分主要为醋酸(用HAc表示)。25℃时,HAc的。某小组研究25℃下HAc电离平衡的影响因素。提出假设:稀释HAc溶液或改变浓度,HAc电离平衡会发生移动。设计方案并完成实验:用浓度均为0.1的HAc和NaAc溶液,按下表配制总体积相同的系列溶液;测定pH,记录数据。
配制250mL 0.1000 的HAc溶液,需要的定量仪器是 , 需5HAc溶液的体积为mL。序号
pH
Ⅰ
40.00
0
2.86
Ⅱ
4.00
/
36.00
0
3.36
…
Ⅶ
4.00
a
b
3∶4
4.53
Ⅷ
4.00
4.00
32.00
1∶1
4.65
(2)、根据表中信息,补充数据: , 。(3)、由实验Ⅰ和Ⅱ可知,稀释HAc溶液,电离平衡(填”正”或”逆”)向移动;结合表中数据,给出判断理由:。(4)、II.查阅资料获悉:一定条件下,按配制的溶液中,的值等于HAc的对比数据发现,实验Ⅷ中pH=4.65与资料数据存在一定差异;推测可能由HAc浓度不够准确引起,故先准确测定HAc溶液的浓度再验证。用移液管取20.00mL HAc溶液于锥形瓶中,加入2滴酚酞溶液,用0.1000 mol/L NaOH溶液滴定至终点,判断滴定至终点的现象是。
(5)、若测定结果偏低,可能原因是____(双选)A、滴定管用蒸馏水洗净后未用氢氧化钠润洗 B、盛装待测液的锥形瓶水洗后未烘干 C、滴定过程中振荡锥形瓶时不慎有少量液体溅出 D、滴定前滴定管内无气泡,滴定后滴定管内出现气泡。(6)、滴定过程共消耗NaOH体积为22.08mL,则该HAc溶液的浓度为。四、元素或物质推断题
-
8. 下图转化关系中,A是一种盐,B是气态氯化物,C是单质,F是强酸。且A、B、C、D、E、F中均含有同一种元素。当X无论是强酸还是强碱时都有如下转化关系(其他反应产物及反应所需条件均已略去),则A物质可以是。
五、结构与性质
-
9. N、P、Sb原子的最外层电子数都是5,与卤素原子形成的化合物有广泛用途。是液晶显示器生产过程中常用的化学清洗剂,可用于面粉的漂白和杀菌,广泛应用于农药、杀虫剂的制造,常用于有机反应催化剂。(1)、几种化学键的键能如下表所示:
化学键
键能/
941.6
154.8
283.0
由两种单质化合形成1mol , 焓变。
(2)、已知:常温常压下为无色气体,熔点-129℃,沸点-207℃;为黄色油状液体,熔点-40℃,沸点70℃,95℃以上易爆炸。根据物质结构知识和题中信息解释以下问题:①热稳定性高于:。
②熔、沸点高于:。
(3)、在水中溶解度不大,而在水中溶解度较大,由此判断是分子,是分子。(填“极性”或“非极性”)10. 离子液体也叫室温离子液体,是一种只由离子组成,但在低温下也能以液态稳定存在物质,是一种很有研究价值的溶剂。(1)、最常见的离子液体主要由阴离子和如图的正离子组成。为了使正离子以单个形式存在以获得良好的溶解性能,与N原子相连的不能被H原子替换,从氢键角度解释原因是:。 (2)、硝酸乙基铵[]是人类发现的第一种常温离子液体,其熔点为12℃。已知结合质子的能力比略强,下列有关硝酸乙基铵的说法正确的是____(双选)A、该离子液体不易挥发,可用作绿色溶剂 B、该物质在常温下不能导电 C、该离子液体阴阳离子体积很大,结构松散,作用力弱 D、同温同物质的量浓度的硝酸乙基铵溶液和硝酸铵溶液相比前者的pH小
(2)、硝酸乙基铵[]是人类发现的第一种常温离子液体,其熔点为12℃。已知结合质子的能力比略强,下列有关硝酸乙基铵的说法正确的是____(双选)A、该离子液体不易挥发,可用作绿色溶剂 B、该物质在常温下不能导电 C、该离子液体阴阳离子体积很大,结构松散,作用力弱 D、同温同物质的量浓度的硝酸乙基铵溶液和硝酸铵溶液相比前者的pH小六、原理综合题
-
11. 甲醇()是一种可再生能源,由制备甲醇的过程可能涉及的反应如下:
反应Ⅰ:
反应Ⅱ:
反应Ⅲ:
(1)、反应Ⅱ的。(2)、反应Ⅲ的0(填“<”或“>”),在(填“较低温度”、“较高温度”或“任何温度”)下能够自发进行。(3)、恒温、恒容密闭容器中,对于反应Ⅰ,下列说法中能说明该反应达到化学平衡状态的是____。A、混合气体的密度不再变化 B、混合气体的平均相对分子质量不再变化 C、、、、的物质的量之比为1∶3∶1∶1(4)、对于反应Ⅰ,不同温度对的转化率及催化剂的效率影响如图所示,下列有关说法不正确的是____(双选)。 A、其他条件不变,若不使用催化剂,则250℃时的平衡转化率仍位于M B、温度低于250℃时,随温度升高甲醇的产率增大 C、使用催化剂时,M点的正反应速率小于N点的正反应速率 D、M点时平衡常数比N点时平衡常数大(5)、若在1L密闭容器中充入3 mol 和1mol 发生反应Ⅰ,则图中M点时,产物甲醇的体积分数为;该温度下,反应的平衡常数。(均保留3位有效数字)(6)、反应Ⅱ在其他条件相同、不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,反应相同时间后,的转化率随反应温度的变化如右图所示。请判断a点所处的状态是不是化学平衡状态并说明理由。
A、其他条件不变,若不使用催化剂,则250℃时的平衡转化率仍位于M B、温度低于250℃时,随温度升高甲醇的产率增大 C、使用催化剂时,M点的正反应速率小于N点的正反应速率 D、M点时平衡常数比N点时平衡常数大(5)、若在1L密闭容器中充入3 mol 和1mol 发生反应Ⅰ,则图中M点时,产物甲醇的体积分数为;该温度下,反应的平衡常数。(均保留3位有效数字)(6)、反应Ⅱ在其他条件相同、不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,反应相同时间后,的转化率随反应温度的变化如右图所示。请判断a点所处的状态是不是化学平衡状态并说明理由。 12. NaClO溶液中逐滴滴入溶液,滴加过程中溶液的pH随溶液的体积的变化曲线及实验现象。
12. NaClO溶液中逐滴滴入溶液,滴加过程中溶液的pH随溶液的体积的变化曲线及实验现象。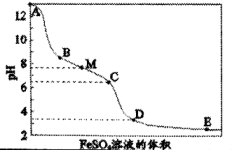
实验现象
ⅰ.A→B产生红褐色沉淀
ⅱ.B→C红褐色沉淀的量增多
ⅲ.C→D红褐色沉淀的量增多
ⅳ.D点附近产生有刺激性气味的气体
ⅴ.D→E红褐色沉淀的量略有增多
(1)、NaClO的电子式是 , 次氯酸钠溶液中离子浓度大小顺序是:(2)、下列关于NaClO溶液说法正确的是____(双选)A、0.01mol/L溶液中, B、长期露置在空气中,释放 , 漂白能力减弱 C、通入过量 , 反应的离子方程式为 D、25℃,pH=7.0的NaClO和HClO的混合溶液中,(3)、25℃,pH=7.0的NaClO和HClO的混合溶液中,[HClO](填<,>或=)(4)、A→B,C→D过程溶液的pH值下降的原因可用下面的方程式来解释,请推测方框里的物质并在横线上写出完整的方程式并配平:①。
②。
(5)、已知的 , , 少量通入NaClO溶液中发生的离子反应方程式为:。
-
-