四川省攀枝花市东区2023年中考二模化学试题
试卷更新日期:2023-08-10 类型:中考模拟
一、单选题
-
1. 下列物品的主要制作材料中属于天然高分子材料的是( )A、羊毛围巾 B、合成橡胶手套 C、玻璃杯 D、尼龙绳2. 化学实验室存放浓硫酸的药品柜上应贴的标志是是( )A、
 B、
B、 C、
C、 D、
D、 3. 下列符号能表示两个氢原子的是( )A、H2 B、2H2 C、2H D、2H+4. 2022年4月16日,神舟十三号载人飞船返回舱在东风着陆场成功着陆。航天员在空间站工作生活了183天,在空间站的生活离不开氧气。下列有关氧气的说法正确的是( )A、氧气的化学性质很不活泼 B、氧气极易溶于水 C、空气中含量最多的气体是氧气 D、氧气能供给呼吸5. 分类是学习化学的方法之一,下列各组物质按单质、氧化物、碱的顺序排列的一组是( )A、Zn、KClO3、NH3·H2O B、H2、H2O、NaOH C、O2、NaOH、H2SO4 D、C、MgO、Cu2(OH)2CO36. 下课要走出教室呼吸新鲜空气,避免头昏。下课前的教室内二氧化碳的体积分数可能是( )A、0.03% B、0.10% C、21% D、78%7. 用“分子的观点”解释下列现象,不正确的是( )A、水结成冰——分子停止运动 B、水加糖变甜——分子不停地运动 C、粥变馊——分子发生变化 D、液化气被压缩进钢瓶——分子间有间隙8. 2月13日,指导“三农”工作的2023年中央一号文件公布。耕地保护是农业的首要问题,下列利用化学知识保护耕地的说法中,错误的是( )A、土壤有肥力粮食才高产,农业上需要大量施用化肥 B、土壤酸化板结,可以施用适量的熟石灰来进行改良 C、植物从土壤里获得各种养分,大多以溶液的形式被吸收的 D、就地焚烧农作物秸秆,容易造成环境污染,破坏土壤结构9. 下表是几种作物适宜生长的pH范围:某地土壤呈碱性,则该地适宜种植的作物是( )
3. 下列符号能表示两个氢原子的是( )A、H2 B、2H2 C、2H D、2H+4. 2022年4月16日,神舟十三号载人飞船返回舱在东风着陆场成功着陆。航天员在空间站工作生活了183天,在空间站的生活离不开氧气。下列有关氧气的说法正确的是( )A、氧气的化学性质很不活泼 B、氧气极易溶于水 C、空气中含量最多的气体是氧气 D、氧气能供给呼吸5. 分类是学习化学的方法之一,下列各组物质按单质、氧化物、碱的顺序排列的一组是( )A、Zn、KClO3、NH3·H2O B、H2、H2O、NaOH C、O2、NaOH、H2SO4 D、C、MgO、Cu2(OH)2CO36. 下课要走出教室呼吸新鲜空气,避免头昏。下课前的教室内二氧化碳的体积分数可能是( )A、0.03% B、0.10% C、21% D、78%7. 用“分子的观点”解释下列现象,不正确的是( )A、水结成冰——分子停止运动 B、水加糖变甜——分子不停地运动 C、粥变馊——分子发生变化 D、液化气被压缩进钢瓶——分子间有间隙8. 2月13日,指导“三农”工作的2023年中央一号文件公布。耕地保护是农业的首要问题,下列利用化学知识保护耕地的说法中,错误的是( )A、土壤有肥力粮食才高产,农业上需要大量施用化肥 B、土壤酸化板结,可以施用适量的熟石灰来进行改良 C、植物从土壤里获得各种养分,大多以溶液的形式被吸收的 D、就地焚烧农作物秸秆,容易造成环境污染,破坏土壤结构9. 下表是几种作物适宜生长的pH范围:某地土壤呈碱性,则该地适宜种植的作物是( )作物
马铃薯
茶树
水稻
莲
pH
4.8~5.5
5.0~5.5
6.0~7.0
8.0~9.0
A、马铃薯 B、茶树 C、水稻 D、莲10. “比较”是常用的学习方法之一,下列通过比较产生的排序正确的是( )A、粒子体积从大到小:分子>原子>电子 B、净化水的程度由高到低;蒸馏>过滤>沉淀 C、微粒质量由大到小:二氧化硫分子>硫酸根离子>铜原子 D、相同质量的钠镁铝三种金属所含原子由多到少:铝>镁>钠11. 近期,我国科学家成功研制出天然气(主要成分为甲烷CH4)在液态锡催化作用下的高效制氢设备,该设备发生反应的微观原理如图所示,下列说法错误的是( )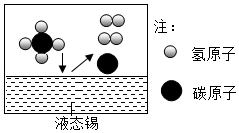 A、甲烷是由碳原子和氢分子构成 B、反应前后液态锡的质量和化学性质不变 C、该反应为分解反应 D、保持甲烷化学性质的最小粒子是甲烷分子12. 实验室电解水的装置示意图如下。下列说法正确的是( )
A、甲烷是由碳原子和氢分子构成 B、反应前后液态锡的质量和化学性质不变 C、该反应为分解反应 D、保持甲烷化学性质的最小粒子是甲烷分子12. 实验室电解水的装置示意图如下。下列说法正确的是( ) A、甲管中产生氧气 B、电源负极与乙管电极相连 C、产生的氢气和氧气质量比为2:1 D、电解的实质是氢原子和氧原子的重新组合13. 逻辑推理是学习化学常用的思维方法,下列推理正确的是( )A、酸中都含有氢元素,所以含有氢元素的化合物一定是酸 B、单质只含有一种元素,所以含一种元素的纯净物一定是单质 C、元素的种类由质子数决定,则质子数相同的微粒一定属于同种元素 D、盐中含金属离子和酸根离子,硝酸铵中不含金属离子,不属于盐类14. 下列有关实验室制取和收集氧气、二氧化碳和氢气的说法,正确的是( )
A、甲管中产生氧气 B、电源负极与乙管电极相连 C、产生的氢气和氧气质量比为2:1 D、电解的实质是氢原子和氧原子的重新组合13. 逻辑推理是学习化学常用的思维方法,下列推理正确的是( )A、酸中都含有氢元素,所以含有氢元素的化合物一定是酸 B、单质只含有一种元素,所以含一种元素的纯净物一定是单质 C、元素的种类由质子数决定,则质子数相同的微粒一定属于同种元素 D、盐中含金属离子和酸根离子,硝酸铵中不含金属离子,不属于盐类14. 下列有关实验室制取和收集氧气、二氧化碳和氢气的说法,正确的是( ) A、用装置①④制取和收集氧气,相关反应的化学方程式为 B、用装置②制取二氧化碳,不仅可随时添加酸液,还可控制反应的速率 C、用装置③制取二氧化碳,若多孔隔板改成隔离铜网,同样可以制取 D、如用装置⑤收集氢气,则气体应从a端通入15. 在反应X+2Y=R+2M中已知R和M的相对分子质量之比为22:9,当1.6gX与Y恰好完全反应时,生成4.4gR,则在此反应中Y与M的质量比为( )A、1:1 B、9:22 C、16:9 D、9:1616. 由两种金属组成的混合物5.6g与足量的稀硫酸完全反应后得到0.23g氢气,则金属混合物的组成可能是( )A、铁和铜 B、铝和镁 C、铁和铝 D、铁和锌
A、用装置①④制取和收集氧气,相关反应的化学方程式为 B、用装置②制取二氧化碳,不仅可随时添加酸液,还可控制反应的速率 C、用装置③制取二氧化碳,若多孔隔板改成隔离铜网,同样可以制取 D、如用装置⑤收集氢气,则气体应从a端通入15. 在反应X+2Y=R+2M中已知R和M的相对分子质量之比为22:9,当1.6gX与Y恰好完全反应时,生成4.4gR,则在此反应中Y与M的质量比为( )A、1:1 B、9:22 C、16:9 D、9:1616. 由两种金属组成的混合物5.6g与足量的稀硫酸完全反应后得到0.23g氢气,则金属混合物的组成可能是( )A、铁和铜 B、铝和镁 C、铁和铝 D、铁和锌二、填空题
-
17. 如图中的①、②是氟元素、钙元素在元素周期表中的信息,A、B、C、D、E是五种粒子的结构示意图。
 请回答:(1)、钙元素属于(填“金属”或“非金属”)元素;(2)、图中X= , C可以用符号表示;(3)、A、B、C、D、E属于同种元素的粒子是(填序号);(4)、A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似(填序号);(5)、②与B形成化合物的原子个数比。
请回答:(1)、钙元素属于(填“金属”或“非金属”)元素;(2)、图中X= , C可以用符号表示;(3)、A、B、C、D、E属于同种元素的粒子是(填序号);(4)、A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似(填序号);(5)、②与B形成化合物的原子个数比。三、综合应用题
-
18. 从科学家认识物质的视角认识。(1)、微观角度
我国研制的一种新型催化剂可将和转化为甲醇和X。若用“
 ”表示氢原子,“
”表示氢原子,“ ”表示氧原子,“
”表示氧原子,“ ”表示碳原子,该反应的微观示意如图1,写出X的化学式。
”表示碳原子,该反应的微观示意如图1,写出X的化学式。 (2)、性质角度
(2)、性质角度将蘸有酒精的棉芯点燃放入烧杯中,向烧杯中缓缓倾倒二氧化碳,观察到烧杯中的棉芯自下而上熄灭,如图2所示。说明二氧化碳具有的性质有。若使棉芯下半段立即恢复燃烧,操作方法是。
(3)、应用角度Ⅰ.可用如图3所示方法自制汽水来消暑解热。制汽水时,与柠檬酸反应生成柠檬酸钠、二氧化碳和水。

①柠檬酸中的阳离子是(填离子符号)。
②自制汽水需要冷藏。说明气体在水中的溶解度与有关。
Ⅱ.电池是一种新型电池。
③电池的工作原理:在的催化下,Al与发生化合反应生成。写出此反应的化学方程式
四、填空题
-
19. 化学就在我们身边,它能改善我们的生活。请回答下列问题:(1)、化石燃料包括煤、石油、;(2)、用洗洁精洗去餐具上的油污,这是利用洗洁精的作用;(3)、生活中可以用的方法,既可以消灭细菌,也可以降低水的硬度;(4)、用嘴吹灭燃着的生日蜡烛,利用的主要灭火原理是;(5)、生活中我们常说“先菜后盐”,即加碘食盐中含碘的物质是碘酸铆,碘酸钾受热易分解,影响人体对碘的摄入。加碘食盐中的“碘”指的是(填“分子”“原子”或“元素”)。
五、科普阅读题
-
20. 铅元素符号Pb,原子序数82,相对原子质量207.2,是IVA族(碳族)金属。熔点327.502℃,沸点1740℃,化合价+2,+4.铅是一种略带蓝色的银白色金属,常温下在干燥的空气中性质稳定,但随着温度升高被空气中的氧气氧化,形成灰黑色的氧化铅,所以我们看到的铅常是灰色的。铅的延性弱,展性强,抗腐蚀性高,抗放射性穿透的性能好。由于性能优良,铅、铅的化合物及其合金被广泛应用于蓄电池、电缆护套、机械制造、船舶制造、轻工、氧化铅等行业。
 (1)、铅的核电荷数为 , 最外层电子数为个。(2)、医院中用放射治疗的方法治疗癌症,常用的放射源为钴 , 在运输过程中通常贮藏在铅罐中,原因是。(3)、用铅单质与二氧化铅制造铅蓄电池(如上图),放电时会生成+2价的铅盐及另一种物质,请写出铅蓄电池化学方程式。
(1)、铅的核电荷数为 , 最外层电子数为个。(2)、医院中用放射治疗的方法治疗癌症,常用的放射源为钴 , 在运输过程中通常贮藏在铅罐中,原因是。(3)、用铅单质与二氧化铅制造铅蓄电池(如上图),放电时会生成+2价的铅盐及另一种物质,请写出铅蓄电池化学方程式。六、填空题
-
21. 磷酸二氢钾为白色粉末,置于空气中易潮解,常作为无土栽培营养液成分之一、如图1是磷酸二氢钾(用A表示)的溶解度曲线图。图2是M,N两点代表的溶液相互转化的途径路线图(”→“表示转化方向)。
 (1)、磷酸二氢钾可以提高果实的结果率,磷酸二氢钾属于肥。(2)、图1中℃时,N点对应的溶液为(填“饱和溶液”或“不饱和溶液”)。图2中,采取“先加水至N点对应的溶质质量分数再升温到℃”这一措施来实现M→N转化的途径路线是(填序号)。(3)、实验室要配制图1中M点的饱和溶液100g,需磷酸二氢钾的质量为。(4)、经检测,同学配制的溶液溶质质量分数偏小,可能的原因是____(填序号)。A、溶解时烧杯内壁有水珠 B、量取溶剂时,仰视读数 C、装瓶时有少量溶液洒出
(1)、磷酸二氢钾可以提高果实的结果率,磷酸二氢钾属于肥。(2)、图1中℃时,N点对应的溶液为(填“饱和溶液”或“不饱和溶液”)。图2中,采取“先加水至N点对应的溶质质量分数再升温到℃”这一措施来实现M→N转化的途径路线是(填序号)。(3)、实验室要配制图1中M点的饱和溶液100g,需磷酸二氢钾的质量为。(4)、经检测,同学配制的溶液溶质质量分数偏小,可能的原因是____(填序号)。A、溶解时烧杯内壁有水珠 B、量取溶剂时,仰视读数 C、装瓶时有少量溶液洒出七、流程题
-
22. 氧化锌软膏用于急性皮炎、湿疹、痱子及轻度皮肤溃疡,其有效成分氧化锌(ZnO)是一种白色固体。一种工业生产药用高纯氧化锌的流程如图:

说明:“沉锌”意为使锌元素转化为沉淀物
(1)、“酸溶”所达到的目的是将锌块转化为可溶于水的(填化学式)。(2)、由草酸铵的化学式推测草酸的化学式为 , 草酸中C的化合价是。(3)、“沉锌”过程中发生反应的化学方程式为。(4)、“操作A”的名称是。(5)、溶液X结晶所得化肥是该工艺有价值的副产品,证明它是一种铵态氨肥的方法是取少量样品与粉末(填药品俗称)混合、研磨,能嗅到氨味。八、推断题
-
23. 下图表示元素的化合价与物质类别的关系,“→”表示物质之间可以转化。A、B、C、D、E、F、G是初中化学所学物质,分别由H、O、S、Cl、K、Ba中的一种、两种或三种元素组成。请回答:
 (1)、A和E的化学式分别为和。(2)、D与G反应的化学方程式为 , 此反应属(填基本反应类型)。(3)、A—G物质间,发生中和反应的化学方程式为。
(1)、A和E的化学式分别为和。(2)、D与G反应的化学方程式为 , 此反应属(填基本反应类型)。(3)、A—G物质间,发生中和反应的化学方程式为。九、实验题
-
24. 用如图装置完成下列实验(夹持仪器略去,、均关闭)。
 (1)、本实验装置使用分液体漏斗的优点是(至少写一条)。(2)、打开 , 放入适量稀盐酸,立即关闭 , 观察到A中有大量气泡产生。发生反应的化学方程式为 , 烧杯中石蕊溶液由紫色变为色。(3)、移开烧杯,按下表进行实验i或实验ⅱ,证明了反应后A中还有碳酸盐。请完成各现象。
(1)、本实验装置使用分液体漏斗的优点是(至少写一条)。(2)、打开 , 放入适量稀盐酸,立即关闭 , 观察到A中有大量气泡产生。发生反应的化学方程式为 , 烧杯中石蕊溶液由紫色变为色。(3)、移开烧杯,按下表进行实验i或实验ⅱ,证明了反应后A中还有碳酸盐。请完成各现象。操作
现象
实验i
打开
稀盐酸流入A中,①
实验ⅱ
打开
A中液体流入锥形瓶②
十、科学探究题
-
25. 我国已成长为一个高铁大国,高铁运营里程居世界第一,高铁建设大国的背后,离不开攀钢对百米重轨的有效支持,目前已建设的高铁线路中,有70%的轨道来自我市,某学习小组对攀钢炼钢厂的某型号的钢铁锈蚀进行探究。
【提出问题】铁锈蚀与哪些因素有关。
【查阅资料】碳粉可加快铁的锈蚀,碳粉不与盐酸反应;氧化铁能与盐酸反应,不产生气体。
【设计实验】
实验一:定性探究铁锈蚀的因素
取四枚大小相同的洁净某型号无锈铁钉分别放入试管,进行图1实验,现象如下表。



试管编号
A
B
C
D
一周后铁钉表面现象
有一层铁锈
无明显变化
无明显变化
有较厚铁锈
(1)、对比AB、C试管中实验现象,说明铁锈蚀是与空气中的发生化学反应。(2)、对比A和D试管中实验现象,说明铁锈蚀快慢与(填化学式)有关;(3)、据图3,说明铁生锈是(填“放热”或“吸热”),~这段时间反应并未停止但温度却开始降低,原因是(4)、据图2、图4分析时刻后压强突然变大,原因是。(5)、连接如图5装置。取部分生锈的铁粉(铁和氧化铁的混合物)0.6g于锥形瓶中,加入足量稀盐酸进行实验。完全反应后,测得生成气体体积为0.2L,已知该条件下氢气密度为0.09g/L,根据以上数据,请计算该固体中铁的质量分数是。 (6)、【反思评价】
(6)、【反思评价】学习小组有同学提出:用这种方法测得的气体体积不够准确,可能会导致测定的铁的质量分数变大,可能的原因是____(填序号)。
A、装置的气密性不好 B、铁与盐酸反应放热 C、生成的气体会部分滞留在锥形瓶中 D、没有扣掉加入的盐酸的体积十一、计算题
-
26. 为了测定某牛奶样品中蛋白质的含量,现采用“盖尔达法”分解其中的蛋白质。其原理是把蛋白质中的氮元素完全转化成氨气,再用稀硫酸吸收氨气,反应的化学方程式: , 现取该牛奶样品30mL,用“盖尔达法”分解其中的蛋白质,产生的氨气用9.5g溶质质量分数为4.9%的稀硫酸恰好完全吸收。计算并回答下列问题:
配料:鲜牛奶
保质期:8个月
净含量:250mL
营养成分(每100mL)钙≥0.11g
脂肪≥3.30g
蛋白质≥2.90g
(1)、30mL牛奶中含氮元素的质量是多少克?(计算结果精确到0.01g,下同)(2)、如图是该牛奶包装标签的部分内容。已知牛奶中的蛋白质含氮元素的质量分数为16%,请你通过计算确定,该牛奶样品中蛋白质的含量是否达到了包装标签所标示的蛋白质的质量标准。
-
-
-
-
-
-
-
-
-