四川省广元市朝天区2023年中考第一次诊断化学试题
试卷更新日期:2023-08-10 类型:中考模拟
一、单选题
-
1. 变化观是化学基本观念之一,下列变化中,属于化学变化的是( )A、金属拉成丝 B、盐酸除铁锈 C、空气液化 D、蔗糖溶解2. 下列物质的名称(俗称)、化学式、类别都正确的是( )A、水银、Ag、单质 B、干冰、、氧化物 C、烧碱、、碱 D、甲烷、、无机物3. 健康生活离不开化学。下列叙述正确的是( )A、米饭、面条中含有的主要营养物质是蛋白质 B、合理使用含氟牙膏可以预防龋齿 C、明矾常用于自来水的杀菌消毒 D、铁强化酱油中的铁是指铁单质4. 下列仪器不能加热的是( )A、烧杯 B、试管 C、量筒 D、燃烧匙5. 嫦娥五号采集的月壤样品中存在氦-3(含有2个质子和1个中子的氦原子)。氦元素在元素周期表中的信息如下图,下列有关氦元素的说法错误的是( )
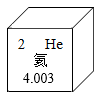 A、属于稀有气体元素 B、元素符号为He C、氦-3的原子结构示意图为
A、属于稀有气体元素 B、元素符号为He C、氦-3的原子结构示意图为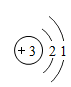 D、氦原子在化学反应中不易失去电子
6. 蓝莓富含花青素(C15H11O6)。花青素是一种水溶性色素,颜色与细胞液的酸碱性有关,酸性时为红色,碱性时为蓝色。下列有关说法正确的是( )A、花青素是有机物 B、花青素中碳、氢、氧的质量比为15:11:6 C、花青素由碳原子、氢原子、氧原子构成 D、在氢氧化钠溶液中滴入蓝莓汁液,溶液呈红色7. 下列实验方案设计正确的是。( )
D、氦原子在化学反应中不易失去电子
6. 蓝莓富含花青素(C15H11O6)。花青素是一种水溶性色素,颜色与细胞液的酸碱性有关,酸性时为红色,碱性时为蓝色。下列有关说法正确的是( )A、花青素是有机物 B、花青素中碳、氢、氧的质量比为15:11:6 C、花青素由碳原子、氢原子、氧原子构成 D、在氢氧化钠溶液中滴入蓝莓汁液,溶液呈红色7. 下列实验方案设计正确的是。( )选项
实验目的
实验方案
A
鉴别硫酸钾和碳酸氢铵
闻气味
B
除去硝酸钾溶液中的氯化钾
加入过量硝酸银溶液
C
由氧化铜制取氢氧化铜
直接加入NaOH溶液
D
检测正常雨水的pH是否等于5.6
用pH试纸测定
A、A B、B C、C D、D8. 为了探究“烧不坏的手帕”原理,将滤纸(着火点 130℃)浸在不同浓度的酒精溶液中,进行如图 1 所示实验,并收集实验过程滤纸中心温度,绘制曲线如图 2所示,下列说法错误的是( )
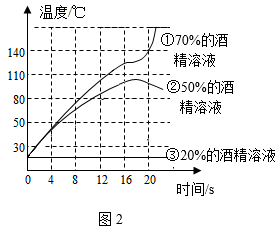 A、曲线 1 在 20 s 时温度突然升高的原因是滤纸燃烧 B、曲线 2 的温度始终没有达到滤纸的着火点,滤纸不燃烧 C、曲线 3 所示的温度没有明显变化,是酒精没有与氧气接触 D、“烧不坏的手帕”原理是液体汽化吸热使其温度达不到着火点9. 20℃时,向盛有100g水的烧杯中加入60 g ZnSO4进行实验(忽略水的蒸发)。依据下图所示的实验和ZnSO4溶解度曲线,下列说法正确的是( )
A、曲线 1 在 20 s 时温度突然升高的原因是滤纸燃烧 B、曲线 2 的温度始终没有达到滤纸的着火点,滤纸不燃烧 C、曲线 3 所示的温度没有明显变化,是酒精没有与氧气接触 D、“烧不坏的手帕”原理是液体汽化吸热使其温度达不到着火点9. 20℃时,向盛有100g水的烧杯中加入60 g ZnSO4进行实验(忽略水的蒸发)。依据下图所示的实验和ZnSO4溶解度曲线,下列说法正确的是( )
 A、20℃时,充分搅拌后烧杯中溶液的质量为160g B、升温到40℃时,烧杯中的溶液为饱和溶液 C、从60℃升温到80℃时,烧杯内溶液中溶质的质量分数减小 D、100℃时,烧杯内溶液中溶质的质量分数为37.5%10. 在研究物质的组成时,等效思维是一种常用的解题技巧,如:可将HCOOH视为。现有由CO、HCOOH、OHC—COOH组成的混合物,测得氢元素的质量分数为y,则碳元素的质量分数为( )A、 B、 C、 D、
A、20℃时,充分搅拌后烧杯中溶液的质量为160g B、升温到40℃时,烧杯中的溶液为饱和溶液 C、从60℃升温到80℃时,烧杯内溶液中溶质的质量分数减小 D、100℃时,烧杯内溶液中溶质的质量分数为37.5%10. 在研究物质的组成时,等效思维是一种常用的解题技巧,如:可将HCOOH视为。现有由CO、HCOOH、OHC—COOH组成的混合物,测得氢元素的质量分数为y,则碳元素的质量分数为( )A、 B、 C、 D、二、填空题
-
11. 化学与生产、生活息息相关。(1)、合成材料的应用和发展大大方便了人类的生活。下列常用物品的主要成分不属于合成材料的是(填序号)。
①有机玻璃 ②羊毛西服 ③汽车轮胎 ④塑料雨衣
(2)、生活中既能杀菌又能降低水的硬度的做法是。(3)、洗洁精除去餐具上的油污,利用的是洗洁精的作用。(4)、新鲜蔬菜、水果中富含的营养素有水和。(5)、炒菜时油锅着火立即向锅内倒入冷油,利用的灭火原理是。12. 阅读材料,回答问题。空气又称大气,是包围地球的气体混合物的总称,除水蒸气外,大气的组成基本上是稳定的,主要含有、、、等气体。空气是生命、燃烧和工业等所需要的氧的主要来源,空气是重要的工业原料。
(1)、空气中,体积分数约占的气体是(填化学用语)。(2)、分离液态空气制是利用了和的不同,淡蓝色钢瓶中存放的液态氧气的构成微粒是(填化学用语)。(3)、英国科学家瑞利在研究空气中的密度时,测出除杂后的密度总是大于标准值。你认为瑞利实验除杂后的中最可能含有的气体是____(填序号)。A、 B、 C、 D、Ar(4)、下图是某地去年空气中各污染物浓度月均变化图。
分析图像,空气中臭氧()浓度较高的月份是4月和月,CO与在1月及12月较高的可能原因是。
三、流程题
-
13. 氯化钠是重要的调味品,也是重要的化工原料。某化工厂使用食盐和其他原料,采用侯德榜先生的联合制碱法生产纯碱,主要化工流程如下图所示:
 (1)、操作Ⅰ的名称是。(2)、反应②的化学方程式为。(3)、利用电解饱和食盐水(选填“能”或“不能”)得到纯碱,理由是。(4)、上述化工流程中能体现绿色化学思想的设计是。
(1)、操作Ⅰ的名称是。(2)、反应②的化学方程式为。(3)、利用电解饱和食盐水(选填“能”或“不能”)得到纯碱,理由是。(4)、上述化工流程中能体现绿色化学思想的设计是。四、填空题
-
14. 铬(Cr)是一种银白色金属,在空气中能形成一层致密的氧化物薄膜。铬的上述性质与常见金属(填名称)相似,其中属于化学性质的是。把铬片放入稀硫酸中,铬片上有气泡产生,溶液逐渐变成蓝色,这是因为生成了亚铬(+2价)盐,写出该反应的化学方程式。
五、实验题
-
15. 如图是实验室制取CO2及进行性质实验的部分装置。
 (1)、 CaCO3固体与稀盐酸反应生成CO2气体的化学方程式是。(2)、检验装置气密性,按图连接装置,先 , 再加水至 A下端形成一段水柱,静置,若观察到 , 说明气密性良好。(3)、加入药品。添加块状CaCO3固体时,为避免打破锥形瓶,应将锥形瓶 , 再放入固体。添加盐酸时,将稀盐酸从 (填仪器A的名称)倒入锥形瓶至。(4)、如图所示,向放置有燃着的蜡烛的烧杯中倒入CO2 , 观察到的现象是。
(1)、 CaCO3固体与稀盐酸反应生成CO2气体的化学方程式是。(2)、检验装置气密性,按图连接装置,先 , 再加水至 A下端形成一段水柱,静置,若观察到 , 说明气密性良好。(3)、加入药品。添加块状CaCO3固体时,为避免打破锥形瓶,应将锥形瓶 , 再放入固体。添加盐酸时,将稀盐酸从 (填仪器A的名称)倒入锥形瓶至。(4)、如图所示,向放置有燃着的蜡烛的烧杯中倒入CO2 , 观察到的现象是。六、科学探究题
-
16. 老师提供了五瓶无色溶液,分别是碳酸钠溶液、稀盐酸、氯化钾溶液、硫酸钠溶液和氢氧化钡溶液。为鉴别它们,同学们进行了如下探究:
[认识性质]
五种溶液两两之间能否发生复分解反应?请写出符合条件的化学方程式各一个:
(1)、有沉淀生成;(2)、中和反应。(3)、[实验探究]他们将五瓶溶液分别编号为A、B、C、D、E,然后将B、C、D、E四种溶液分别取少量,并两两混合,观察现象,记录如下:
[得出结论]B C D E B / 无明显现象 产生白色沉淀 ? C / 无明显现象 无明显现象 D / 无明显现象 E / 通过已有实验可以确定溶液A不可能是哪一种溶液?(填溶液中溶质的化学式,下同)。
(4)、分析B、E混合的可能现象,会得出不同的结论。若B、E混合有气泡产生,则可推知五种溶液的组合是:A:;B:;C:;D:;E:。七、计算题
-
17. 中华人民共和国国家标准(GB2760-2011)规定葡萄酒中SO2最大使用量为0.25g/L。某综合实践活动小组测定葡萄酒中SO2的含量,取320mL某葡萄酒(加适量稀酸),加热使SO2全部逸出,并将SO2通入足量的H2O2溶液中发生化合反应,待完全反应后,得到含溶质质量分数为0.098%的硫酸溶液100g。请回答下列问题:(1)、从上述信息可知:当压强一定时,升高温度,SO2气体在水中的溶解度。(选填“增大”、“减小”或“不变”)(2)、通过计算判断该葡萄酒中SO2的含量是否符合国家标准?(写出计算过程)
-
-
-
-