【备考2024年】高考化学全国乙卷真题变式分层精准练第6题
试卷更新日期:2023-08-04 类型:二轮复习
一、原题
-
1. 室温钠-硫电池被认为是一种成本低、比能量高的能源存储系统。一种室温钠-硫电池的结构如图所示。将钠箔置于聚苯并咪唑膜上作为一个电极,表面喷涂有硫黄粉末的炭化纤维素纸作为另一电极。工作时,在硫电极发生反应:S8+e-→S , S+e-→S , 2Na++S+2(1-)e-→Na2Sx
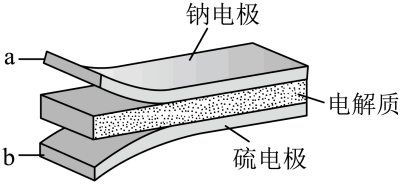
下列叙述错误的是
A、充电时Na+从钠电极向硫电极迁移 B、放电时外电路电子流动的方向是a→b C、放电时正极反应为:2Na++S8+2e-→Na2Sx D、炭化纤维素纸的作用是增强硫电极导电性能二、基础
-
2. 镉镍可充电电池的充、放电反应如下:Cd + 2NiO(OH) + 2H2OCd(OH)2 + 2Ni(OH)2。则该电池充电时阳极放电的是( )A、Cd(OH)2 B、Cd C、Ni(OH)2 D、NiO(OH)3. 我国《政府工作报告》首次写入“推动充电、加氢等设施的建设”。如图是一种新型“全氢电池”,能量效率可达。下列说法错误的是 ( )
 A、该装置将化学能转化为电能 B、离子交换膜不允许和通过 C、吸附层为负极,电极反应式为 D、电池总反应为4. 氨—空气燃料电池的结构如图所示。关于该电池的工作原理,下列说法正确的是( )
A、该装置将化学能转化为电能 B、离子交换膜不允许和通过 C、吸附层为负极,电极反应式为 D、电池总反应为4. 氨—空气燃料电池的结构如图所示。关于该电池的工作原理,下列说法正确的是( ) A、b极发生氧化反应 B、O2-由b极移向a极 C、a极的电极反应:2NH3+3O2-+6e-=N2+3H2O D、理论上消耗2molNH3 , 同时消耗33.6LO25. 电能属于可再生性能源,下列叙述正确的是( )A、火力发电能将化学能直接转化为电能 B、原电池是把化学能转化为电能的装置 C、化学电源均是安全、无污染的 D、生活中的化学电源均属于二次电池6. 实验发现,298K时,在氯化铁酸性溶液中加少量锌粒后,立即被还原成。某夏令营兴趣小组根据该实验事实设计了如图所示原电池装置。下列有关说法正确的是( )
A、b极发生氧化反应 B、O2-由b极移向a极 C、a极的电极反应:2NH3+3O2-+6e-=N2+3H2O D、理论上消耗2molNH3 , 同时消耗33.6LO25. 电能属于可再生性能源,下列叙述正确的是( )A、火力发电能将化学能直接转化为电能 B、原电池是把化学能转化为电能的装置 C、化学电源均是安全、无污染的 D、生活中的化学电源均属于二次电池6. 实验发现,298K时,在氯化铁酸性溶液中加少量锌粒后,立即被还原成。某夏令营兴趣小组根据该实验事实设计了如图所示原电池装置。下列有关说法正确的是( ) A、盐桥中的阴离子往左侧烧杯移动 B、左侧烧杯中电极上发生还原反应,溶液的红色逐渐褪去 C、电子由Zn极流出到Pt电极,再经过溶液回到Zn极,形成闭合回路 D、该电池总反应为7. 银锌电池以为正极、Zn为负极,KOH溶液作电解质,放电反应为: , 下列说法错误的是( )A、基态的价电子排布式: B、为含有极性键的非极性分子 C、的电子式:
A、盐桥中的阴离子往左侧烧杯移动 B、左侧烧杯中电极上发生还原反应,溶液的红色逐渐褪去 C、电子由Zn极流出到Pt电极,再经过溶液回到Zn极,形成闭合回路 D、该电池总反应为7. 银锌电池以为正极、Zn为负极,KOH溶液作电解质,放电反应为: , 下列说法错误的是( )A、基态的价电子排布式: B、为含有极性键的非极性分子 C、的电子式: D、放电时,电子由Zn流向
D、放电时,电子由Zn流向
三、提高
-
8. 我国科学家研发了一种室温下“可呼吸”的Na-CO2二次电池。将NaClO4溶于有机溶剂作电解液,钠和负载碳纳米管的镍网分别作电极材料,电池的总反应为3CO2+4Na
 2Na2CO3+C。下列说法错误的是( )
2Na2CO3+C。下列说法错误的是( ) A、放电时,ClO4-向负极移动 B、充电时释放CO2 , 放电时吸收CO2 C、放电时,正极反应式为3CO2+4e-=2CO32-+C D、放电时,负极反应式为Na++e-=Na9. 高铁电池是一种新型可充电电池,能长时间保持稳定的放电电压。其电池总反应为:3Zn + 2K2FeO4 + 8H2O 3Zn(OH)2 + 2Fe(OH)3 + 4KOH,下列叙述错误的是( )A、放电时负极反应为:Zn-2e-+2OH-= Zn(OH)2 B、充电时阳极发生氧化反应,附近溶液碱性增强 C、充电时每转移3mol电子,阴极有1.5molZn生成 D、放电时正极反应为:FeO42- + 3e- + 4H2O = Fe(OH)3 + 5OH-10. 肼(N2H4)暴露在空气中容易爆炸,但利用其作燃料电池是一种理想的电池,具有容量大、能量转化效率高、产物无污染等特点,其工作原理如图所示,下列叙述错误的是( )
A、放电时,ClO4-向负极移动 B、充电时释放CO2 , 放电时吸收CO2 C、放电时,正极反应式为3CO2+4e-=2CO32-+C D、放电时,负极反应式为Na++e-=Na9. 高铁电池是一种新型可充电电池,能长时间保持稳定的放电电压。其电池总反应为:3Zn + 2K2FeO4 + 8H2O 3Zn(OH)2 + 2Fe(OH)3 + 4KOH,下列叙述错误的是( )A、放电时负极反应为:Zn-2e-+2OH-= Zn(OH)2 B、充电时阳极发生氧化反应,附近溶液碱性增强 C、充电时每转移3mol电子,阴极有1.5molZn生成 D、放电时正极反应为:FeO42- + 3e- + 4H2O = Fe(OH)3 + 5OH-10. 肼(N2H4)暴露在空气中容易爆炸,但利用其作燃料电池是一种理想的电池,具有容量大、能量转化效率高、产物无污染等特点,其工作原理如图所示,下列叙述错误的是( ) A、电池工作时,正极附近的pH升高 B、当消耗1molO2时,有2molNa+由甲槽向乙槽迁移 C、负极反应为4OH-+N2H4-4e-=N2+4H2O D、若去掉离子交换膜电池不能正常工作11. 下列四个常用电化学装置的叙述错误的是 ( )
A、电池工作时,正极附近的pH升高 B、当消耗1molO2时,有2molNa+由甲槽向乙槽迁移 C、负极反应为4OH-+N2H4-4e-=N2+4H2O D、若去掉离子交换膜电池不能正常工作11. 下列四个常用电化学装置的叙述错误的是 ( )



图I水果电池
图II干电池
图III铅蓄电池
图IV氢氧燃料电池
A、图I所示电池中,电子从锌片流出 B、图II所示干电池中锌作负极 C、图III所示电池为二次电池,放电时正极的电极反应式为Pb-2e-+=PbSO4 D、图IV所示电池中正极反应为:12. 火星大气由96%的二氧化碳气体组成,火星探测器采用Li—CO2电池供电,其反应机理如图所示,下列说法错误的是( ) A、R方向为电子移动的方向 B、CO2电极反应式为4Li++4e-+3CO2=2Li2CO3+C C、可采用LiNO3溶液作为电解质溶液 D、碳酸锂的生成和分解形式提供了实现可逆电化学电池13. Mg-AgCl电池是一种能被海水激活的一次性贮备电池,电池反应方程式为Mg+2AgCl=Mg2++2Ag+2Cl-。下列说法正确的是( )A、该电池的负极反应式为Mg2++2e-=Mg B、该电池的正极反应式为Ag-e-+Cl-=AgCl C、AgCl为原电池的正极,发生了氧化反应 D、海水中的Na+向AgCl极移动
A、R方向为电子移动的方向 B、CO2电极反应式为4Li++4e-+3CO2=2Li2CO3+C C、可采用LiNO3溶液作为电解质溶液 D、碳酸锂的生成和分解形式提供了实现可逆电化学电池13. Mg-AgCl电池是一种能被海水激活的一次性贮备电池,电池反应方程式为Mg+2AgCl=Mg2++2Ag+2Cl-。下列说法正确的是( )A、该电池的负极反应式为Mg2++2e-=Mg B、该电池的正极反应式为Ag-e-+Cl-=AgCl C、AgCl为原电池的正极,发生了氧化反应 D、海水中的Na+向AgCl极移动四、培优
-
14. 下列有关说法正确的是( )

 A、图1中气体甲为O2 B、图2电路中流过7.5mol电子时,共产生标准状况下N2的体积为16.8L C、图1中若不考虑溶液体积变化,阳极室溶液的pH减小 D、图2中微生物的硝化过程是缺氧环境下进行的15. 钠离子电池具有资源丰富、成本低、安全性好、转换效率高等特点,有望成为锂离子电池之后的新型首选电池,如图是一种钠离子电池工作示意图:
A、图1中气体甲为O2 B、图2电路中流过7.5mol电子时,共产生标准状况下N2的体积为16.8L C、图1中若不考虑溶液体积变化,阳极室溶液的pH减小 D、图2中微生物的硝化过程是缺氧环境下进行的15. 钠离子电池具有资源丰富、成本低、安全性好、转换效率高等特点,有望成为锂离子电池之后的新型首选电池,如图是一种钠离子电池工作示意图:
下列说法中错误的是( )
A、放电时,Na+通过交换膜向N极移动 B、充电时,光照可促进电子的转移 C、充电时,TiO2光电极上发生的电极反应为3I-+2e-=I D、放电时,若负极室有2mol阴离子发生反应,则电路中转移3mol电子16. 太阳能路灯蓄电池是磷酸铁锂电池,其工作原理如图。M电极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料,隔膜只允许Li+通过,电池反应式为LixC6+Li1-xFePO4 LiFePO4+6C。下列说法正确的是( ) A、放电时Li+从左边移向右边,PO 从右边移向左边 B、放电时,正极反应式为Li1-xFePO4+xLi++xe-=LiFePO4 C、充电时M极连接电源的负极,电极反应式为6C+xe-=C D、充电时电路中通过2.0 mol电子,产生28 g Li17. 一种新型镁硫电池的工作原理如图所示。下列说法正确的是( )
A、放电时Li+从左边移向右边,PO 从右边移向左边 B、放电时,正极反应式为Li1-xFePO4+xLi++xe-=LiFePO4 C、充电时M极连接电源的负极,电极反应式为6C+xe-=C D、充电时电路中通过2.0 mol电子,产生28 g Li17. 一种新型镁硫电池的工作原理如图所示。下列说法正确的是( ) A、该电池使用碱性电解质水溶液 B、充电时,电子从硫电极流出 C、使用的隔膜是阴离子交换膜 D、放电时,正极反应包括3Mg2++MgS8-6e-=4MgS218. 燃料电池对新能源的发展有划时代的意义。甲池是一种氢氧燃料电池,乙池是高分子膜电解池(苯、环己烷均为气态)。已知D中进入10 mol混合气体(其中苯物质的量分数为20%,杂质不参与反应),C中出来含苯的物质的量分数为10%的混合气体(不含H2)。
A、该电池使用碱性电解质水溶液 B、充电时,电子从硫电极流出 C、使用的隔膜是阴离子交换膜 D、放电时,正极反应包括3Mg2++MgS8-6e-=4MgS218. 燃料电池对新能源的发展有划时代的意义。甲池是一种氢氧燃料电池,乙池是高分子膜电解池(苯、环己烷均为气态)。已知D中进入10 mol混合气体(其中苯物质的量分数为20%,杂质不参与反应),C中出来含苯的物质的量分数为10%的混合气体(不含H2)。
下列说法错误的是( )
A、甲池中F极为正极 B、乙池中流经水溶液的电子为6NA C、乙池中苯发生还原反应 D、甲池中G极发生:H2-2e-=2H+19. Al-H2O2 电池是一种新型电池,已知H2O2是一种弱酸,在强碱性溶液中以HO 形式存在。现以Al-H2O2为电源(如甲池所示,电池总反应为2Al+3HO =2AlO +OH-+H2O),电解处理有机质废水(如乙池所示)。下列说法正确的是( ) A、电池工作时,甲池、乙池用导线连接的顺序为a连c,b连d B、电池工作一段时间后甲池中pH值减小 C、乙池工作时,质子将从B电极室移向A电极室 D、若B电极上转化1.5molCO2 , 则甲池中溶解4molAl
A、电池工作时,甲池、乙池用导线连接的顺序为a连c,b连d B、电池工作一段时间后甲池中pH值减小 C、乙池工作时,质子将从B电极室移向A电极室 D、若B电极上转化1.5molCO2 , 则甲池中溶解4molAl
-