【备考2024年】高考化学全国甲卷真题变式分层精准练第6题
试卷更新日期:2023-08-04 类型:二轮复习
一、原题
-
1. 用可再生能源电还原时,采用高浓度的抑制酸性电解液中的析氢反应来提高多碳产物(乙烯、乙醇等)的生成率,装置如下图所示。下列说法正确的是
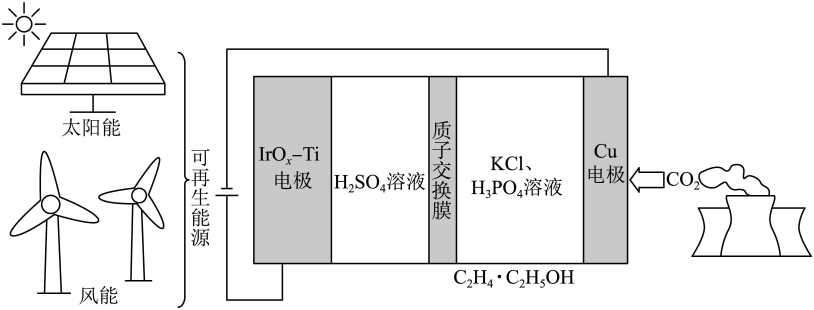 A、析氢反应发生在电极上 B、从电极迁移到电极 C、阴极发生的反应有: D、每转移电子,阳极生成气体(标准状况)
A、析氢反应发生在电极上 B、从电极迁移到电极 C、阴极发生的反应有: D、每转移电子,阳极生成气体(标准状况)二、基础
-
2. 2022年2月进行的北京冬奥会尽显化学高科技,下列有关说法错误的是( )A、“飞扬”火炬外壳是用密度小且耐高温的碳纤维与高性能树脂做成的复合材料,碳纤维是新型无机非金属材料 B、跨临界直接制冰使用的CO2是由极性键构成的非极性分子 C、本届冬奥会使用氢燃料,氢燃料电池工作时,氢气在正极发生还原反应 D、“防切割竞赛服”里面的“剪切增稠液体”是由聚乙二醇和硅微粒加工而成,其中聚乙二醇是由乙二醇经过缩聚反应制得3. 下列相关方程式书写正确的是( )A、的水解方程式: B、的电离方程式: C、明矾可作为净水剂: D、铅蓄电池放电时负极反应式:4. 下列说法不正确的是( )A、锌锰电池是一次电池 B、燃料电池是一类高效污染小的新型电池 C、化学电池的反应原理是氧化还原反应 D、铅蓄电池放电时正极是Pb5. 下列装置中,能形成原电池的是( )A、
 B、
B、 C、
C、 D、
D、 6. 磷酸铁锂电池在充放电过程中表现出了良好的循环稳定性,具有较长的使用寿命,放电时的反应为: LixC6+Li1-xFePO4= 6C+LiFePO4。图1为某磷酸铁锂电池的切面,图2为LiFePO4晶胞充放电时Li+脱出和嵌入的示意图。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。下列说法错误的是
6. 磷酸铁锂电池在充放电过程中表现出了良好的循环稳定性,具有较长的使用寿命,放电时的反应为: LixC6+Li1-xFePO4= 6C+LiFePO4。图1为某磷酸铁锂电池的切面,图2为LiFePO4晶胞充放电时Li+脱出和嵌入的示意图。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。下列说法错误的是 A、放电时,负极反应: LixC6- xe- = xLi++6C B、(a)过程中1mol晶胞转移的电子数为NA C、(b)代表放电过程, Li+脱离石墨,经电解质嵌入正极 D、充电时的阳极反应: LiFePO4- xe-= Li1-xFePO4+xLi+7. 已知:杂环共轭聚合物制成的电极材料具有体积不膨胀的特性。铝-聚合物电池以杂环共轭聚合物为正极材料、氯化铝/尿素(AlCl/urea,urea为尿素)为电解液,其有关工作原理如下图所示。
A、放电时,负极反应: LixC6- xe- = xLi++6C B、(a)过程中1mol晶胞转移的电子数为NA C、(b)代表放电过程, Li+脱离石墨,经电解质嵌入正极 D、充电时的阳极反应: LiFePO4- xe-= Li1-xFePO4+xLi+7. 已知:杂环共轭聚合物制成的电极材料具有体积不膨胀的特性。铝-聚合物电池以杂环共轭聚合物为正极材料、氯化铝/尿素(AlCl/urea,urea为尿素)为电解液,其有关工作原理如下图所示。
下列说法错误的是( )
A、放电时,负极附近AlCl减少 B、放电时,正极上生成1mol聚合物时,电路中通过4mol电子 C、充电时,阴极反应为:2AlCl2(urea)+3e-=Al+AlCl+4urea D、用杂环共轭聚合物为正极材料能克服体积膨胀对电极结构造成的破坏三、提高
-
8. 我国科学家最近开发出锌硒电池,工作原理如图所示。放电时,电池总反应为。下列说法正确的是( )
 A、放电时电能转化成化学能 B、a极的电极反应式为 C、放电时,溶液中向a极迁移 D、1mol Se完全反应时外电路中转移2mol电子9. 西北工业大学报道了一种水溶液电池,它不仅将乙炔脱除的耗能过程转换为发电过程,而且能通过独特的放电机制将乙炔还原为乙烯,反应原理为 , 其放电装置如图所示,下列说法正确的是( )
A、放电时电能转化成化学能 B、a极的电极反应式为 C、放电时,溶液中向a极迁移 D、1mol Se完全反应时外电路中转移2mol电子9. 西北工业大学报道了一种水溶液电池,它不仅将乙炔脱除的耗能过程转换为发电过程,而且能通过独特的放电机制将乙炔还原为乙烯,反应原理为 , 其放电装置如图所示,下列说法正确的是( ) A、锌电极是原电池正极,发生还原反应 B、铜枝晶电极的电极反应式为 C、电子流向为锌电极→KOH溶液→铜枝晶电极 D、生成标准状况下33.6L , 则转移的电子数为10. 某小组设计如图装置(盐桥中盛有浸泡了溶液的琼胶)研究电化学原理。下列叙述正确的是( )
A、锌电极是原电池正极,发生还原反应 B、铜枝晶电极的电极反应式为 C、电子流向为锌电极→KOH溶液→铜枝晶电极 D、生成标准状况下33.6L , 则转移的电子数为10. 某小组设计如图装置(盐桥中盛有浸泡了溶液的琼胶)研究电化学原理。下列叙述正确的是( ) A、银片为负极,电极反应为: B、用稀硫酸代替溶液,也可形成原电池 C、电子的流向是Mg→导线→Ag→溶液→盐桥→溶液 D、取出盐桥,电流表指针依然偏转11. 用下列实验装置进行相应实验,有关说法不正确的是( )
A、银片为负极,电极反应为: B、用稀硫酸代替溶液,也可形成原电池 C、电子的流向是Mg→导线→Ag→溶液→盐桥→溶液 D、取出盐桥,电流表指针依然偏转11. 用下列实验装置进行相应实验,有关说法不正确的是( ) A、装置①可用于比较金属X和的金属活动性强弱 B、装置②可用于实验室制备并收集 C、装置③可用于制备乙酸乙酯 D、装置④可用于探究乙醇的还原性12. 二氧化氯(ClO2 , 黄绿色气体,易溶于水)是一种安全稳定、高效低毒的消毒剂,疫情防控中常用于环境的消毒。工业上通过情性电极电解氯化铵和盐酸的方法制备ClO2的原理如图所示。下列说法正确的是( )
A、装置①可用于比较金属X和的金属活动性强弱 B、装置②可用于实验室制备并收集 C、装置③可用于制备乙酸乙酯 D、装置④可用于探究乙醇的还原性12. 二氧化氯(ClO2 , 黄绿色气体,易溶于水)是一种安全稳定、高效低毒的消毒剂,疫情防控中常用于环境的消毒。工业上通过情性电极电解氯化铵和盐酸的方法制备ClO2的原理如图所示。下列说法正确的是( ) A、当有0.2mol离子通过离子交换膜时,二氧化氯发生器中理论上产生13.5g ClO2 B、d为直流电源的负极,电解池a极上发生的电极反应为 C、二氧化氯发生器内,氧化剂与还原剂的物质的量之比为6∶1 D、离子交换膜为阳离子交换膜,在b极区流出的Y溶液是稀盐酸13. 新能源汽车在我国蓬勃发展,新能源汽车所用电池多采用三元锂电池,某三元锂电池放电时工作原理如图所示。下列说法错误的是( )
A、当有0.2mol离子通过离子交换膜时,二氧化氯发生器中理论上产生13.5g ClO2 B、d为直流电源的负极,电解池a极上发生的电极反应为 C、二氧化氯发生器内,氧化剂与还原剂的物质的量之比为6∶1 D、离子交换膜为阳离子交换膜,在b极区流出的Y溶液是稀盐酸13. 新能源汽车在我国蓬勃发展,新能源汽车所用电池多采用三元锂电池,某三元锂电池放电时工作原理如图所示。下列说法错误的是( ) A、充电时,M极有电子流入,发生还原反应 B、锂电池的优点是质量小,电容量大,可重复使用 C、用该电池电解精炼铜,当电池中迁移时,理论上可获得纯铜 D、充电时,N极的电极反应式为
A、充电时,M极有电子流入,发生还原反应 B、锂电池的优点是质量小,电容量大,可重复使用 C、用该电池电解精炼铜,当电池中迁移时,理论上可获得纯铜 D、充电时,N极的电极反应式为四、培优
-
14. 某新型电池以 NaBH4(B的化合价为+3价)和H2O2作原料,负极材料采用 Pt,正极材料采用MnO2(既作电极材料又对该极的电极反应共有催化作用),其工作原理如图所示。
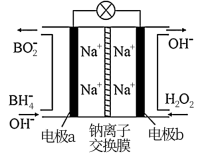
下列说法不正确的是( )A、每消耗3 mol H2O2 , 转移6 mol e- B、该电池的的总反应方程式为:NaBH4+4H2O2=NaBO2+6H2O C、a极上的电极反应式为+8OH--8e-=+6H2O D、电池工作时Na+从b极区移向a极区15. 一种清洁、低成本的三步法氯碱工艺工作原理的示意图如图。下列说法错误的是( ) A、与传统氯碱工艺相比,该方法可避免使用离子交换膜 B、第一步中阳极反应为:Na0.44MnO2-xe-=Na0.44-xMnO2+xNa+ C、第二步中,放电结束后,电解质溶液中NaCl的含量增大 D、理论上,每消耗1mol O2 , 可生产4mol NaOH和2mol Cl216. 科学家发现对冶金硅进行电解精炼提纯可降低高纯硅制备成本。相关电解槽装置如图所示,用Cu—Si合金作硅源,在950℃下利用三层液熔盐进行电解精炼,并利用某CH4燃料电池(如图所示)作为电源。下列有关说法不正确的是( )
A、与传统氯碱工艺相比,该方法可避免使用离子交换膜 B、第一步中阳极反应为:Na0.44MnO2-xe-=Na0.44-xMnO2+xNa+ C、第二步中,放电结束后,电解质溶液中NaCl的含量增大 D、理论上,每消耗1mol O2 , 可生产4mol NaOH和2mol Cl216. 科学家发现对冶金硅进行电解精炼提纯可降低高纯硅制备成本。相关电解槽装置如图所示,用Cu—Si合金作硅源,在950℃下利用三层液熔盐进行电解精炼,并利用某CH4燃料电池(如图所示)作为电源。下列有关说法不正确的是( ) A、左侧电解槽中:Si优先于Cu被氧化 B、电极c与b相连,d与a相连 C、a极的电极反应为CH4-8e-+4O2-=CO2+2H2O D、相同时间下,通入CH4、O2的体积不同,会影响硅的提纯速率17. 我国某科研团队设计了一种新型能量存储/转化装置(如图所示)。闭合K2、断开K1时,制氢并储能;断开K2、闭合K1时,供电。下列说法正确的是( )
A、左侧电解槽中:Si优先于Cu被氧化 B、电极c与b相连,d与a相连 C、a极的电极反应为CH4-8e-+4O2-=CO2+2H2O D、相同时间下,通入CH4、O2的体积不同,会影响硅的提纯速率17. 我国某科研团队设计了一种新型能量存储/转化装置(如图所示)。闭合K2、断开K1时,制氢并储能;断开K2、闭合K1时,供电。下列说法正确的是( ) A、制氢时,溶液中向X电极移动 B、供电时,Zn电极反应式为 C、供电时,X电极发生氧化反应 D、制氢时,X电极反应式为18. 耦合电化学合成法从 合成碳酸二甲酯( )的反应原理如图1所示,反应②的机理如图2所示。下列说法正确的是( )
A、制氢时,溶液中向X电极移动 B、供电时,Zn电极反应式为 C、供电时,X电极发生氧化反应 D、制氢时,X电极反应式为18. 耦合电化学合成法从 合成碳酸二甲酯( )的反应原理如图1所示,反应②的机理如图2所示。下列说法正确的是( ) A、该电化学合成法从 合成碳酸二甲酯的总反应是非氧化还原反应 B、图2含 物质中 的价态保持不变 C、 是反应②的催化剂 D、工作过程中反应①、②和③逐级转移电子,电子的能量保持不变19. 城市污水循环用作城市稳定的第二水源,对缓解城市水危机有重要意义。高铁酸盐[Fe(VI)]作为一种绿色环保水处理剂,兼具极强的氧化性和良好的絮凝效果,图为电解制备高铁酸盐的装置示意图(电解液为NaOH溶液),下列说法正确的是( )
A、该电化学合成法从 合成碳酸二甲酯的总反应是非氧化还原反应 B、图2含 物质中 的价态保持不变 C、 是反应②的催化剂 D、工作过程中反应①、②和③逐级转移电子,电子的能量保持不变19. 城市污水循环用作城市稳定的第二水源,对缓解城市水危机有重要意义。高铁酸盐[Fe(VI)]作为一种绿色环保水处理剂,兼具极强的氧化性和良好的絮凝效果,图为电解制备高铁酸盐的装置示意图(电解液为NaOH溶液),下列说法正确的是( ) A、石墨作阳极,铁作阴极 B、阳极的电极方程式为: C、生成1mol高铁酸盐,II室溶液质量理论上增大56g D、工作时,I室和II室溶液的pH均增大
A、石墨作阳极,铁作阴极 B、阳极的电极方程式为: C、生成1mol高铁酸盐,II室溶液质量理论上增大56g D、工作时,I室和II室溶液的pH均增大
-