广东省广州市2022-2023学年高一下学期期末考试化学试题
试卷更新日期:2023-08-04 类型:期末考试
一、选择题:本题共20小题,共52分,第1~14小题,每小题2分;第15~20小题,每小题4分。每小题只有一个选项符合题意。
-
1. 材料在生活和生产的各领域中都有极为广泛的应用。下列物体的主要材质属于有机高分子材料的是( )A、光导纤维
 B、炫纹贯耳瓷壶
B、炫纹贯耳瓷壶 C、透雕重环玉佩
C、透雕重环玉佩 D、PVC(聚氯乙烯)水管
D、PVC(聚氯乙烯)水管 2. “端午节”是我国传统节日,节日习俗有吃粽子、赛龙舟及喝雄黄酒等。制作粽子的主要原料有糯米、粽叶,还有蛋黄、猪肉等馅料。下列有关说法正确的是( )A、糯米也是酿酒原料,酿酒加入的“酒曲(含酶)”起催化作用 B、赛龙舟时,挥舞的龙旗是用涤纶制作,涤纶属于天然纤维 C、蛋黄、猪肉富含油脂和蛋白质,油脂和蛋白质均属于高分子化合物 D、糯米的主要成分是淀粉,粽叶的主要成分是纤维素,淀粉和纤维素的分子式都是 , 互为同分异构体3. 下列叙述正确的是( )A、酒越陈越香与酯化反应有关 B、乙烷、丙烷和丁烷都没有同分异构体 C、乙烯和聚乙烯都能使溴的四氯化碳溶液褪色 D、在光照下甲烷与足量氯气反应只生成难溶于水的四氯化碳4. 氮及其化合物的转化具有重要应用。下列说法错误的是( )A、工业上通过催化氧化等系列反应生产 B、自然固氮、人工固氮都是将转化为 C、多种形态的氮及其化合物间的转化形成了自然界的“氮循环” D、侯氏制碱法以为原料制备和5. 下列化学用语错误的是( )A、乙醇的分子式: B、正丁烷的球棍模型:
2. “端午节”是我国传统节日,节日习俗有吃粽子、赛龙舟及喝雄黄酒等。制作粽子的主要原料有糯米、粽叶,还有蛋黄、猪肉等馅料。下列有关说法正确的是( )A、糯米也是酿酒原料,酿酒加入的“酒曲(含酶)”起催化作用 B、赛龙舟时,挥舞的龙旗是用涤纶制作,涤纶属于天然纤维 C、蛋黄、猪肉富含油脂和蛋白质,油脂和蛋白质均属于高分子化合物 D、糯米的主要成分是淀粉,粽叶的主要成分是纤维素,淀粉和纤维素的分子式都是 , 互为同分异构体3. 下列叙述正确的是( )A、酒越陈越香与酯化反应有关 B、乙烷、丙烷和丁烷都没有同分异构体 C、乙烯和聚乙烯都能使溴的四氯化碳溶液褪色 D、在光照下甲烷与足量氯气反应只生成难溶于水的四氯化碳4. 氮及其化合物的转化具有重要应用。下列说法错误的是( )A、工业上通过催化氧化等系列反应生产 B、自然固氮、人工固氮都是将转化为 C、多种形态的氮及其化合物间的转化形成了自然界的“氮循环” D、侯氏制碱法以为原料制备和5. 下列化学用语错误的是( )A、乙醇的分子式: B、正丁烷的球棍模型: C、乙烯的结构简式:
D、甲烷的空间填充模型:
C、乙烯的结构简式:
D、甲烷的空间填充模型: 6. 原电池原理的发现和各种电池装置的发明,改变了人们的生活方式。下列关于图1所示装置的叙述,错误的是( )
6. 原电池原理的发现和各种电池装置的发明,改变了人们的生活方式。下列关于图1所示装置的叙述,错误的是( ) A、能将化学能转化为电能 B、锌片逐渐溶解 C、铜片做正极,正极上发生还原反应 D、溶液中的移向锌片7. “劳动创造幸福”。下列劳动项目所涉及的化学知识错误的是( )
A、能将化学能转化为电能 B、锌片逐渐溶解 C、铜片做正极,正极上发生还原反应 D、溶液中的移向锌片7. “劳动创造幸福”。下列劳动项目所涉及的化学知识错误的是( )选项
劳动项目
化学知识
A
酿酒师在葡萄酒中添加适量的二氧化硫
可以杀菌和抗氧化
B
面点师制作糕点时添加小苏打作膨松剂
碳酸钠可受热分解成
C
厨师用天然气做燃料烧饭做菜
天然气的主要成分具有可燃性
D
果农在未成熟水果的包装袋中充入乙烯
乙烯可用于催熟果实
A、A B、B C、C D、D8. 下列陈述Ⅰ和Ⅱ均正确但不具有因果关系的是( )选项
陈述Ⅰ
陈述Ⅱ
A
用焦炭和石英砂制取粗硅
石英砂硬度高
B
干冰可用在舞台上制造“云雾”
干冰升华吸热,空气中的水蒸气迅速冷凝
C
用石英器皿盛放氢氟酸
二氧化硅不与强酸反应
D
用铁或铝槽车运输浓硫酸
冷浓硫酸与铁和铝不反应
A、A B、B C、C D、D9. 有4种碳骨架如图所示的烃,下列说法正确的是( )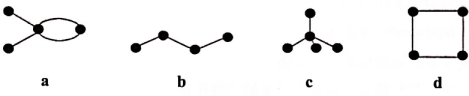 A、a和b、d互为同分异构体 B、a和b都能发生加成反应 C、b和c互为同系物 D、只有b和c能发生取代反应10. 喷泉实验装置如图所示,下列喷泉颜色与实验事实不相符的是( )
A、a和b、d互为同分异构体 B、a和b都能发生加成反应 C、b和c互为同系物 D、只有b和c能发生取代反应10. 喷泉实验装置如图所示,下列喷泉颜色与实验事实不相符的是( )
选项
气体
溶液
喷泉颜色
A
溶液
白色
B
(含酚酞)
红色
C
溶液
无色
D
(含紫色石蕊)
蓝色
A、A B、B C、C D、D11. 关于化学反应中物质或能量的变化,下列说法正确的是( )A、加热条件下进行的化学反应一定是吸热反应 B、化学键的断裂和形成是化学反应中能量变化的主要原因 C、一定条件下进行的化学反应,只能将化学能转化为热能和光能 D、将固体与固体混合并搅拌,反应放出热量12. 设为阿伏加德罗常数的值。下列说法正确的是( )A、溶液中含有的数目为 B、标准状况下,乙醇所含的分子数为 C、一定条件下,与足量的充分反应,转移的电子数为 D、固体中含有的离子数为13. 实验室用氯化铵和氢氧化钙反应制取氨气,按照制备、收集、性质检验及尾气处理的顺序进行实验,下列装置(“→”表示气流方向)不能达到实验目的的是A、 B、
B、 C、
C、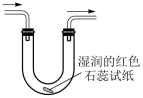 D、
D、 14. 关于有机物的说法错误的是( )A、分子式为 B、一定条件下,该物质可与氢气发生加成反应 C、该物质属于酯类 D、该物质与足量金属钠反应可生成15. 用如图所示装置制备乙酸乙酯。下列说法错误的是( )
14. 关于有机物的说法错误的是( )A、分子式为 B、一定条件下,该物质可与氢气发生加成反应 C、该物质属于酯类 D、该物质与足量金属钠反应可生成15. 用如图所示装置制备乙酸乙酯。下列说法错误的是( ) A、右侧试管内液体的上层有无色透明的油状液体产生 B、右侧导管不伸入液面下,可防止倒吸 C、加入过量乙醇,可使乙酸完全转化为乙酸乙酯 D、饱和碳酸钠溶液的作用有除去乙酸、吸收乙醇等16. 除去下列物质中的杂质(括号内的物质),所使用的试剂和操作都正确的是( )
A、右侧试管内液体的上层有无色透明的油状液体产生 B、右侧导管不伸入液面下,可防止倒吸 C、加入过量乙醇,可使乙酸完全转化为乙酸乙酯 D、饱和碳酸钠溶液的作用有除去乙酸、吸收乙醇等16. 除去下列物质中的杂质(括号内的物质),所使用的试剂和操作都正确的是( )选项
物质(杂质)
使用的试剂
操作
A
甲烷(乙烯)
酸性高锰酸钾溶液
洗气
B
水
洗气
C
溶液
过量铁粉
过滤
D
乙醇(水)
蒸馏
A、A B、B C、C D、D17. 部分含氮物质的分类与相应化合价关系如图所示。下列推断错误的是( ) A、c溶于水可得d和b B、a既可被氧化,也可被还原 C、将铜丝插入d的浓溶液可产生b D、自然界存在a→b→c→d→e的转化18. 下列离子方程式书写正确的是( )A、通入水中制氯水: B、铜片与稀硝酸反应: C、与水反应: D、溶液与溶液混合:19. 2022年我国科学家首次在月球上发现一种磷酸盐矿物,该物质含有五种主族元素,原子序数依次增大且均不大于20。为非金属元素,为金属元素,的最高正化合价为 , Z和同族。下列说法正确的是( )A、原子半径: B、和可形成含有非极性键的离子化合物 C、的最高价氧化物对应的水化物均为强碱 D、的简单气态氢化物比氨气稳定20. 实验室进行粗盐提纯时,需除去和 , 所用试剂包括以及( )A、 B、 C、 D、
A、c溶于水可得d和b B、a既可被氧化,也可被还原 C、将铜丝插入d的浓溶液可产生b D、自然界存在a→b→c→d→e的转化18. 下列离子方程式书写正确的是( )A、通入水中制氯水: B、铜片与稀硝酸反应: C、与水反应: D、溶液与溶液混合:19. 2022年我国科学家首次在月球上发现一种磷酸盐矿物,该物质含有五种主族元素,原子序数依次增大且均不大于20。为非金属元素,为金属元素,的最高正化合价为 , Z和同族。下列说法正确的是( )A、原子半径: B、和可形成含有非极性键的离子化合物 C、的最高价氧化物对应的水化物均为强碱 D、的简单气态氢化物比氨气稳定20. 实验室进行粗盐提纯时,需除去和 , 所用试剂包括以及( )A、 B、 C、 D、二、非选择题:本题共4小题,共48分。
-
21. 某学习小组在实验室制备并探究其性质,将铜丝插入热浓硫酸中进行如图所示的探究活动(a~d均为浸有相应试液的棉花)。
 (1)、该实验装置的优点是(至少写两点)。(2)、具支试管中发生反应的化学方程式为。(3)、a处的实验现象是 , 说明的水溶液具有性。(4)、说明具有还原性的实验现象是。(5)、d处发生反应的离子方程式为。(6)、关于b处品红褪色的原因,一般认为是由于与品红生成了不稳定的无色物质。请设计实验证明:。22. 丙烯酸乙酯是一种食品用合成香料,可以用乙烯、丙烯等石油化工产品为原料进行合成:
(1)、该实验装置的优点是(至少写两点)。(2)、具支试管中发生反应的化学方程式为。(3)、a处的实验现象是 , 说明的水溶液具有性。(4)、说明具有还原性的实验现象是。(5)、d处发生反应的离子方程式为。(6)、关于b处品红褪色的原因,一般认为是由于与品红生成了不稳定的无色物质。请设计实验证明:。22. 丙烯酸乙酯是一种食品用合成香料,可以用乙烯、丙烯等石油化工产品为原料进行合成: (1)、乙烯和丙烯互为(填“同分异构体”或“同系物”)。(2)、A的结构简式是。(3)、B中含有的官能团有(写名称)。(4)、下列试剂可用于鉴别A和B的是(填字母)。
(1)、乙烯和丙烯互为(填“同分异构体”或“同系物”)。(2)、A的结构简式是。(3)、B中含有的官能团有(写名称)。(4)、下列试剂可用于鉴别A和B的是(填字母)。a.氯化钠溶液 b.溴的四氯化碳溶液 c.碳酸钠溶液
(5)、A与B合成丙烯酸乙酯的化学方程式为 , 该反应的类型是。(6)、久置的丙烯酸乙酯自身会发生聚合反应,该反应的化学方程式为。23. 硫酸是重要的化工原料,工业制硫酸的其中一步重要反应是 , 正反应放热。一定条件下,恒容密闭容器中发生该反应,各物质浓度随时间变化的曲线如下图所示。 (1)、反应开始至20分钟,的平均反应速率为。(2)、图中点,正反应速率逆反应速率(填“>”“<”或“=”)。(3)、反应进行到第分钟时恰好达到平衡,结合图像分析,能说明转化成的反应在该条件下达到限度的证据是。(4)、下列说法错误的是____。A、上述条件下,不可能地转化为 B、升高温度,可以实现的完全转化 C、通过调控反应条件,可以提高该反应进行的程度 D、使用催化剂可以增大反应速率,提高生产效率(5)、硫酸厂产生的尾气中含有少量。双碱法脱硫的原理示意图如下:
(1)、反应开始至20分钟,的平均反应速率为。(2)、图中点,正反应速率逆反应速率(填“>”“<”或“=”)。(3)、反应进行到第分钟时恰好达到平衡,结合图像分析,能说明转化成的反应在该条件下达到限度的证据是。(4)、下列说法错误的是____。A、上述条件下,不可能地转化为 B、升高温度,可以实现的完全转化 C、通过调控反应条件,可以提高该反应进行的程度 D、使用催化剂可以增大反应速率,提高生产效率(5)、硫酸厂产生的尾气中含有少量。双碱法脱硫的原理示意图如下:
①可以循环使用的物质是(写化学式)。
②理论上,过程Ⅲ中消耗氧气时,过程Ⅰ中吸收的物质的量是。
24. 浩瀚的海洋里蕴藏着丰富的资源,可以从海水中获得镁和溴等物质。从海水中提取镁和溴的步骤如下: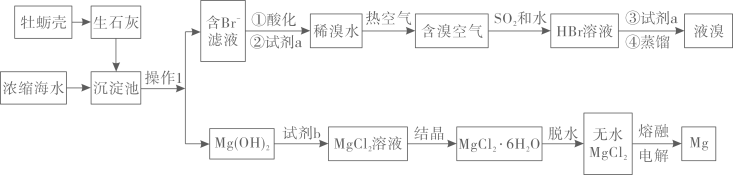
已知:相关物质熔点
物质
熔点/
2852
714
(1)、以牡蛎壳为原料的优点是。(2)、“操作1”名称是。(3)、加入试剂a发生反应的离子方程式为。(4)、下列说法正确的是____(填字母)。A、利用蒸馏法实现海水淡化,发生了化学变化 B、“酸化”的目的之一是与滤液中的碱反应 C、能用热空气吹出 , 是利用了的挥发性(5)、上述海水提溴的过程经过2次“”转化,目的是。(6)、试剂b可以选用(填名称)。(7)、工业上电解冶炼金属镁,以为原料而不用的原因是。