【备考2024年】高考化学全国甲卷真题变式分层精准练第3题
试卷更新日期:2023-08-04 类型:二轮复习
一、原题
-
1. 实验室将粗盐提纯并配制的溶液。下列仪器中,本实验必须用到的有
①天平②温度计③坩埚④分液漏斗⑤容量瓶⑥烧杯⑦滴定管⑧酒精灯
A、①②④⑥ B、①④⑤⑥ C、②③⑦⑧ D、①⑤⑥⑧二、基础
-
2. 实验室用NaCl晶体配制0.2mol/L NaCl溶液,一定不涉及的仪器的是( )A、
 B、
B、 C、
C、 D、
D、 3. 实验室欲用固体配制250mL溶液,下列仪器不需要的是A、
3. 实验室欲用固体配制250mL溶液,下列仪器不需要的是A、 B、
B、 C、
C、 D、
D、 4. 实验室用98%的浓硫酸配制的稀硫酸。下列说法错误的是A、应选用200mL容量瓶 B、可选用量筒量取浓硫酸 C、在烧杯中稀释浓硫酸 D、定容时应选用胶头滴管5. 室温下,甲同学配制5%的溶液100g,乙同学配制的溶液100mL(的溶解度为水),下列说法正确的是A、所需溶质的质量相同 B、所需仪器均包括100mL容量瓶 C、所配溶液均为不饱和溶液 D、所配溶液质量相同6. 配制一定体积的2.00mol/L溶液,不需要使用的仪器是A、
4. 实验室用98%的浓硫酸配制的稀硫酸。下列说法错误的是A、应选用200mL容量瓶 B、可选用量筒量取浓硫酸 C、在烧杯中稀释浓硫酸 D、定容时应选用胶头滴管5. 室温下,甲同学配制5%的溶液100g,乙同学配制的溶液100mL(的溶解度为水),下列说法正确的是A、所需溶质的质量相同 B、所需仪器均包括100mL容量瓶 C、所配溶液均为不饱和溶液 D、所配溶液质量相同6. 配制一定体积的2.00mol/L溶液,不需要使用的仪器是A、 B、
B、 C、
C、 D、
D、 7. 将30mL0.5mol/ L NaOH溶液加水稀释到 0.03 mol/L ,则选用的容量瓶规格为A、100 mL B、250 mL C、500 mL D、1000 mL8. 实验室配制碳酸钠标准溶液并用其标定盐酸浓度,下列步骤中所选仪器正确的是( )
7. 将30mL0.5mol/ L NaOH溶液加水稀释到 0.03 mol/L ,则选用的容量瓶规格为A、100 mL B、250 mL C、500 mL D、1000 mL8. 实验室配制碳酸钠标准溶液并用其标定盐酸浓度,下列步骤中所选仪器正确的是( )



A.量取25.00mL碳酸钠标准溶液置于锥形瓶中
B.用带塑料塞的容量瓶配制碳酸钠标准液
C.用称量纸称量碳酸钠固体
用盛有盐酸的滴定管进行滴定
A、A B、B C、C D、D三、提高
-
9. 下列实验操作中:①过滤;②取固体试剂;③蒸发;④取液体试剂;⑤溶解;⑥配制一定物质的量浓度的溶液。一定要用到玻璃棒的是( )A、①③④⑥ B、①②③④ C、①③⑤⑥ D、②③④⑤10. 下列有关实验说法,不正确的是A、碱液不慎溅到手上,先用大量水冲洗,再用饱和硼酸溶液洗,最后用水冲洗 B、中学实验室中可以将未用完的钠放回原试剂瓶 C、向Na2CO3粉末中滴加几滴蒸馏水,Na2CO3结块变成晶体,并伴随着吸热现象 D、用容量瓶配制溶液,定容时若加水超过刻度线,应重新配制11. 下列关于容量瓶使用方法的叙述中,正确的是( )
①使用容量瓶前检查是否漏水;
②在容量瓶中溶解固体溶质;
③溶液需冷却至室温方可注入容量瓶;
④尽可能将溶质全部转移到容量瓶中;
⑤加水定容时,不小心超过刻度线,用胶头滴管吸出多余液体
A、①②③ B、①③④ C、③④⑤ D、①④⑤12. 下列实验装置及操作完全正确的是A、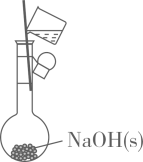 配制H溶液
B、
配制H溶液
B、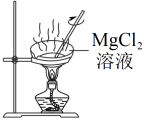 制备无水氯化镁
C、
制备无水氯化镁
C、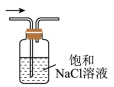 除去中的
D、
除去中的
D、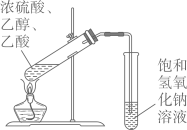 制备乙酸乙酯
13. 配制480 mL0.1 mol/LCuSO4溶液时,下列有关说法正确的是( )A、称量的胆矾晶体质量为12.0 g B、容量瓶中原有少量蒸馏水,会使所配溶液浓度偏低 C、称量的胆矾晶体部分失去结晶水,会使所配溶液浓度偏高 D、配制过程中需要使用的玻璃仪器只有烧杯、玻璃棒、500 mL容量瓶14. 下列操作可能使所配Na2CO3溶液浓度偏大的是( )A、烧杯和玻璃棒未洗涤 B、称量前Na2CO3·10H2O固体已失去部分结晶水 C、加水时超过刻度线,用胶头滴管吸出多余的液体 D、上下颠倒摇匀后溶液液面低于刻度线,补充加水至刻度线15. 下列实验装置能达到相应实验目的的是
制备乙酸乙酯
13. 配制480 mL0.1 mol/LCuSO4溶液时,下列有关说法正确的是( )A、称量的胆矾晶体质量为12.0 g B、容量瓶中原有少量蒸馏水,会使所配溶液浓度偏低 C、称量的胆矾晶体部分失去结晶水,会使所配溶液浓度偏高 D、配制过程中需要使用的玻璃仪器只有烧杯、玻璃棒、500 mL容量瓶14. 下列操作可能使所配Na2CO3溶液浓度偏大的是( )A、烧杯和玻璃棒未洗涤 B、称量前Na2CO3·10H2O固体已失去部分结晶水 C、加水时超过刻度线,用胶头滴管吸出多余的液体 D、上下颠倒摇匀后溶液液面低于刻度线,补充加水至刻度线15. 下列实验装置能达到相应实验目的的是实验装置
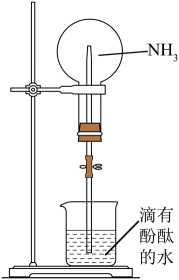

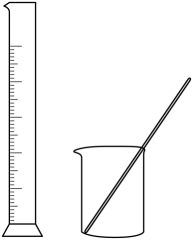

实验目的
演示喷泉实验
证明能与水反应
配制100mLNaOH溶液
分离苯和苯酚的混合物
选项
A
B
C
D
A、A B、B C、C D、D四、培优
-
16. 下列实验过程能达到实验目的的是( )
实验目的
实验过程
A
配制0.4mol•L-1的NaOH溶液
称取4.0g固体NaOH于烧杯中溶解,立即转移至250mL容量瓶中定容
B
证明酸性:H2SO3>H2CO3
室温下,用pH计测定SO2饱和溶液和CO2 饱和溶液的pH,比较pH大小
C
探究维生素C的还原性
向黄色FeCl3溶液中滴加足量无色维生素C浓溶液,观察颜色变化
D
制备NaHCO3固体
向饱和NaCl溶液中先通入CO2至饱和,再通入足量NH3 , 过滤并洗涤
A、A B、B C、C D、D17. 下列有关实验原理或操作正确的是( )A、用20 mL量筒量取15 mL酒精,加水5 mL,配制质量分数为75%酒精溶液 B、在200 mL某硫酸盐溶液中,含有1.5NA个硫酸根离子,同时含有NA个金属离子,则该硫酸盐的物质的量浓度为2.5 mol·L-1 C、实验中需用2.0 mol·L-1的Na2CO3溶液950 mL,配制时应选用的容量瓶的规格和称取Na2CO3的质量分别为950 mL、201.4 g D、实验室配制500 mL 0.2 mol·L-1的硫酸亚铁溶液,其操作是:用天平称15.2 g绿矾(FeSO4·7H2O),放入小烧杯中加水溶解,转移到500 mL容量瓶,洗涤、稀释、定容、摇匀18. 下列有关实验说法,错误的是( )A、碱液不慎溅到手上,先用大量水冲洗,再用饱和硼酸溶液洗,最后用水冲洗 B、 和 的混合物经溶解、过滤,洗涤、干燥,可分离出 C、用容量瓶配制溶液,定容时若加水超过刻度线,立即用滴管吸出多余液体 D、火柴头的浸泡液中滴加 溶液,稀 和 溶液,可检验火柴头是否含有氯元素19. 下列实验操作可以达到实验目的的是( )选项
实验目的
实验操作
A
探究浓度对反应速率的影响
向2支各盛有4mL0.01mol·L-1KMnO4酸性溶液的试管中,分别加入2mL0.1mol·L-1H2C2O4溶液和2mL0.2mol·L-1H2C2O4溶液,记录溶液褪色所需的时间
B
配制1.00mol·L-1的NaOH溶液
称取4.0g固体NaOH于烧杯中,加入少量蒸馏水溶解,然后转移至100mL容量瓶中定容
C
探究固体表面积对反应速率的影响
称取相同质量的大理石和纯碱,加入到盛有浓度、体积均相同的盐酸的小烧杯中,观察实验现象
D
探究淀粉溶液在稀硫酸和加热条件下是否水解
取少量的水解液于试管中,先加适量的NaOH溶液,再滴入碘水,观察实验现象
A、A B、B C、C D、D
-