广东省深圳市两校2022-2023学年高二下学期7月期末考试化学试题
试卷更新日期:2023-08-04 类型:期末考试
一、选择题:本题共16个小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在每小题给出的四个选项中,只有一项是符合题目要求的。
-
1. 2022年11月20日晚卡塔尔世界杯正式开幕。在此次史上最“壕”的世界杯中,中国元素随处可见。下列有关说法错误的是( )A、世界杯吉祥物“拉伊卜”毛绒玩具主要来自中国义乌,所用的材料是以羊毛为原料的绒线,其主要成分为蛋白质 B、中国铁建打造的主场馆——卢塞尔体育场内幕墙设置的完全封闭的隔热玻璃属于混合物 C、中国宇通新能源客车的引入有助于实现卡塔尔“碳中和”的世界杯目标 D、中国电建承建的阿尔卡萨光伏电站使用的电池材料主要为二氧化硅2. 下列有关化学用语表示正确的是( )A、HF分子中键的电子云轮廓图:
 B、的VSEPR模型:
B、的VSEPR模型: C、KCl的形成过程:
D、次氯酸的结构式:
3. 下列劳动项目与所述的化学知识不相符的是( )
C、KCl的形成过程:
D、次氯酸的结构式:
3. 下列劳动项目与所述的化学知识不相符的是( )选项
劳动项目
化学知识
A
传统工艺:手工制作陶瓷
是陶瓷主要成分
B
学农活动:使用复合肥料培育植物
复合肥含N、P、K三种元素中的两种或三种
C
自主探究:海带提碘
通过灼烧将有机碘转化为碘离子
D
家务劳动:烹煮鱼时加入少量料酒和食醋可以去腥提鲜
食醋与料酒发生酯化反应,增加香味
A、A B、B C、C D、D4. 某有机物结构如图。下列关于该有机物的说法正确的是( ) A、分子式为 B、该有机物属于酯类 C、分子中含有4种官能团 D、能发生加成、取代反应5. 设NA为阿伏加德罗常数的值,下列说法正确的是( )A、25℃,的溶液中含有的数目为 B、中含键的数目为 C、在反应中,若有213g氯气生成,则反应中转移电子的数目为 D、固体中含有阴阳离子的总数目为6. 菠菜中富含铁元素,实验室可以检验菠菜中的铁元素,实验过程中涉及下列操作及相关叙述错误的是( )
A、分子式为 B、该有机物属于酯类 C、分子中含有4种官能团 D、能发生加成、取代反应5. 设NA为阿伏加德罗常数的值,下列说法正确的是( )A、25℃,的溶液中含有的数目为 B、中含键的数目为 C、在反应中,若有213g氯气生成,则反应中转移电子的数目为 D、固体中含有阴阳离子的总数目为6. 菠菜中富含铁元素,实验室可以检验菠菜中的铁元素,实验过程中涉及下列操作及相关叙述错误的是( )A
B
C
D




将菠菜叶剪碎后灼烧
在通风橱中,用稀硝酸浸取菠菜灰
过滤
往滤液中滴加溶液检验
A、A B、B C、C D、D7. 物质的类别和核心元素的化合价是研究物质化学性质的两个重要角度。某短周期元素的单质及其部分化合物的价类二维图如图所示。下列推断合理的是( ) A、到b、c、d、e、f均可直接转化 B、标准状况下,1molb和c的混合物体积为22.4L C、可先加盐酸,再加氯化钡溶液检验e的钠盐是否变质 D、f的水溶液在空气中放置,不易被氧化8. 下列指定反应的离子方程式错误的是( )A、明矾溶液中加入少量的: B、向氯化铁中加入少量的: C、四氯化钛的浓溶液制备水合二氧化钛: D、次氯酸钠溶液中通入少量:(已知酸性)9. 下列类比或推理合理的是( )
A、到b、c、d、e、f均可直接转化 B、标准状况下,1molb和c的混合物体积为22.4L C、可先加盐酸,再加氯化钡溶液检验e的钠盐是否变质 D、f的水溶液在空气中放置,不易被氧化8. 下列指定反应的离子方程式错误的是( )A、明矾溶液中加入少量的: B、向氯化铁中加入少量的: C、四氯化钛的浓溶液制备水合二氧化钛: D、次氯酸钠溶液中通入少量:(已知酸性)9. 下列类比或推理合理的是( )已知
方法
结论
A
沸点:
类比
沸点:
B
酸性:
类比
酸性:
C
金属性:
推理
氧化性:
D
:
推理
溶解度:
A、A B、B C、C D、D10. 广东名酒“玉冰烧”始载于宋代赵珣的《熙宁酒课》,其独特的风味在于从醪液中得到浓度更高的初酒后,浸入猪膘肉“陈肉酝浸”而成。因粤语中“玉”与“肉”同音,故取名为玉冰烧,下图为“玉冰烧”的简要造流程,其中说法错误的是( )
 A、糖化过程中,淀粉是分步水解为单糖的 B、酒化过程的反应原理为: C、操作1为过滤 D、猪膘肉中溶出的酯类化合物可使酒的香气、口感更丰富11. 普鲁士蓝是一种辐射应急药物。最初,狄斯巴赫把草木灰和牛血混在一起,制成亚铁氰化钾(其三水合物俗称黄血盐),之后与反应获得了普鲁士蓝。如图是普鲁士蓝晶体的单元结构,下列说法正确的是( )
A、糖化过程中,淀粉是分步水解为单糖的 B、酒化过程的反应原理为: C、操作1为过滤 D、猪膘肉中溶出的酯类化合物可使酒的香气、口感更丰富11. 普鲁士蓝是一种辐射应急药物。最初,狄斯巴赫把草木灰和牛血混在一起,制成亚铁氰化钾(其三水合物俗称黄血盐),之后与反应获得了普鲁士蓝。如图是普鲁士蓝晶体的单元结构,下列说法正确的是( ) A、黄血盐的化学式为 B、在制备黄血盐时,牛血的作用是仅提供Fe元素 C、普鲁士蓝中与的配位数均为6 D、普鲁士蓝可用于金属铊中毒治疗,铊元素是有放射性的过渡元素12. 已知反应 , 在一定温度下,反应达到平衡时,B的体积分数(B%)与压强变化的关系如图所示,下列叙述一定正确的是( )
A、黄血盐的化学式为 B、在制备黄血盐时,牛血的作用是仅提供Fe元素 C、普鲁士蓝中与的配位数均为6 D、普鲁士蓝可用于金属铊中毒治疗,铊元素是有放射性的过渡元素12. 已知反应 , 在一定温度下,反应达到平衡时,B的体积分数(B%)与压强变化的关系如图所示,下列叙述一定正确的是( )
①
②x点表示的正反应速率大于逆反应速率
③x点表示的反应速率比y点的大
④
A、①② B、②④ C、②③ D、①③13. 浓差电池是一种利用电解质溶液浓度差产生电势差而形成的电池。理论上当电解质溶液的浓度相等时停止放电。图1为浓差电池,图2为电渗析法制备磷酸二氢钠,用浓差电池为电源完成电渗析法制备磷酸二氢钠。下列说法错误的是( )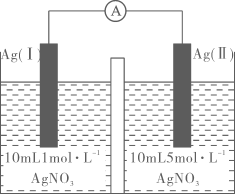

图1 图2
A、电极a应与Ag(Ⅱ)相连 B、电渗析装置中膜b为阳离子交换膜 C、电渗析过程中左、右室中和NaOH的浓度均增大 D、电池从开始到停止放电,理论上可制备14. 一定条件下,与HCl发生加成反应有①、②两种可能,反应进程中能量变化如图所示。下列说法中不正确的是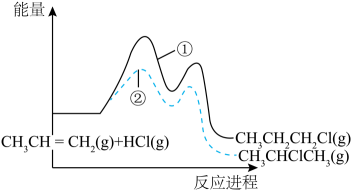 A、反应①、②焓变不同,与产物稳定性有关,与反应的中间状态无关 B、反应①、②均经过两步反应完成,对应的分步反应过程中均放出能量 C、其他条件不变,适当提高反应温度,可以提高产物中的比例 D、相同条件下,的生成速率大于15. 乙醇和乙酸在酸性条件下生成乙酸乙酯,反应机理如图,下列说法错误的是( )
A、反应①、②焓变不同,与产物稳定性有关,与反应的中间状态无关 B、反应①、②均经过两步反应完成,对应的分步反应过程中均放出能量 C、其他条件不变,适当提高反应温度,可以提高产物中的比例 D、相同条件下,的生成速率大于15. 乙醇和乙酸在酸性条件下生成乙酸乙酯,反应机理如图,下列说法错误的是( ) A、Ⅰ→Ⅱ形成配位键,Ⅴ→Ⅵ断裂配位键 B、Ⅱ→Ⅲ的反应的原子利用率为100% C、Ⅲ→Ⅳ质子发生转移 D、加入催化剂浓硫酸,能加快反应速率,不能提高平衡产率16. 常温下,向溶液中逐滴加入等浓度NaOH溶液,所得溶液中含A元素的微粒的物质的量分数与溶液pH的关系如图,下列说法正确的是( )
A、Ⅰ→Ⅱ形成配位键,Ⅴ→Ⅵ断裂配位键 B、Ⅱ→Ⅲ的反应的原子利用率为100% C、Ⅲ→Ⅳ质子发生转移 D、加入催化剂浓硫酸,能加快反应速率,不能提高平衡产率16. 常温下,向溶液中逐滴加入等浓度NaOH溶液,所得溶液中含A元素的微粒的物质的量分数与溶液pH的关系如图,下列说法正确的是( ) A、的水解离子方程式为 , B、室温下,水解常数 C、溶液中存在 D、常温下,等物质的量浓度的NaHA与溶液等体积混合后溶液的
A、的水解离子方程式为 , B、室温下,水解常数 C、溶液中存在 D、常温下,等物质的量浓度的NaHA与溶液等体积混合后溶液的二、非选择题:本题共4小题,共56分。
-
17. 84消毒液的有效成分为NaClO,广泛应用于物体表面和环境等的消毒。实验室利用以下装置制备NaClO并进行性质探究。
 (1)、装置B的作用是。(2)、生成NaClO的离子反应方程式为。(3)、某小组研究25℃下NaClO稳定性的影响因素。
(1)、装置B的作用是。(2)、生成NaClO的离子反应方程式为。(3)、某小组研究25℃下NaClO稳定性的影响因素。提出假设:NaClO溶液中加入或改变NaCl浓度,对NaClO的稳定性有影响。
设计方案并完成实验:用浓度为的NaClO溶液、NaCl溶液,溶液和NaOH溶液按下表配制总体积相同的系列溶液:相同时间内测定溶液中有效氯(指次氯酸钠中氯元素质量占样品的百分含量),记录数据。
序号
V(NaClO)/mL
V(NaCl)/mL
V(NaOH)/mL
有效氯/%
Ⅰ
40.00
/
/
/
10.00
3.6
Ⅱ
40.00
/
4.00
a
4.18
Ⅲ
40.00
/
2.00
8.00
4.12
Ⅳ
40.00
/
1.00
9.00
4.24
Ⅴ
40.00
b
8.00
4.28
Ⅵ
40.00
6.00
4.00
4.38
①根据表中信息,补充数据:;。
②由实验Ⅱ和Ⅲ可知,增加NaCl的浓度,NaClO溶液的稳定性(填“增强”、“减弱”或“不变”)。
③由实验可知,增加浓度NaClO稳定性增加,结合上述数据用相关原理解释。
实验结论:假设成立。
(4)、实验拓展。探索NaClO分解规律,发现其浓度和速率常数k满足下列关系:[其中b为常数,t为时间(单位为h)]。①25℃下速率常数 , c(NaClO)变为原来一半时,所需的时间约为h.(已知)。
②除添加NaCl、NaOH、浓溶液外,提出一条减缓NaClO分解的措施。
18. 工业上可由菱锌矿(主要成分为 , 还含有Ni、Cd、Fe、Mn等元素)制备ZnO。工艺如图所示:
相关金属离子形成氢氧化物沉淀的pH范围如下:
金属离子
开始沉淀的pH
1.5
6.3
6.0
7.4
8.1
6.9
沉淀完全的pH
2.8
8.3
8.0
9.4
10.1
8.9
已知①“溶浸”后的溶液 , 所含金属离子主要有:、、、、。
②弱酸性溶液中氧化时,产物中含Mn元素物质只有。
③氧化性强弱顺序:
(1)、基态Zn原子的简化电子排布式为[Ar] ,(2)、①“溶浸”过程中,为了提高浸出率,可采取的措施是。(写一条即可)②“调pH”时,可替代ZnO的一种含锌化合物是。(用化学式表示)
③“调pH”时,若 , 此时溶液中的最大浓度c=mol/L。
(3)、写出“氧化除杂”时溶液与反应的离子方程式。(4)、“还原除杂”除去的离子是;(5)、氧化锌的一种晶体的晶胞是立方晶胞(如图所示),请在图中画出该晶胞沿z轴方向的平面投影图
 19. 碘及其化合物在人类活动中占有重要地位。回答下列问题:(1)、“大象牙膏”实验中,将、KI和洗洁精混合后,短时间内产生大量的泡沫。其反应过程分为两步:
19. 碘及其化合物在人类活动中占有重要地位。回答下列问题:(1)、“大象牙膏”实验中,将、KI和洗洁精混合后,短时间内产生大量的泡沫。其反应过程分为两步:第一步: 慢反应
第二步: 快反应
该反应的决速步骤为 , 总反应方程式为;
(2)、已知:25℃下,(ⅰ)
(ⅱ)
(ⅲ)
其中,反应(ⅱ)的随温度的变化如图,若烧杯甲:将加入20mL水中(含沉淀);烧杯乙:将加入20mL KI溶液(含沉淀)。

①甲中存在平衡(ⅰ),乙中存在平衡(ⅰ)和(ⅱ),不考虑碘与水的反应以及其它反应,下列正确的是。
A.烧杯乙中剩余的沉淀质量比甲的沉淀质量小
B.室温下,甲中加水稀释,溶液中浓度一定减小
C.乙中浓度与甲中浓度相等
D.升高温度,反应ⅱ的平衡常数大于640
(3)、②为了探究乙中溶液含碘微粒的存在形式,进行实验:恒温25℃向10mL一定浓度的溶液中加入溶液,反应结束后碘元素的微粒主要存在平衡(ⅱ),相关微粒浓度如下:其中(用含c的代数式表示),若 , 说明平衡体系中。
微粒
a
b
c
(4)、③计算25℃下的平衡常数K=mol/L(写出计算过程)。20. 化合物G是合成一种杀虫剂的重要中间体,其合成路线如图:
回答下列问题:
(1)、E中含氧官能团的名称为 , E物质的手性碳原子共有个(2)、A生成B的反应类型为。(3)、写出B生成C的化学方程式。(4)、W的分子式为 , 其结构简式为。(5)、写出所有满足下列条件的A的同分异构体。①分子中含有苯环,不含其它环:②核磁共振氢谱有3组峰。
(6)、根据上述信息,写出以 和
和 为主要原料制备
为主要原料制备 合成路线。(无机试剂任选)
合成路线。(无机试剂任选)