高考二轮复习知识点:合成有机高分子化合物的性质实验
试卷更新日期:2023-08-02 类型:二轮复习
一、选择题
-
1. 有机玻璃的单体甲基丙烯酸甲酯(MMA) 的合成原理如下:
 (MMA)
(MMA)下列说法正确的是( )
A、若反应①的原子利用率为100%,则物质X为CO2 B、可用分液漏斗分离MMA和甲醇 C、 、
、  均可发生加成反应、氧化反应、取代反应
D、MMA与H2反应生成Y,能与NaHCO3溶液反应的Y的同分异构体有3种
2. 下列物质不属于高分子化合物的是( )A、顺丁橡胶 B、硬脂酸甘油酯 C、纤维素 D、蛋白质3. 合成导电高分子化合物PPV的反应为:( )
均可发生加成反应、氧化反应、取代反应
D、MMA与H2反应生成Y,能与NaHCO3溶液反应的Y的同分异构体有3种
2. 下列物质不属于高分子化合物的是( )A、顺丁橡胶 B、硬脂酸甘油酯 C、纤维素 D、蛋白质3. 合成导电高分子化合物PPV的反应为:( )
下列说法正确的是( )A、PPV 是聚苯乙烯 B、PPV 难溶于水,易溶于乙醇等有机溶剂 C、 属于芳香烃
D、1mol
属于芳香烃
D、1mol  最多可与5molH2发生反应
4. 有5种有机物:
最多可与5molH2发生反应
4. 有5种有机物:
⑤CH2=CH—CH=CH2 , 其中可用于合成
 高分子材料的正确组合为( )A、①②④ B、①②⑤ C、②④⑤ D、③④⑤5. 下列物质中,属于高分子化合物的是( )
高分子材料的正确组合为( )A、①②④ B、①②⑤ C、②④⑤ D、③④⑤5. 下列物质中,属于高分子化合物的是( )①蛋白质 ②氨基酸 ③油脂 ④淀粉 ⑤氯乙烯 ⑥纤维素 ⑦聚乙烯
A、只有①⑦ B、除②外都是 C、只有①③ D、只有①④⑥⑦6. 下列对于有机高分子化合物的叙述错误的是( )A、高分子化合物可分为天然高分子化合物和合成高分子化合物两大类 B、高分子化合物的特点之一是组成元素简单、结构复杂、相对分子质量大 C、高分子化合物均为混合物 D、合成的有机高分子化合物大部分是由小分子化合物通过聚合反应而制得的7. 下列说法正确的是( )A、甲醛俗称蚁醛、福尔马林,可用于制造酚醛树脂 B、医用酒精、84 消毒液、盐水均能使蛋白质变性而常用来家庭杀菌 C、用 FeCl3 溶液能鉴别乙醇、苯酚、己烷、溴苯 D、甘油醛是最简单的醛糖,分子中存在 1 个手性碳,一定条件下与 H2 充分反应后, 生成的氧化产物不存在手性碳二、多选题
-
8. 现代以石油化工为基础的三大合成材料是( )A、合成洗涤剂 B、合成纤维 C、合成橡胶 D、塑料
三、非选择题
-
9. 8-羟基喹啉被广泛用作金属离子的洛合剂和萃取剂,也是重要的医药中间体。下图是8-羟基喹啉的合成路线。

已知:i.

ii.同一个碳原子上连有2个羟基的分子不稳定。
(1)、按官能团分类,A的类别是。(2)、A→B的化学方程式是。(3)、C可能的结构简式是。(4)、C→D所需的试剂a是。(5)、D→E的化学方程式是。(6)、F→G的反应类型是。(7)、将下列K→L的流程图补充完整: (8)、合成8-羟基喹啉时,L发生了(填“氧化”或“还原”)反应,反应时还生成了水,则L与G物质的量之比为。10. 2−氨−3−氯苯甲酸是白色晶体,是重要的医药中间体,其制备流程如下:
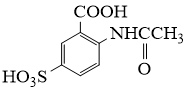
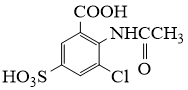
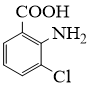
(8)、合成8-羟基喹啉时,L发生了(填“氧化”或“还原”)反应,反应时还生成了水,则L与G物质的量之比为。10. 2−氨−3−氯苯甲酸是白色晶体,是重要的医药中间体,其制备流程如下: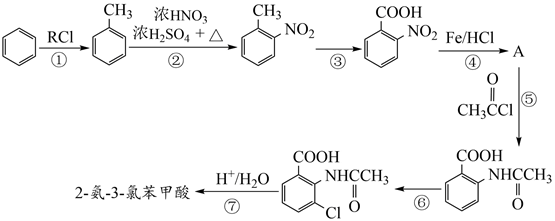
回答下列相关问题
(1)、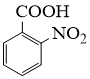 的名称是。反应②的反应类型为。 (2)、为了实现反应③的转化,通常可采用的试剂是。(3)、生成2−氨−3−氯苯甲酸的方程式为。(4)、同时符合下列两个条件的有机物共有种同分异构体。其中仅有3种等效氢的有机物结构简式为。
的名称是。反应②的反应类型为。 (2)、为了实现反应③的转化,通常可采用的试剂是。(3)、生成2−氨−3−氯苯甲酸的方程式为。(4)、同时符合下列两个条件的有机物共有种同分异构体。其中仅有3种等效氢的有机物结构简式为。①相对分子质量比
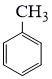 大42的苯的同系物;②与酸性KMnO4反应能生成二元羧酸;(5)、事实证明上述流程的目标产物的产率很低;据此,研究人员提出将步骤⑥设计为以下三步,产率有了一定提高。
大42的苯的同系物;②与酸性KMnO4反应能生成二元羧酸;(5)、事实证明上述流程的目标产物的产率很低;据此,研究人员提出将步骤⑥设计为以下三步,产率有了一定提高。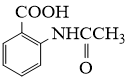
请从步骤⑥产率低的原因进行推测,上述过程能提高产率的原因可能是。若想要进一步提高产率,2−氨−3−氯苯甲酸的合成流程中,可以优化的步骤还有。
11. 乙酰苯胺( )具有退热镇痛作用,在OTC药物中占有重要地位。乙酰苯胺可通过苯胺(
)具有退热镇痛作用,在OTC药物中占有重要地位。乙酰苯胺可通过苯胺( )和乙酸反应制得,该反应是放热的可逆反应。
)和乙酸反应制得,该反应是放热的可逆反应。 已知:I.苯胺在空气中易被氧化。
II.可能用到的有关性质如下:
名称
相对分子质量
性状
密度g/cm3
熔点/℃
沸点/℃
溶解度
g/100水
g/100g乙醇
苯胺
93
棕黄色油状液体
1.02
-6.3
184
微溶
∞
冰醋酸
60
无色透明液体
1.05
16.6
117.9
∞
∞
乙酰苯胺
135
无色片状晶体
1.21
155~156
280~290
温度高,溶解度大
较水中大
I.制备乙酰苯胺的实验步骤如下:
步骤1:在制备装置加入9.2 mL苯胺、17.4 mL冰醋酸、0.1 g锌粉及少量水。
步骤2:小火加热回流1 h。
步骤3:待反应完成,在不断搅拌下,趁热把反应混合物缓慢地倒入盛有250 mL冷水的烧杯中,乙酰苯胺晶体析出。冷却,减压过滤(抽滤),制得粗乙酰苯胺。
II.乙酰苯胺的提纯
将上述制得的粗乙酰苯胺固体移人500 mL烧杯中,加入100 mL热水,加热至沸腾,待粗乙酰苯胺完全溶解后,再补加少量蒸馏水。稍冷后,加入少量活性炭吸附色素等杂质,在搅拌下微沸5 min,趁热过滤。待滤液冷却至室温,有晶体析出,称量产品为10.8 g。
回答下列问题:
(1)、写出制备乙酰苯胺的化学方程式。(2)、将三种试剂混合时,最后加入的试剂是。(3)、步骤2:小火加热回流1 h,装置如图所示。a处使用的仪器为 (填“A”、“B”或“C”),该仪器的名称是。 (4)、步骤I反应体系的温度控制在100℃~105℃,目的是。(5)、步骤II中,粗乙酰苯胺溶解后,补加少量蒸馏水的目的是。这种提纯乙酰苯胺的方法叫。(6)、乙酰苯胺的产率是 (精确到小数点后1位),导致实际值低于理论值的原因不可能是 (填字母标号)。
(4)、步骤I反应体系的温度控制在100℃~105℃,目的是。(5)、步骤II中,粗乙酰苯胺溶解后,补加少量蒸馏水的目的是。这种提纯乙酰苯胺的方法叫。(6)、乙酰苯胺的产率是 (精确到小数点后1位),导致实际值低于理论值的原因不可能是 (填字母标号)。A.没有等充分冷却就开始过滤 B.在抽滤时,有产物残留在烧杯壁
C.乙酰苯胺中的乙酸未除干净 D.抽滤时乙酰苯胺有部分溶于水中
12. 化合物J是有机合成中的一种重要中间体,具体合成过程如图:
①


②RCHO+R′CH2CHO

③
 +
+  →
→ 
④化合物A的一氯代物只有一种
(1)、I分子中含有的官能团名称为;(2)、E+F→G的反应类型为 , G→H的反应类型为;(3)、D的化学名称为;(4)、C的结构简式为 , L的结构简式为;(5)、G→J中①的化学方程式为;J→K的化学方程式为;(6)、同时满足下列条件的I的同分异构体有种(不考虑立体异构)。①与I具有相同的官能团;②具有六元碳环结构;③分子中含有一个甲基
13. 氢化阿托醛 是一种重要的化工原料,其合成路线如下:(M代表相对分子量)
是一种重要的化工原料,其合成路线如下:(M代表相对分子量)  (1)、在合成路线上①~⑤反应中,属于消去反应的为(填反应序号)。(2)、写出反应④的化学方程式:。(3)、在一定条件下,D与有机物X发生酯化反应生成E(M =164),则X的结构简式为。
(1)、在合成路线上①~⑤反应中,属于消去反应的为(填反应序号)。(2)、写出反应④的化学方程式:。(3)、在一定条件下,D与有机物X发生酯化反应生成E(M =164),则X的结构简式为。写出满足下述两个条件的E的两种同分异构体的结构简式:
a.能与NaHCO3反应产生气体 b.苯环上的一氯取代物只有一种结构 ,
(4)、氢化阿托醛被氧化后的含氧官能团的名称是。(5)、1mol氢化阿托醛最多可和mol氢气加成。(6)、由 反应的化学方程式为 14. 功能高分子P可用作光电材料,其合成路线如下:
反应的化学方程式为 14. 功能高分子P可用作光电材料,其合成路线如下: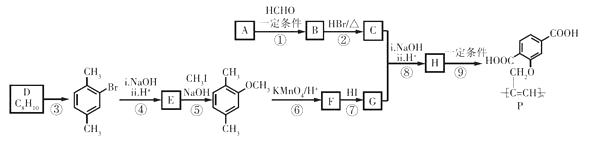
已知:
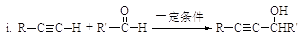 (R、R’表示氢或烃基)
(R、R’表示氢或烃基)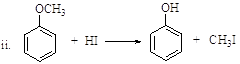
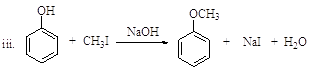 (1)、烃A的相对分子质量是26,其结构简式是。(2)、反应①的反应类型是。(3)、C中含有的官能团是。(4)、D为苯的同系物,反应③的化学方程式是。(5)、G的结构简式是。(6)、反应⑨的化学方程式是。(7)、反应⑤和⑦的目的是。(8)、以乙炔和甲醛为起始原料,选用必要的无机试剂合成1,3-丁二烯,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。15. CS(NH2)2(硫脲,白色而有光泽的晶体,溶于水,20℃时溶解度为13.6g;在150 ℃时转变成NH4SCN)是用于制造药物、染料、金属矿物的浮选剂等的原料。某化学实验小组同学用Ca(HS)2与CaCN2(石灰氮)合成硫脲并探究其性质。
(1)、烃A的相对分子质量是26,其结构简式是。(2)、反应①的反应类型是。(3)、C中含有的官能团是。(4)、D为苯的同系物,反应③的化学方程式是。(5)、G的结构简式是。(6)、反应⑨的化学方程式是。(7)、反应⑤和⑦的目的是。(8)、以乙炔和甲醛为起始原料,选用必要的无机试剂合成1,3-丁二烯,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。15. CS(NH2)2(硫脲,白色而有光泽的晶体,溶于水,20℃时溶解度为13.6g;在150 ℃时转变成NH4SCN)是用于制造药物、染料、金属矿物的浮选剂等的原料。某化学实验小组同学用Ca(HS)2与CaCN2(石灰氮)合成硫脲并探究其性质。 (1)、制备Ca(HS)2溶液,所用装置如图(已知酸性:H2CO3>H2S):
(1)、制备Ca(HS)2溶液,所用装置如图(已知酸性:H2CO3>H2S):①装置a中反应发生的操作为 ;装置b中盛放的试剂是 。
②装置c中的长直导管的作用是。
(2)、制备硫脲:将CaCN2与Ca(HS)2溶液混合,加热至80℃时,可合成硫脲,同时生成一种常见的碱,合适的加热方式是;该反应的化学方程式为。(3)、探究硫脲的性质:①取少量硫脲溶于水并加热,验证有NH4SCN生成,可用的试剂是(填化学式,下同)②向盛有少量硫脲的试管中加入NaOH溶液,有NH3放出,检验该气体的方法为 。
③可用酸性KMnO4溶液滴定硫脲,已知MnO 被还原为Mn2+ , CS(NH2)2被反应为CO2、N2及SO , 该反应中氧化剂与还原剂的物质的量之比为。
16. 某气态烃A在标准状况下的密度为1.25g/L,其产量可以用来衡量一个国家的石油化工发展水平。B和D都是生活中常见的有机物,D能跟碳酸氢钠反应,F有香味。它们之间的转化关系如下图所示: (1)、A的结构简式为 , B中官能团的电子式为 , D中官能团的名称为。(2)、反应①的反应类型是 , 反应③的化学方程式为:。(3)、反应②在Cu做催化剂的条件下进行,该实验的步骤是将红亮的铜丝置于酒精灯上加热,待铜丝变为黑色时,迅速将其插入到装有B的试管中(如图所示)。重复操作2-3次,观察到的现象是。该反应的化学方程式为。
(1)、A的结构简式为 , B中官能团的电子式为 , D中官能团的名称为。(2)、反应①的反应类型是 , 反应③的化学方程式为:。(3)、反应②在Cu做催化剂的条件下进行,该实验的步骤是将红亮的铜丝置于酒精灯上加热,待铜丝变为黑色时,迅速将其插入到装有B的试管中(如图所示)。重复操作2-3次,观察到的现象是。该反应的化学方程式为。 (4)、D与碳酸氢钠溶液反应的离子方程式为。(5)、B、D在浓硫酸的作用下实现反应④,实验装置如下图所示:
(4)、D与碳酸氢钠溶液反应的离子方程式为。(5)、B、D在浓硫酸的作用下实现反应④,实验装置如下图所示:
图中X的化学式为。浓硫酸的作用是。
该反应的化学方程式为。
17. 为回收和利用废旧塑料减轻“白色污染”,某兴趣小组进行如下探究:实验课题
探究废旧塑料热分解的主要产物为多种烃的混合物
查阅资料
①CuO能将烃氧化成CO2和H2O
②甲苯可被酸性KMnO4溶液氧化为甲酸,苯甲酸能溶于苯
实验设计

实验记录
按如图连接装置,隔绝空气强热装置A中的试管(忽略装置内空气的影响)一段时间后,可观察到如下现象:
①B装置试管中有液态物质生成
②C中溴水的颜色变浅
③E中黑色氧化铜变红
④F中无水硫酸铜变蓝
试根据上表回答下列问题:
(1)、写出一定条件下制备聚丙烯化学方程式 .(2)、经分析得知装置B试管中的液态产物是甲苯和苯的混合物.设计实验除去其中含有的甲苯 .(3)、实验中装置C的作用是 .(4)、若没有装置D,对实验结论产生的影响是 .(5)、有同学认为“E中黑色氧化铜变红,F中无水硫酸铜变蓝”是废旧聚丙烯塑料热分解产物中含氢气导致的.请你在F装置后增加一个实验装置,以确认使CuO变红是气态烃,而不是氢气,画出增加的装置图(要注明其中盛放的试剂名称)18.咖啡酸苯乙酯
 是一种天然抗癌药物,在一定条件下能发生如下转化:
是一种天然抗癌药物,在一定条件下能发生如下转化:
请填写下列空白.
(1)、D分子中的官能团是 ;高分子M的结构简式是(2)、写出A→B反应的化学方程式:(3)、B→C发生的反应类型有(4)、A的同分异构体很多种,其中,同时符合下列条件的同分异构体有 种.①苯环上只有两个取代基;②能发生银镜反应;③能与碳酸氢钠溶液反应;④能与氯化铁溶液发生显色反应.
(5)、以下对A具有的性质描述正确的是a.1molA可消耗2molNaOH
b.一定条件下1molA最多能与1mol氢气加成
c.能发生银镜反应
d.能发生取代反应.
19. 桥环化合物是指共用两个或两个以上碳原子的多环烃,广泛应用于药物合成。囧烷是结构类似我国汉字“囧”的一种桥环化合物,其合成路线如下: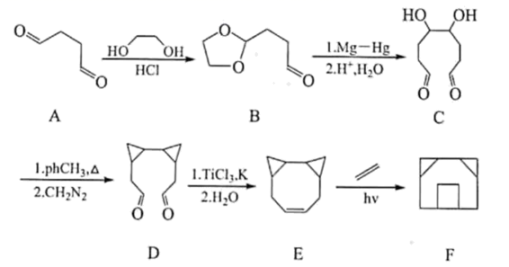 (1)、的名称是 , 中所含官能团名称为 , 的分子式为。(2)、、的反应类型分别是、。(3)、一定条件下,可以氧化为:
(1)、的名称是 , 中所含官能团名称为 , 的分子式为。(2)、、的反应类型分别是、。(3)、一定条件下,可以氧化为: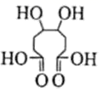 , 发生酯化反应可以形成分子内含有两个五元环的酯,该酯化反应的化学方程式为。 (4)、的同分异构体有很多种,写出同时满足下列条件的结构简式。
, 发生酯化反应可以形成分子内含有两个五元环的酯,该酯化反应的化学方程式为。 (4)、的同分异构体有很多种,写出同时满足下列条件的结构简式。①与溶液反应显紫色 ②该物质最多消耗
③核磁共振氢谱有4组峰,且峰面积比为
(5)、参照题中的合成路线并结合所学知识,以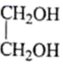 、
、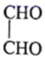 和为主要原料,设计
和为主要原料,设计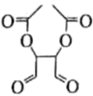 的合成路线。(其他无机试剂任选) 20. 三氯乙醛(CCl3CHO)作为有机原料,常用于生产氯霉素、氯仿等。实验室制备三氯乙醛的装置示意图(加热装置未画出)和有关数据如下:
的合成路线。(其他无机试剂任选) 20. 三氯乙醛(CCl3CHO)作为有机原料,常用于生产氯霉素、氯仿等。实验室制备三氯乙醛的装置示意图(加热装置未画出)和有关数据如下:
反应原理:
相关物质的相对分子质量及部分物理性质:
相对原子质量
熔点/℃
沸点/℃
溶解性
CH3CH2OH
46
-114.1
78.3
与水互溶
CCl3CHO
147.5
-57.5
97.8
可溶于水、乙醇
CCl3COOH
163.5
58
198
可溶于水、乙醇、三氯乙醛
回答下列问题:
(1)、仪器 a 的名称是 ,往 a 中加入盐酸,将其缓慢加入到高锰酸钾中,反应的化学方程式: 。(2)、装置 D 的作用是 ,仪器 F 的作用是 ,E 中冷凝水应从 (填“b”或“c”)口进。(3)、反应过程中若存在次氯酸,CCl3CHO 可能被氧化为 CCl3COOH,写出 CCl3CHO 被次氯酸氧化的化学反应方程式:。(4)、该设计流程存在一处缺陷导致副产物增多,请提出改进的措施: 。(5)、测定产品纯度:称取产品 0.36g 配成待测溶液,加入 0.1000mol·L-1碘标准溶液20.00mL,再加入适量 Na2CO3溶液,反应完全后加盐酸调节溶液的 pH,立即用0.0200mol·L-1 Na2S2O3溶液滴定至终点。进行三次平行实验,测得平均消耗溶液 20.00mL。则产品的纯度为 (计算结果保留三位有效数字)。( ; )21. 对硝基苯甲酸(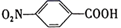 )是一种广泛用于医药、染料、感光材料等的重要精细化工中间体。工业上以对硝基甲苯(
)是一种广泛用于医药、染料、感光材料等的重要精细化工中间体。工业上以对硝基甲苯(  )、Cr(SO)3等物质为主要原料,通过间接电合成法制备对硝基苯甲酸,生产工艺流程如下:
)、Cr(SO)3等物质为主要原料,通过间接电合成法制备对硝基苯甲酸,生产工艺流程如下:

已知:①对硝基甲苯:黄色晶体,熔点为51.7℃,沸点为238.5℃,不溶于水,易溶于乙醇、乙醚、氯仿和苯。②对硝基苯甲酸:黄色晶体,熔点为242℃,沸点为359℃,微溶于水,溶于乙醇,能升华。
回答下列问题:
(1)、电解制备Cr2O72-:用H型隔膜电解槽电解制备Cr2O72- , 装置如下图1所示。外接电源的负极为(填“A”或“B”),反应II的离子方程式为。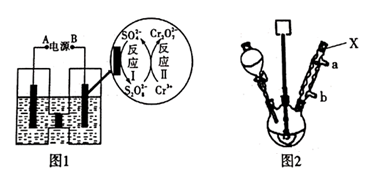 (2)、氧化制备对硝基苯甲酸:用上图2所示装置制备对硝基苯甲酸,具体过程如下:
(2)、氧化制备对硝基苯甲酸:用上图2所示装置制备对硝基苯甲酸,具体过程如下:步骤1:向250 mL三颈烧瓶中依次加入一定量含Cr2O72-的电解液、对硝基甲苯,搅拌、水浴升温到设定温度,恒温下进行反应,直至反应液由棕红色变为墨绿色时为止。
步骤2:待反应混合物冷却至室温后,与适量冰水充分混合,抽滤。滤液返回电解槽中重新电解。
步骤3:把步骤2中抽滤所得固体溶于5%的热NaOH溶液中(约60℃),待温度降到50℃时,抽滤,向滤液中加入过量2 mol/L H2SO4 , 析出黄色沉淀,再抽滤,并用冷水洗涤,然后在低于80℃的条件下烘干,可得粗产品。
①仪器X的名称是 , 冷却水应从口进入(填“a”或“b”)。
②步骤2中,抽滤所得固体的主要成分是。
③步骤3中,用NaOH溶液处理后,需待温度降到50℃时进行抽滤的原因是。
④制得的粗产品需要进一步纯化,根据对硝基苯甲酸的有关性质可知,对其进行纯化还可以采用法完成。
⑤该合成技术的优点是实现了(填化学式)的循环利用,绿色环保。
(3)、测定对硝基苯甲酸的纯度:称取1.670 g粗产品,配成100 mL溶液,取25.00 mL溶液,用0.1000 mol·L-1 KOH溶液滴定,重复滴定四次,每次消耗KOH溶液的体积如下表所示。已知:对硝基苯甲酸的摩尔质量为167.0 g·mol-1 , 则对硝基苯甲酸的纯度为。第一次
第二次
第三次
第四次
体积( mL)
23.00
23.10
21.40
22.90
22. 由有机物A和F合成I、J和高聚物H的流程如下:
已知:①

②

③有机物B的分子式为C4H6Br2 , 其核磁共振氢谱有2组峰,且峰面积之比为1:2。
请回答下列问题
(1)、有机物F的名称是 , 反应⑤利用试剂a的哪种性质? 填“氧化性”或“还原性”)。(2)、高聚物H的结构简式为 , 已知J中含有一个六元环,则J的结构简式为。(3)、D→E的化学方程式为 , 反应类型为。(4)、1mol的E生成I最多可以消耗molH2 , B和C的相对分子质量的差值为。(5)、C的同分异构体中满足下列条件的有种。①可以发生银镜反应 ②可以与金属钠反应产生氢气
-