吉林省大安三中 大安四中 大安五中2023年化学初中学业水平考试试题
试卷更新日期:2023-08-02 类型:中考模拟
一、单选题
-
1. 用如图装置进行实验(夹持仪器略去)。能体现物质 物理变化的现象是( )
 A、酒精燃烧 B、蜡烛熔化 C、火柴燃烧 D、铜片变黑2. 下列实验操作正确的是( )
A、酒精燃烧 B、蜡烛熔化 C、火柴燃烧 D、铜片变黑2. 下列实验操作正确的是( )
A、稀释浓硫酸 B、加热液体
B、加热液体  C、点燃酒精灯
C、点燃酒精灯  D、称量NaOH固体
D、称量NaOH固体  3. 一些物质的pH范围如下,其中呈碱性的是( )A、柠檬汁(2-3) B、酱油(4-5) C、西瓜汁(5-6) D、洗发水(8-9)4. 下列关于物质用途的描述不正确的是( )A、氧气可用作燃料 B、稀有气体可用作电光源 C、干冰可用作制冷剂 D、氮气可用作焊接金属时的保护气5. 下列物质的化学式书写正确的是( )A、氯化铁FeCl2 B、氧化镁MgO2 C、硫酸铜CuSO4 D、氯化铝AlCl6. “含氟牙膏”中“氟”指的是( )A、原子 B、分子 C、元素 D、单质7. 已知一种碳原子可用于测定文物的年代,该原子的原子核内含有6个质子和8个中子,则核外电子数为A、2 B、6 C、8 D、148. 下图为某化学反应的微观示意图,且各微粒恰好完全反应,其中“
3. 一些物质的pH范围如下,其中呈碱性的是( )A、柠檬汁(2-3) B、酱油(4-5) C、西瓜汁(5-6) D、洗发水(8-9)4. 下列关于物质用途的描述不正确的是( )A、氧气可用作燃料 B、稀有气体可用作电光源 C、干冰可用作制冷剂 D、氮气可用作焊接金属时的保护气5. 下列物质的化学式书写正确的是( )A、氯化铁FeCl2 B、氧化镁MgO2 C、硫酸铜CuSO4 D、氯化铝AlCl6. “含氟牙膏”中“氟”指的是( )A、原子 B、分子 C、元素 D、单质7. 已知一种碳原子可用于测定文物的年代,该原子的原子核内含有6个质子和8个中子,则核外电子数为A、2 B、6 C、8 D、148. 下图为某化学反应的微观示意图,且各微粒恰好完全反应,其中“ ”、“
”、“ ”、“
”、“ ”分别代表不同元素的原子,则构成反应物X的微粒中( )
”分别代表不同元素的原子,则构成反应物X的微粒中( ) A、一定含有
A、一定含有 和
和 B、一定含有
B、一定含有 和
和 C、只有
C、只有 D、只有
D、只有 9. 如图是甲、乙两种固体物质的溶解度曲线,下列说法中正确的是( )
9. 如图是甲、乙两种固体物质的溶解度曲线,下列说法中正确的是( ) A、甲中混有少量乙,可以用蒸发溶剂的方法得到甲 B、把100g溶质质量分数为5%的甲溶液从t2℃降温到t1℃,其溶质质量分数仍为5% C、甲的溶解能力比乙强 D、t2℃时,将甲、乙溶液恒温蒸发等质量的水,析出晶体的质量相同
A、甲中混有少量乙,可以用蒸发溶剂的方法得到甲 B、把100g溶质质量分数为5%的甲溶液从t2℃降温到t1℃,其溶质质量分数仍为5% C、甲的溶解能力比乙强 D、t2℃时,将甲、乙溶液恒温蒸发等质量的水,析出晶体的质量相同二、多选题
-
10. 下列操作能达到目的的是( )
选项
目的
操作
A
除去CO中的少量CO2
点燃
B
除去FeSO4溶液中的少量CuSO4
加入过量的铁粉
C
鉴别NaOH溶液和石灰水
取样,加入过量的稀盐酸
D
鉴别硫酸铜溶液和食盐水
观察颜色
A、A B、B C、C D、D三、填空题
-
11. 下图中A是钨元素在元素周期表中的信息,B~E是四种粒子的结构示意图,请回答:
 (1)、从A中可知,钨原子的核内质子数为。(2)、B~E四种粒子中:
(1)、从A中可知,钨原子的核内质子数为。(2)、B~E四种粒子中:①属于同种元素的是(填字母,下同)。
②具有相对稳定结构的原子是。
③与B化学性质相似的微粒是。
四、实验题
-
12. 配制50g质量分数为10%的氯化钠溶液。
 (1)、托盘天平右盘上砝码的质量为g。(2)、实验操作顺序是(填序号)。(3)、配制好的溶液中溶质和溶剂的质量比为。
(1)、托盘天平右盘上砝码的质量为g。(2)、实验操作顺序是(填序号)。(3)、配制好的溶液中溶质和溶剂的质量比为。五、填空题
-
13. 醋是日常生活中常用的调味品,主要通过大米或高粱等谷物经过发酵制成。
 (1)、谷物中富含的营养素是____(填序号)。A、糖类 B、油脂 C、蛋白质(2)、醋酸(CH3COOH)中质量分数最大的元素是。(3)、葡萄糖和酒精两种物质的共同点是。
(1)、谷物中富含的营养素是____(填序号)。A、糖类 B、油脂 C、蛋白质(2)、醋酸(CH3COOH)中质量分数最大的元素是。(3)、葡萄糖和酒精两种物质的共同点是。六、实验题
-
14. 如图,小亮同学在实验室完成“铁丝在氧气中燃烧”实验。
 (1)、为了防止高温的熔融物掉落使瓶底炸裂,可采取的操作是:。(2)、为了探究反应后所得黑色固体中是否含有铁,小亮将冷却后的黑色物质碾碎,装入试管,加入 , 说明铁燃烧后得到的黑色物质中含有铁。15. 用如图所示的装置进行实验,验证可燃物燃烧的条件并测定空气中氧气含量。
(1)、为了防止高温的熔融物掉落使瓶底炸裂,可采取的操作是:。(2)、为了探究反应后所得黑色固体中是否含有铁,小亮将冷却后的黑色物质碾碎,装入试管,加入 , 说明铁燃烧后得到的黑色物质中含有铁。15. 用如图所示的装置进行实验,验证可燃物燃烧的条件并测定空气中氧气含量。已知:白磷的着火点为40℃,红磷的着火点为240℃。
 (1)、验证可燃物燃烧的条件:向Y型管中放入足量红磷和白磷,塞好橡胶塞,关闭弹簧夹。然后将Y型管放入80℃的热水中,观察到红磷不燃烧,白磷燃烧,说明可燃物燃烧的条件之一是 , 一段时间后白磷熄灭,白磷熄灭的原因是。(2)、测定空气中氧气含量:已知Y型管的容积是60mL,待白磷熄灭,装置冷却至室温后,打开弹簧夹,会观察到量筒中的水减少了mL。
(1)、验证可燃物燃烧的条件:向Y型管中放入足量红磷和白磷,塞好橡胶塞,关闭弹簧夹。然后将Y型管放入80℃的热水中,观察到红磷不燃烧,白磷燃烧,说明可燃物燃烧的条件之一是 , 一段时间后白磷熄灭,白磷熄灭的原因是。(2)、测定空气中氧气含量:已知Y型管的容积是60mL,待白磷熄灭,装置冷却至室温后,打开弹簧夹,会观察到量筒中的水减少了mL。七、流程题
-
16. 新型材料纳米级Fe粉具有广泛的用途,它比普通Fe粉更易与氧气反应,其制备流程如图所示:
 (1)、上述流程中涉及的单质除N2外,还有。(2)、纳米级Fe粉比普通Fe粉更易与氧气反应,原因是。
(1)、上述流程中涉及的单质除N2外,还有。(2)、纳米级Fe粉比普通Fe粉更易与氧气反应,原因是。八、填空题
-
17. 如下图所示,向加有不同试剂的点滴板孔穴中分别滴加稀盐酸,研究物质的性质。
 (1)、孔穴1中观察到的现象是。(2)、孔穴2中的溶液变黄,反应的化学方程式为。(3)、从金属活动性的角度解释孔穴3、4现象不同的原因是。(4)、孔穴5中证明氢氧化钠和盐酸发生了化学反应的现象是。
(1)、孔穴1中观察到的现象是。(2)、孔穴2中的溶液变黄,反应的化学方程式为。(3)、从金属活动性的角度解释孔穴3、4现象不同的原因是。(4)、孔穴5中证明氢氧化钠和盐酸发生了化学反应的现象是。九、实验题
-
18. 根据如图中的实验装置,回答下列问题:
 (1)、用装置A制取O2 , 试管中反应的化学方程式为。(2)、检查装置B气密性的方法:关闭活塞, , 则气密性良好;(3)、C装置的优点是。(4)、若用装置D收集CO2 , 集气瓶中导管应处的位置是。(填“a”或“b”)
(1)、用装置A制取O2 , 试管中反应的化学方程式为。(2)、检查装置B气密性的方法:关闭活塞, , 则气密性良好;(3)、C装置的优点是。(4)、若用装置D收集CO2 , 集气瓶中导管应处的位置是。(填“a”或“b”)十、科学探究题
-
19. 兴趣小组在学校的实验室进行【粗盐的提纯】实验,邀请你一起完成。
Ⅰ、溶解
Ⅱ、过滤
(1)、过滤时玻璃棒的作用是。(2)、小明引同学对过滤后滤液的成分产生了浓厚的兴趣。a.粗盐中除含泥沙等难溶性杂质外,还含有CaCl2、MgCl2、Na2SO4等可溶性杂质。
b.BaSO4不溶于水、不溶于酸
【设计实验方案并进行实验】
为确认滤液中CaCl2、MgCl2、Na2SO4的存在,小明利用实验台上的NaOH溶液、BaCl2溶液、Na2CO3溶液进行以下实验探究。
实验操作
实验现象
实验结论
①往上述所得的滤液中加入足量的NaOH溶液,充分反应,静置,过滤
。
滤液中含有MgCl2
②往上述①的滤液中滴加足量的X溶液,充分反应,静置,过滤
产生白色沉淀
滤液中含有CaCl2发生反应的化学方程式为。
③往上述②的滤液中加入足量的氯化钡溶液,充分反应,静置,过滤
有白色沉淀生成
滤液中含有Na2SO4
(3)、【实验反思】小宇同学认为实验③不够严谨,理由是。
(4)、请设计实验方案验证滤液中含有Na2SO4:取少量实验③所得的白色沉淀于试管中,。(5)、【实验结论】小组同学在老师的帮助下将上述杂质除去,然后将除杂后的滤液置于蒸发皿进行蒸发结晶,当观察到 , 就停止加热,利用余热蒸干。小明宣布:我们得到了纯净的氯化钠。
十一、计算题
-
20. 某品牌炉具清洁剂的有效成分是氢氧化钠,化学兴趣小组的同学测定该炉具清洁剂中氢氧化钠的含量。取100g炉具清洁剂倒入烧杯中,逐次加入质量分数为9.8%的稀硫酸,测出溶液的pH随加入稀硫酸的质量变化关系如图所示。完成下列问题:
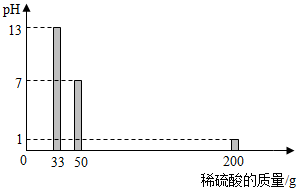 (1)、当恰好中和时,消耗的稀硫酸的质量为g。(2)、计算该炉具清洁剂中氢氧化钠的质量分数(写出计算过程)。
(1)、当恰好中和时,消耗的稀硫酸的质量为g。(2)、计算该炉具清洁剂中氢氧化钠的质量分数(写出计算过程)。
-
-
-
-
-
-
-
-