高考二轮复习知识点:中和滴定5
试卷更新日期:2023-08-01 类型:二轮复习
一、选择题
-
1. 室温下,用0.100mol•L﹣1 NaOH溶液分别滴定20.00mL 0.100mol•L﹣1的盐酸和醋酸,滴定曲线如图所示.下列说法正确的是( )
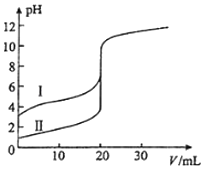 A、Ⅱ表示的是滴定醋酸的曲线 B、pH=7时,滴定醋酸消耗的V(NaOH)小于20mL C、V(NaOH)=20.00mL时,两份溶液中c(Cl﹣)=c(CH3COO﹣) D、V(NaOH)=10.00mL时,醋酸溶液中c(Na+)>c(CH3COO﹣)>c(H+)>c(OH﹣)2. NaOH溶液滴定盐酸实验中,不必用到的是( )A、酚酞 B、圆底烧杯 C、锥形瓶 D、碱式滴定管3.
A、Ⅱ表示的是滴定醋酸的曲线 B、pH=7时,滴定醋酸消耗的V(NaOH)小于20mL C、V(NaOH)=20.00mL时,两份溶液中c(Cl﹣)=c(CH3COO﹣) D、V(NaOH)=10.00mL时,醋酸溶液中c(Na+)>c(CH3COO﹣)>c(H+)>c(OH﹣)2. NaOH溶液滴定盐酸实验中,不必用到的是( )A、酚酞 B、圆底烧杯 C、锥形瓶 D、碱式滴定管3.下列图示与对应的叙述不相符合的是( )
 A、图甲表示燃料燃烧反应的能量变化 B、图乙表示酶催化反应的反应速率随反应温度的变化 C、图丙表示弱电解质在水中建立电离平衡的过程 D、图丁表示强碱滴定强酸的滴定曲线4.
A、图甲表示燃料燃烧反应的能量变化 B、图乙表示酶催化反应的反应速率随反应温度的变化 C、图丙表示弱电解质在水中建立电离平衡的过程 D、图丁表示强碱滴定强酸的滴定曲线4.室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol•L﹣1的三种酸(HA、HB和HD)溶液,滴定曲线如图所示,下列判断错误的是( )
 A、三种酸的电离常数关系:KHA>KHB>KHD B、滴定至P点时,溶液中:c(B﹣)>c(Na+)>c(HB)>c(H+)>c(OH﹣) C、pH=7时,三种溶液中:c(A﹣)=c(B﹣)=c(D﹣) D、当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH﹣)﹣c(H+)5. 常温下,在体积均为20mL、浓度均为0.1mol•L-1的HX溶液、HY溶液中分别滴加同浓度的NaOH溶液,反应后溶液中水电离的c(H+)的负对数[-lgc(H+)水]与滴加氢氧化钠溶液体积的关系如图所示:下列说法错误的是( )
A、三种酸的电离常数关系:KHA>KHB>KHD B、滴定至P点时,溶液中:c(B﹣)>c(Na+)>c(HB)>c(H+)>c(OH﹣) C、pH=7时,三种溶液中:c(A﹣)=c(B﹣)=c(D﹣) D、当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH﹣)﹣c(H+)5. 常温下,在体积均为20mL、浓度均为0.1mol•L-1的HX溶液、HY溶液中分别滴加同浓度的NaOH溶液,反应后溶液中水电离的c(H+)的负对数[-lgc(H+)水]与滴加氢氧化钠溶液体积的关系如图所示:下列说法错误的是( ) A、a、b、c三点溶液均显中性 B、a点溶液,c(Na+)=c(X-)>c(H+)=c(OH-) C、b点溶液中的离子总浓度大于d点溶液 D、常温下,Ka(HX)≈10-56. 25℃先将Cl2缓慢通入水中至饱和,然后向所得饱和氯水中滴加0.1mol/L的KOH溶液以测定氯水的浓度。此过程中溶液pH变化的曲线如图所示。
A、a、b、c三点溶液均显中性 B、a点溶液,c(Na+)=c(X-)>c(H+)=c(OH-) C、b点溶液中的离子总浓度大于d点溶液 D、常温下,Ka(HX)≈10-56. 25℃先将Cl2缓慢通入水中至饱和,然后向所得饱和氯水中滴加0.1mol/L的KOH溶液以测定氯水的浓度。此过程中溶液pH变化的曲线如图所示。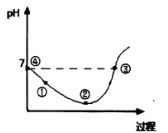
下列叙述中正确的是( )
A、滴定过程中,当水电离的c(H+)=10-7mol/L时,溶液显中性 B、滴定过程中宜选用酚酞为指示剂,不宜选用甲基橙为指示剂 C、②点的溶液中c(H+)>c(Cl-)>c(HClO)>c(ClO-) D、③点溶液中c(K+)+c(H+)=c(OH-)+c(Cl-)7. 室温下,用相同浓度的NaOH溶液分别滴定20.00mL浓度均为0.1mol·L-1的三种酸(HA、HB和HC)溶液,滴定的曲线如图所示,下列判断错误的是( ) A、当中和百分数达50%时: B、滴定至①点时,溶液中: C、当中和百分数达100%时,消耗的NaOH溶液体积 D、①和④所示溶液中都有:8. 有关酸碱中和滴定的说法正确的是( )A、可用石蕊作指示剂 B、滴定时眼睛注视滴定管中液面下降 C、需做平行实验2~3次 D、当溶液颜色变化时立即读数9. 有关酸碱滴定实验,下列说法的正确的是( )A、滴定管和锥形瓶都需要使用蒸馏水和待装液润洗 B、滴定前,必须将滴定管中液体的液面调至0刻度 C、滴定至终点时,溶液一定呈中性 D、测定待测液的浓度,至少需要完成两组平行实验,取消耗标准液的平均值10. 实验室用标准盐酸滴定氢氧化钠溶液,下列情况不影响测定结果的是( )A、洗净的锥形瓶,再用碱液润洗 B、酸式滴定管洗净后,直接注入标准盐酸 C、在放碱液时,锥形瓶中留有少量蒸馏水 D、滴定至终点时,在滴定管尖嘴部位有气泡11. 下列酸碱溶液恰好完全中和,如图所示,则下列叙述正确的是( )
A、当中和百分数达50%时: B、滴定至①点时,溶液中: C、当中和百分数达100%时,消耗的NaOH溶液体积 D、①和④所示溶液中都有:8. 有关酸碱中和滴定的说法正确的是( )A、可用石蕊作指示剂 B、滴定时眼睛注视滴定管中液面下降 C、需做平行实验2~3次 D、当溶液颜色变化时立即读数9. 有关酸碱滴定实验,下列说法的正确的是( )A、滴定管和锥形瓶都需要使用蒸馏水和待装液润洗 B、滴定前,必须将滴定管中液体的液面调至0刻度 C、滴定至终点时,溶液一定呈中性 D、测定待测液的浓度,至少需要完成两组平行实验,取消耗标准液的平均值10. 实验室用标准盐酸滴定氢氧化钠溶液,下列情况不影响测定结果的是( )A、洗净的锥形瓶,再用碱液润洗 B、酸式滴定管洗净后,直接注入标准盐酸 C、在放碱液时,锥形瓶中留有少量蒸馏水 D、滴定至终点时,在滴定管尖嘴部位有气泡11. 下列酸碱溶液恰好完全中和,如图所示,则下列叙述正确的是( ) A、因为两种酸溶液的pH相等,故V1一定等于V2 B、若V1>V2 , 则说明HA为强酸,HB为弱酸 C、若实验①中,V=V1 , 则混合液中c(Na+)=c(A-) D、实验②的混合溶液,可能溶液呈酸性12. 已知Ka(CH3COOH)=1.7×10−5 ,Kb(NH3·H2O)=1.7×10−5。常温下,用0.01mol·L−1氨水滴定20 mL浓度均为 0.01 mol·L−1的HCl和CH3COOH混合溶液,相对导电能力随加入氨水体积变化曲线如图所示。下列叙述错误的是( )
A、因为两种酸溶液的pH相等,故V1一定等于V2 B、若V1>V2 , 则说明HA为强酸,HB为弱酸 C、若实验①中,V=V1 , 则混合液中c(Na+)=c(A-) D、实验②的混合溶液,可能溶液呈酸性12. 已知Ka(CH3COOH)=1.7×10−5 ,Kb(NH3·H2O)=1.7×10−5。常温下,用0.01mol·L−1氨水滴定20 mL浓度均为 0.01 mol·L−1的HCl和CH3COOH混合溶液,相对导电能力随加入氨水体积变化曲线如图所示。下列叙述错误的是( ) A、a点的混合溶液中c(CH3COO−)约为1.7×10−5mol·L−1 B、b点的混合溶液中:c(CH3COOH) >c(NH4+) C、c点的混合溶液中: D、混合溶液pH=7时,加入氨水体积大于40mL13. 常温下,用0.1mol/LKOH溶液滴定10mL0.1mol/LHA溶液的滴定曲线如图所示。下列说法错误的是( )
A、a点的混合溶液中c(CH3COO−)约为1.7×10−5mol·L−1 B、b点的混合溶液中:c(CH3COOH) >c(NH4+) C、c点的混合溶液中: D、混合溶液pH=7时,加入氨水体积大于40mL13. 常温下,用0.1mol/LKOH溶液滴定10mL0.1mol/LHA溶液的滴定曲线如图所示。下列说法错误的是( ) A、a点pH约为3,可以判断HA是弱酸 B、b点溶液:c(A-)>c(K+)>c(HA)>c(H+)>c(OH-) C、c点溶液:c(K+)=c(A-) D、水的电离程度:c点>d点14. 室温下用等浓度的NaOH溶液滴定25.00mL0.1000mol·L-1H2C2O4溶液至终点。滴定过程得到的下列溶液中微粒的物质的量浓度关系正确的是( )
A、a点pH约为3,可以判断HA是弱酸 B、b点溶液:c(A-)>c(K+)>c(HA)>c(H+)>c(OH-) C、c点溶液:c(K+)=c(A-) D、水的电离程度:c点>d点14. 室温下用等浓度的NaOH溶液滴定25.00mL0.1000mol·L-1H2C2O4溶液至终点。滴定过程得到的下列溶液中微粒的物质的量浓度关系正确的是( )已知:①Ka1(H2C2O4)=5.4×10-2 Ka2(H2C2O4)=5.4×10-5
②设H2C2O4溶液中c(总)=c(H2C2O4)+c(HC2O4-)+c(C2O42-)
A、滴入NaOH溶液体积为25.00mL时:c(Na+)>c(H2C2O4)>c(C2O42-)>c(H+) B、pH=7的溶液:c(Na+)=c(C2O42-)+c(HC2O4-) C、当c(Na+)=2c(总)时:c(OH-)=c(H+)+c((HC2O4-)+c(H2C2O4) D、0.1000mol·L-1H2C2O4溶液:c(H+)=0.1000mol·L-1+c(C2O42-)+c(OH-)-c(H2C2O4)15. 室温下,用0.1000mol•L-1NaOH溶液滴定20mL0.1000mol•L-1H3PO4溶液,溶液的pH与所加NaOH溶液的体积关系如图所示。下列说法错误的是( ) A、H3PO4的电离平衡常数Ka1约为10-2 B、当V(NaOH溶液)=40mL时,c(PO )+c(OH-)=c(H+)+c(H2PO )+2c(H3PO4) C、当pH=7时,c(Na+)=c(H2PO )+2c(HPO )+3c(PO ) D、当V(NaOH溶液)=20mL时,c(Na+)>c(H2PO )>c(H3PO4)>c(HPO )16. 下列图示与对应的叙述正确的是( )A、
A、H3PO4的电离平衡常数Ka1约为10-2 B、当V(NaOH溶液)=40mL时,c(PO )+c(OH-)=c(H+)+c(H2PO )+2c(H3PO4) C、当pH=7时,c(Na+)=c(H2PO )+2c(HPO )+3c(PO ) D、当V(NaOH溶液)=20mL时,c(Na+)>c(H2PO )>c(H3PO4)>c(HPO )16. 下列图示与对应的叙述正确的是( )A、 反应达到平衡后,升高温度,平衡常数K值变大
B、
反应达到平衡后,升高温度,平衡常数K值变大
B、 表示镁条放入盐酸中生成氢气速率随时间的变化
C、
表示镁条放入盐酸中生成氢气速率随时间的变化
C、 表示25 ℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1氨水,溶液的pH随加入盐酸体积的变化
D、
表示25 ℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1氨水,溶液的pH随加入盐酸体积的变化
D、 表示向Al2(SO4)3溶液中滴入NaOH溶液,生成Al(OH)3沉淀的量随NaOH溶液体积的变化
17. 25℃下,向20mL0.1mol•L-1HA溶液中逐滴加入0.1mol•L-1NaOH溶液,随滴入NaOH溶液体积的变化混合溶液的pH的变化如图所示。下列说法正确的是( )
表示向Al2(SO4)3溶液中滴入NaOH溶液,生成Al(OH)3沉淀的量随NaOH溶液体积的变化
17. 25℃下,向20mL0.1mol•L-1HA溶液中逐滴加入0.1mol•L-1NaOH溶液,随滴入NaOH溶液体积的变化混合溶液的pH的变化如图所示。下列说法正确的是( ) A、A-的水解常数约为10-11 B、水的电离程度:e>d>c>b>a C、c点和d点溶液中均符合c(Na+)=c(A-) D、b点溶液中粒子浓度关系:c(A-)>c(HA)>c(H+)>c(OH-)18. 已知:pKa=- lgKa, 25℃时,弱酸H2A的pKa1=1.85,pKa2=7.19。常温下,用0.1 mo/L NaOH溶液滴定20 mL 0.1 mol/L H2A溶液的曲线如下图所示。
A、A-的水解常数约为10-11 B、水的电离程度:e>d>c>b>a C、c点和d点溶液中均符合c(Na+)=c(A-) D、b点溶液中粒子浓度关系:c(A-)>c(HA)>c(H+)>c(OH-)18. 已知:pKa=- lgKa, 25℃时,弱酸H2A的pKa1=1.85,pKa2=7.19。常温下,用0.1 mo/L NaOH溶液滴定20 mL 0.1 mol/L H2A溶液的曲线如下图所示。
下列说法错误的是( )
A、d点所得溶液中溶质的水解平衡常数Kh1=10-7.19 B、c点所得溶液中:c(Na+)+c(H+)= 2c(A2-)+ c(HA-)+ c(OH-) C、b点所得溶液中: c(A2-)>c(H2A) D、a点所得溶液中:溶质是NaHA和H2A19. 室温时,向20.0 mL 0.10 mol·L-1的两种酸HA、HB中分别滴加0.10 mol·L-1 NaOH溶液,其pH变化分别对应图中的Ⅰ、Ⅱ。下列说法错误的是( ) A、向NaA溶液中滴加HB可产生HA B、a点时,溶液中存在:c(A-)>c(Na+)>c(HA) C、滴加NaOH溶液至pH=7时,两种溶液中c(A-)=c(B-) D、滴加20.0 mL NaOH溶液时,水的电离程度:Ⅰ>Ⅱ20. 常温下,向20mL0.05mol•L-1的某稀酸H2B溶液中滴入0.1mol•L-1氨水,溶液中由水电离出氢离子浓度随滴入氨水体积变化如图。下列分析正确是( )
A、向NaA溶液中滴加HB可产生HA B、a点时,溶液中存在:c(A-)>c(Na+)>c(HA) C、滴加NaOH溶液至pH=7时,两种溶液中c(A-)=c(B-) D、滴加20.0 mL NaOH溶液时,水的电离程度:Ⅰ>Ⅱ20. 常温下,向20mL0.05mol•L-1的某稀酸H2B溶液中滴入0.1mol•L-1氨水,溶液中由水电离出氢离子浓度随滴入氨水体积变化如图。下列分析正确是( ) A、NaHB溶液中一定含有H2B分子 B、A,B,C三点溶液的pH逐渐减小,D、E、F三点溶液的pH逐渐增大 C、E溶液中离子浓度大小关系为c(NH4+)>c(B2-)>c(H+)>c(OH-) D、B点溶液pH=721. 已知某二元酸H2MO4在水中电离分以下两步:H2MO4⇌H++HMO4- , HMO4-⇌H++MO42-。常温下向20 mL0.1mol/L NaHMO4溶液中滴入cmol/LNaOH溶液,溶液温度与滴入NaOH溶液体积关系如图。下列说法正确是( )
A、NaHB溶液中一定含有H2B分子 B、A,B,C三点溶液的pH逐渐减小,D、E、F三点溶液的pH逐渐增大 C、E溶液中离子浓度大小关系为c(NH4+)>c(B2-)>c(H+)>c(OH-) D、B点溶液pH=721. 已知某二元酸H2MO4在水中电离分以下两步:H2MO4⇌H++HMO4- , HMO4-⇌H++MO42-。常温下向20 mL0.1mol/L NaHMO4溶液中滴入cmol/LNaOH溶液,溶液温度与滴入NaOH溶液体积关系如图。下列说法正确是( ) A、该氢氧化钠溶液pH=12 B、图像中F点对应的溶液中c(OH-)>c(HMO4-) C、滴入NaOH溶液过程中水的电离程度一直增大 D、图像中G点对应的溶液中c(Na+)=c(HMO4-)+2c(MO42-)22. 常温下,向20mL0.1mol• L-1HB溶液中逐滴滴入 0.1mol• L-1NaOH溶液,所得 PH变化曲线如图所示。下列说法不正确的是 ( )
A、该氢氧化钠溶液pH=12 B、图像中F点对应的溶液中c(OH-)>c(HMO4-) C、滴入NaOH溶液过程中水的电离程度一直增大 D、图像中G点对应的溶液中c(Na+)=c(HMO4-)+2c(MO42-)22. 常温下,向20mL0.1mol• L-1HB溶液中逐滴滴入 0.1mol• L-1NaOH溶液,所得 PH变化曲线如图所示。下列说法不正确的是 ( ) A、OA各点溶液均存在:c(B-) >c(Na+) B、C至 D各点溶液导电能力依次增强 C、点 O时,PH>1 D、点 C时,X约为 10.423. 在25mL0.1mol•L﹣1某一元碱中,逐滴加入0.1个mol•L﹣1醋酸,滴定曲线如图所示。则下列说法不正确的是( )
A、OA各点溶液均存在:c(B-) >c(Na+) B、C至 D各点溶液导电能力依次增强 C、点 O时,PH>1 D、点 C时,X约为 10.423. 在25mL0.1mol•L﹣1某一元碱中,逐滴加入0.1个mol•L﹣1醋酸,滴定曲线如图所示。则下列说法不正确的是( ) A、该碱溶液可以溶解Al(OH)3 B、a点对应的体积值大于25mL C、C点时,c(CH3COO﹣)>c(Na+)>c(H+)>c(OH﹣) D、D点时,c(CH3COO﹣)+c(OH﹣)=c(H+)+c(CH3COOH)24. 已知 pOH=-lgc(OH-)。向20 mL 0.1 mol·L-1 的氨水中滴加未知浓度的稀 H2SO4 , 测得混合溶液的温度、pOH随加入稀硫酸体积的变化如下图所示,下列说法不正确的是( )
A、该碱溶液可以溶解Al(OH)3 B、a点对应的体积值大于25mL C、C点时,c(CH3COO﹣)>c(Na+)>c(H+)>c(OH﹣) D、D点时,c(CH3COO﹣)+c(OH﹣)=c(H+)+c(CH3COOH)24. 已知 pOH=-lgc(OH-)。向20 mL 0.1 mol·L-1 的氨水中滴加未知浓度的稀 H2SO4 , 测得混合溶液的温度、pOH随加入稀硫酸体积的变化如下图所示,下列说法不正确的是( )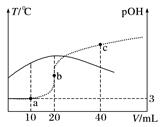 A、稀H2SO4 的物质的量浓度为0.05 mol·L-1 B、当溶液中pH=pOH时,水的电离程度最大 C、a点时溶液中存在c(NH3·H2O)+2c(OH-)=c(NH )+2c(H+) D、a、b、c 三点对应 NH 的水解平衡常数:Kh(b)>Kh(a)>Kh(c)25. 用一定浓度 NaOH 溶液滴定某醋酸溶液。滴定终点附近溶液 pH 和导电能力的变化分别如下图所示(利用溶液导电能力的变化可判断滴定终点;溶液总体积变化忽略不计)。下列说法不正确的是( )
A、稀H2SO4 的物质的量浓度为0.05 mol·L-1 B、当溶液中pH=pOH时,水的电离程度最大 C、a点时溶液中存在c(NH3·H2O)+2c(OH-)=c(NH )+2c(H+) D、a、b、c 三点对应 NH 的水解平衡常数:Kh(b)>Kh(a)>Kh(c)25. 用一定浓度 NaOH 溶液滴定某醋酸溶液。滴定终点附近溶液 pH 和导电能力的变化分别如下图所示(利用溶液导电能力的变化可判断滴定终点;溶液总体积变化忽略不计)。下列说法不正确的是( )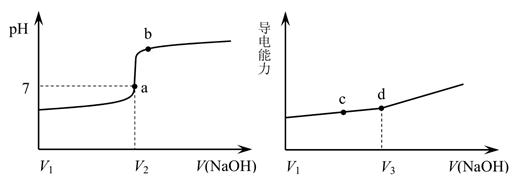 A、a 点对应的溶液中:c(CH3COO-) = c(Na+) B、a→b 过程中,n(CH3COO-)不断增大 C、c→d 溶液导电性增强的主要原因是 c(OH-)和 c(Na+)增大 D、根据溶液 pH 和导电能力的变化可判断:V2<V3
A、a 点对应的溶液中:c(CH3COO-) = c(Na+) B、a→b 过程中,n(CH3COO-)不断增大 C、c→d 溶液导电性增强的主要原因是 c(OH-)和 c(Na+)增大 D、根据溶液 pH 和导电能力的变化可判断:V2<V3二、非选择题
-
26. (15分)水中溶解氧是水生生物生存不可缺少的条件.某课外小组采用碘量法测定学校周边河水中的溶解氧.实验步骤及测定原理如下:
Ⅰ.取样、氧的固定
用溶解氧瓶采集水样.记录大气压及水体温度.将水样与Mn(OH)2碱性悬浊液(含有KI)混合,反应生成MnO(OH)2 , 实现氧的固定.
Ⅱ.酸化,滴定
将固氧后的水样酸化,MnO(OH)2被I﹣还原为Mn2+ , 在暗处静置5min,然后用标准Na2S2O3溶液滴定生成的I2(2S2O32﹣+I2=2I﹣+S4O62﹣).
回答下列问题:
(1)、取水样时应尽量避免扰动水体表面,这样操作的主要目的是 .(2)、“氧的固定”中发生反应的化学方程式为 .(3)、Na2S2O3溶液不稳定,使用前需标定.配制该溶液时需要的玻璃仪器有烧杯、玻璃棒、试剂瓶和;蒸馏水必须经过煮沸、冷却后才能使用,其目的是杀菌、除及二氧化碳.(4)、取100.00mL水样经固氧、酸化后,用a mol•L﹣1Na2S2O3溶液滴定,以淀粉溶液作指示剂,终点现象为;若消耗Na2S2O3溶液的体积为b mL,则水样中溶解氧的含量为mg•L﹣1 .(5)、上述滴定完成后,若滴定管尖嘴处留有气泡会导致测量结果偏 . (填“高”或“低”)27. 为了监测某烟道气中的NOx的含量,选用如下采样和检测方法。 (1)、I.采样步骤
(1)、I.采样步骤①检验系统气密性;②加热器将烟道气加热至140℃;③打开抽气泵置换系统内空气;④采集无尘、干燥的气样;⑤关闭系统,停止采样。
A中装有无碱玻璃棉,其作用是。采样步骤②加热烟道气的目的是。
C中填充的干燥剂最好的选择是(选填编号)。
a.碱石灰 b.无水CuSO4 c.P2O5
(2)、用实验室常用仪器组装一套装置,其作用与D(装有碱液)相同,在虚线框中画出该装置的示意图,标明气体的流向及试剂。 (3)、Ⅱ.NOx含量的测定
(3)、Ⅱ.NOx含量的测定将一定量的气样通入适量酸化的H2O2溶液中,使NOx完全被氧化为NO3- , 然后加入过量的FeSO4标准溶液,充分反应后,再用K2Cr2O7标准溶液滴定剩余的Fe2+。
NO被H2O2氧化为NO3-的离子方程式是。滴定操作使用的玻璃仪器主要有。
(4)、滴定过程中发生下列反应:3Fe2++NO3−+4H+=NO↑+3Fe3++2H2O、Cr2O72−+6Fe2++14H+=2Cr3++6Fe3++7H2O。判断下列情况对NOx含量测定结果的影响(填“偏高”、“偏低”或“无影响”):若缺少采样步骤③,会使测试结果;若FeSO4标准溶液部分变质,会使测定结果。28. 某实验小组同学为了测定工业纯碱的纯度,进行了一系列实验。(1)、和索氏制碱法相比,侯氏制碱法的优势有;(2)、工业纯碱中常含有少量NaCl杂质,解释原因 , 检验是否含有氯化钠杂质的方法为;(3)、使用重量法测定纯碱的纯度,用到的试剂有;(4)、使用滴定法测定纯碱的纯度,用(填仪器名称)称量1.200g工业纯碱样品,溶解,用1mol/L盐酸做标准液,滴定过程中溶液pH变化和生成CO2的量如图所示,A点溶液呈碱性的原因 , 计算该工业纯碱样品的质量分数。(计算结果保留两位小数)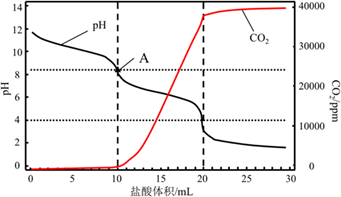 。29. H2O2是生产、生活、实验中常用的试剂。(1)、I.工业上制备H2O2的流程如下:
。29. H2O2是生产、生活、实验中常用的试剂。(1)、I.工业上制备H2O2的流程如下:
“转化”中反应的化学方程式为:“低温放置”的目的是、
(2)、图甲为“减压蒸馏”的部分装置,该装置由克氏蒸馏头和(填仪器名称)组成。 (3)、II.实验小组利用图乙装置测定阿伏加德罗常数(NA)
(3)、II.实验小组利用图乙装置测定阿伏加德罗常数(NA)实验准备
①H2O2溶液浓度标定。可选用 (填标号)试剂对H2O2溶液进行滴定,测定其浓度。
A.H2C2O4 B.KMnO4 C.淀粉KI
②装置气密性检查。打开止水夹,将注射器b的活塞推至底部,拉动注射器a活塞吸入10 mL空气,关闭止水夹。向下推动注射器a活塞至底,当观察到注射器b的现象为 , 说明装置的气密性良好。
(4)、测定过程①在反应室中加入适量MnO2 , 将注射器b活塞推至底部,关闭止水夹。用注射器a准确抽取cmol.L-1 H2O2溶液Vl mL,缓慢地注入反应室后,固定注射器a活塞。
②反应结束后,待反应体系处于状态时,读取注射器b的气体体积为V2 mL,则产生O2的体积为mL。
③设室温下O2的密度为ρ g.L-1 , 一个O2实际质量为mg,则NA=(用含ρ等字母的代数式表示)。
(5)、该实验利用H2O2作为生氧剂的优点有 (写两条)。30. 草酸钴用途广泛,可用于指示剂和催化剂的制备。用含钴废料(主要成分为 ,还含有一定量的 、 、 、 、 等)制备草酸钴晶体 的工业流程如下图所示。请回答下列问题:
已知:①草酸钴晶体难溶于水
② 为有机物(难电离)
③相关金属离子 形成氢氧化物沉淀的 范围如下:
金属离子
开始沉淀的
7.5
2.7
3.4
6.9
沉淀完全的
9.0
3.7
4.7
8.9
(1)、滤渣Ⅰ的成分。(2)、 是一种绿色氧化剂,写出加入 后溶液中发生的主要反应的离子方程式。(3)、加入氧化钴调节浸出液的 的范围是。(4)、加入有机溶剂的目的是。(5)、若仅从沉淀转化角度考虑,能否利用反应 将 转化为 (填“能”或“不能”),说明理由:。(已知 , )(6)、为测定制得的草酸钴晶体样品的纯度,现称取样品 ,先用适当试剂将其转化,稀释后得到纯净的草酸铵溶液 。移取 该溶液加入过量的稀硫酸酸化,用 高锰酸钾溶液滴定,当溶液由(填颜色变化),消耗高锰酸钾溶液 ,计算草酸钴晶体样品的纯度为 。(用含 、 、 的代数式表示)(已知 的摩尔质量为 )31. 过氧乙酸(CH3COOOH)是一种高效消毒剂,性质不稳定遇热易分解,可利用高浓度的双氧水和冰醋酸反应制得,某实验小组利用该原理在实验室中合成少量过氧乙酸。装置如图所示。回答下列问题:
已知:①常压下过氧化氢和水的沸点分别是158℃和100℃。
②过氧化氢易分解,温度升高会加速分解。
③双氧水和冰醋酸反应放出大量的热。
(1)、双氧水的提浓:蛇形冷凝管连接恒温水槽,维持冷凝管中的水温为60℃,c口接抽气泵,使装置中的压强低于常压,将滴液漏斗中低浓度的双氧水(质量分数为30%)滴入蛇形冷凝管中。①蛇形冷凝管的进水口为。
②向蛇形冷凝管中通入60℃水的主要目的是。
③高浓度的过氧化氢最终主要收集在(填圆底烧瓶A/圆底烧瓶B)。
(2)、过氧乙酸的制备:向100mL的三颈烧瓶中加入25mL冰醋酸,滴加提浓的双氧水12mL,之后加入浓硫酸1mL,维持反应温度为40℃,磁力搅拌4h后,室温静置12h。①向冰醋酸中滴加提浓的双氧水要有冷却措施,其主要原因是。
②磁力搅拌4h的目的是。
(3)、取V1mL制得的过氧乙酸溶液稀释为100mL,取出5.0mL,滴加酸性高锰酸钾溶液至溶液恰好为浅红色(除残留H2O2),然后加入足量的KI溶液和几滴指示剂,最后用0.1000mol/L的Na2S2O3溶液滴定至终点,消耗标准溶液V2mL(已知:过氧乙酸能将KI氧化为I2;2Na2S2O3+I2=Na2S4O6+2NaI)。①滴定时所选指示剂为 , 滴定终点时的现象为。
②过氧乙酸与碘化钾溶液反应的离子方程式为。
③制得过氧乙酸的浓度为mol/L。
32. 草酸铵[(NH4)2C2O4] 为无色柱状晶体,不稳定 ,受热易分解,可用于测定 Ca2+、Mg2+的含量。(1)、I.某同学利用如图所示实验装置检验草酸铵的分解产物。
实验过程中,观察到浸有酚酞溶液的滤纸变红,装置 B 中澄清石灰水变浑浊,说明分解产物中含有(填化学式);若观察到 , 说明分解产物中含有 CO。草酸铵分解的化学方程式为。
(2)、反应开始前 ,通入氮气的目的是。(3)、装置 C 的作用是。(4)、还有一种分解产物在一定条件下也能还原CuO , 该反应的化学方程式为。(5)、II.该同学利用草酸铵测定血液中钙元素的含量 。取 20.00 mL 血液样品 ,定容至 l00m L, 分别取三份体积均为25.00 mL 稀释后的血液样品,加入草酸铵,生成草酸钙沉淀,过滤,将该沉淀溶于过量稀硫酸中,然后用 0.0l00mol/L KMnO4 溶液进行滴定。滴定至终点时的实验现象为。三次滴定实验消耗 KMnO4 溶液的体积分别为0.43mL , 0.41 m L , 0.52mL, 则该血液样品中钙元素的含量为m mol/L。
33. 亚硝酰氯(ClNO)是有机物合成中的重要试剂,其沸点为-5.5℃,易水解。已知:AgNO2微溶于水,能溶于硝酸,AgNO2+HNO3=AgNO3 +HNO2 , 某学习小组在实验室用Cl2和NO制备ClNO并测定其纯度,相关实验装置如图所示。 (1)、制备Cl2的发生装置可以选用(填字母代号)装置,发生反应的离子方程式为。(2)、欲收集一瓶干燥的氯气,选择合适的装置,其连接顺序为 a→(按气流方向,用小写字母表示)。(3)、实验室可用图示装置制备亚硝酰氯:
(1)、制备Cl2的发生装置可以选用(填字母代号)装置,发生反应的离子方程式为。(2)、欲收集一瓶干燥的氯气,选择合适的装置,其连接顺序为 a→(按气流方向,用小写字母表示)。(3)、实验室可用图示装置制备亚硝酰氯:
①实验室也可用 B 装置制备 NO,X装置的优点为
②检验装置气密性并装入药品,打开K2 , 然后再打开K3 , 通入一段时间气体,其目的是 , 然后进行其他操作,当Z中有一定量液体生成时,停止实验。
(4)、已知:ClNO 与H2O反应生成HNO2和 HCl。①设计实验证明 HNO2是弱酸:。(仅提供的试剂:1 mol•L-1盐酸、1mol•L-1HNO2溶液、 NaNO2溶液、红色石蕊试纸、蓝色石蕊试纸)。
②通过以下实验测定ClNO样品的纯度。取Z中所得液体m g 溶于水,配制成250 mL 溶液;取出25.00 mL样品溶于锥形瓶中,以K2CrO4溶液为指示剂,用c mol•L-1 AgNO3标准溶液滴定至终点,消耗标准溶液的体积为20.00mL。滴定终点的现象是 , 亚硝酰氯(ClNO)的质量分数为。(已知:Ag2CrO4为砖红色固体;Ksp(AgCl)=1.56×10-10 , Ksp(Ag2CrO4)=1×10-12)
34. 草酸亚铁晶体(FeC2O4·2H2O,M=180g/mol)呈淡黄色,可用于晒制蓝图。某实验小组对其进行了一系列探究。(1)、Ⅰ.纯净草酸亚铁晶体热分解产物的探究气体产物成分的探究。小组成员采用如图装置进行实验:
A.
 B.
B.  C.
C.  D.
D.  E.
E. 
①按照气流从左到右的方向,上述装置的接口顺序为a→g→f→→尾气处理装置(仪器可重复使用)。
②检查装置气密性后,先通入一段时间N2 , 其目的为。
③实验证明了气体产物中含有CO,依据的实验现象为。
④结束实验时先熄灭A、C处的酒精灯再停止通入N2 , 其目的是。
(2)、小组成员设计实验证明了A中分解后的固体成分为FeO,则草酸亚铁晶体分解的化学方程式为。(3)、晒制蓝图时,草酸亚铁晶体是感光剂,会失去结晶水转化为FeC2O4 , 现以K3[Fe(CN)6]溶液为显色剂,该显色反应的化学方程式为。(4)、Ⅱ.草酸亚铁晶体样品纯度的测定工业制得的草酸亚铁晶体中常含有FeSO4杂质,测定其纯度的步骤如下:
步骤1:称取mg草酸亚铁晶体样品并溶于稀H2SO4中,配成250mL溶液;
步骤2:取上述溶液25.00mL,用cmol·L-1KMnO4标准液滴定至终点,消耗标准液V1mL;
步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀H2SO4 , 再用cmol·L-1KMnO4标准溶液滴定至终点,消耗标准液V2mL。
步骤2中滴定终点的现象为;步骤3中加入锌粉的目的为。
(5)、若步骤 配制溶液时部分Fe2+被氧化变质,则测定结果将(填“偏高”、“偏低”或“不变”)35. 由废铁制备FeCl2并测定FeCl2的含量。主要过程如下所示: (1)、I.按上图所示过程制备FeCl3·6H2O。
(1)、I.按上图所示过程制备FeCl3·6H2O。用离子方程式表示过程②中稀硝酸的作用:。
(2)、在过程②中要不断向溶液中补充盐酸,目的是。(3)、步骤③的操作是 。Ⅱ.由FeCl3·6H2O制得干燥FeCl2的过程如下所示:
①向盛有FeCl3·6H2O的容器中加入SOCl2 , 加热,获得无水FeCl3;
②将无水FeCl3置于反应管中,通入过程①中产生的气体一段时间后加热,生成FeCl2;
③收集FeCl2 , 保存备用。
(4)、上述过程2中产生FeCl2的化学方程式是。Ⅲ.测定FeCl2的含量。
分析方法:①取a g样品配制成100 mL溶液;②用移液管吸取所配溶液5.00 mL,放入500 mL、锥形瓶内并加水200 mL;③加硫酸锰溶液20.00mL,用0.1 mol/L酸性高锰酸钾标准溶液滴定,终点时消耗酸性高锰酸钾标准溶液V mL。
(5)、滴定终点的判断依据是。(6)、滴定时如果不加入硫酸锰很容易导致测定结果偏高,则加入硫酸锰可使测定结果准确的原因可能是 。(7)、若所配溶液中 (FeCl2) (g/L) =kV(式中V——消耗的酸性高锰酸钾标准溶液的毫升数),则k=(保留四位有效数字)。