高考二轮复习知识点:有机分子式的推断与计算
试卷更新日期:2023-08-01 类型:二轮复习
一、选择题
-
1.
 是合成平喘药沙丁胺醇的中间体,可由如下路线合成。下列叙述正确的是( )
是合成平喘药沙丁胺醇的中间体,可由如下路线合成。下列叙述正确的是( )  A、Y分子中所有原子不可能在同一平面上 B、Z的分子式为C12H12O5 C、X是乙醇的同系物 D、X的一氯代物只有2种2. X的相对分子质量为58,完全燃烧只生成 和 。下列判断正确的是( )A、若X只含C、H两种元素,则X有三种结构 B、若X能与新制 反应生成砖红色沉淀,则X是醛或甲酸酯 C、若0.1molX与足量银氨溶液反应得到43.2g的Ag,则X是 D、若X能使溴水褪色,又能与Na反应放出 ,则X是3. 某有机化合物,只含碳、氢二种元素,相对分子质量为56,完全燃烧时产生等物质的量的CO2和H2O。它可能的结构共有(需考虑顺反异构)( )A、3种 B、4种 C、5种 D、6种4. 美国“芬太尼”事件引发全世界关注,芬太尼为一种麻醉、镇痛药物,其结构简式为
A、Y分子中所有原子不可能在同一平面上 B、Z的分子式为C12H12O5 C、X是乙醇的同系物 D、X的一氯代物只有2种2. X的相对分子质量为58,完全燃烧只生成 和 。下列判断正确的是( )A、若X只含C、H两种元素,则X有三种结构 B、若X能与新制 反应生成砖红色沉淀,则X是醛或甲酸酯 C、若0.1molX与足量银氨溶液反应得到43.2g的Ag,则X是 D、若X能使溴水褪色,又能与Na反应放出 ,则X是3. 某有机化合物,只含碳、氢二种元素,相对分子质量为56,完全燃烧时产生等物质的量的CO2和H2O。它可能的结构共有(需考虑顺反异构)( )A、3种 B、4种 C、5种 D、6种4. 美国“芬太尼”事件引发全世界关注,芬太尼为一种麻醉、镇痛药物,其结构简式为 ,超剂量使用该药物会导致严重后果,下列说法正确的是( ) A、芬太尼的分子式为C22H27N2O B、芬太尼分子中含有碳碳双键 C、芬太尼分子中所有的碳原子可能共平面 D、芬太尼的一氯代物有13种(不考虑立体异构)5. 已知烯烃X与氢气反应的热化学方程式为X(g)十H2(g)=Y(g)△H<0,其中烃Y的键线式为“王”字,下列有关说法不正确的是( )A、烯烃X只有一种结构 B、烯烃X的摩尔质量为126g/mol C、烃Y的一个氢原子被C4H9取代,所得产物有12种 D、降温可以使该反应在较短时间内得到更多产物6. 在同温同压下,某有机物和过量Na反应得到V1 L氢气,另一份等量的该有机物和足量的NaHCO3反应得到V2 L二氧化碳,若V1=V2≠0,则该有机物可能是( )A、
,超剂量使用该药物会导致严重后果,下列说法正确的是( ) A、芬太尼的分子式为C22H27N2O B、芬太尼分子中含有碳碳双键 C、芬太尼分子中所有的碳原子可能共平面 D、芬太尼的一氯代物有13种(不考虑立体异构)5. 已知烯烃X与氢气反应的热化学方程式为X(g)十H2(g)=Y(g)△H<0,其中烃Y的键线式为“王”字,下列有关说法不正确的是( )A、烯烃X只有一种结构 B、烯烃X的摩尔质量为126g/mol C、烃Y的一个氢原子被C4H9取代,所得产物有12种 D、降温可以使该反应在较短时间内得到更多产物6. 在同温同压下,某有机物和过量Na反应得到V1 L氢气,另一份等量的该有机物和足量的NaHCO3反应得到V2 L二氧化碳,若V1=V2≠0,则该有机物可能是( )A、 B、HOOC﹣COOH
C、HOCH2CH2OH
D、CH3COOH
7. EDTA是一种重要的络合剂.4mol 一氯乙酸和1mol乙二胺(
B、HOOC﹣COOH
C、HOCH2CH2OH
D、CH3COOH
7. EDTA是一种重要的络合剂.4mol 一氯乙酸和1mol乙二胺( )在一定条件下发生反应生成1mol EDTA和4mol HCl,则EDTA的分子式为( ) A、C10H16N2O8 B、C10H20N2O8 C、C8H16N2O8 D、C16H20N2O8Cl8. 只含C、H、O三种元素的有机物,在空气中燃烧时消耗的O2和生成的CO2的体积比是1:2,在这类有机物中( )A、相对分子质量最小的化合物分子式是CH2O B、相对分子质量最小的化合物分子式是C2H2O C、含相同碳原子数的各化合物,其相对分子质量之差是16的整数倍 D、含相同碳原子数的各化合物,其相对分子质量之差是18的整数倍9. 过氧化氢分子中含有过氧键(﹣O﹣O﹣).有机化合物A的相对分子质量为120.经分析,其中氧的质量分数为0.5334,其余为碳和氢,则A分子中过氧键数最多为( )A、1 B、2 C、3 D、410. 鲨鱼是世界上唯一不患癌症的动物,科学研究表明,鲨鱼体内含有一种角鲨烯,具有抗癌性。实验测得角鲨烯分子是链状结构,分子中含有30个碳原子,且碳、氢元素质量比为7.2∶1,下列说法中不正确的是( )A、角鲨烯分子式为C30H50 B、角鲨烯完全加氢后为C30H60 C、1 mol角鲨烯最多可与6 mol溴单质加成 D、角鲨烯与分子式为C29H48的物质可能属于同系物11. 麻黄素有平喘作用,我国药物学家从中药麻黄中提取麻黄素作为平喘药。某实验兴趣小组用李比希法、现代仪器等测定麻黄素的分子式,测得含C、H、O、N四种元素中的若干种,其中含氮8.48%;同时将5.0g麻黄素完全燃烧可得 , , 据此,判断麻黄素的分子式为A、 B、 C、 D、12. 由乙炔()、苯()、乙醛()组成的混合物,经测定其中碳的质量分数为72%。则混合物中氧的质量分数为( )A、19.6% B、22% C、24.9% D、无法确定13. 洋川芎内酯J具有抗炎镇痛的功效,其结构简式如图所示。下列有关洋川芎内酯J的说法错误的是( )
)在一定条件下发生反应生成1mol EDTA和4mol HCl,则EDTA的分子式为( ) A、C10H16N2O8 B、C10H20N2O8 C、C8H16N2O8 D、C16H20N2O8Cl8. 只含C、H、O三种元素的有机物,在空气中燃烧时消耗的O2和生成的CO2的体积比是1:2,在这类有机物中( )A、相对分子质量最小的化合物分子式是CH2O B、相对分子质量最小的化合物分子式是C2H2O C、含相同碳原子数的各化合物,其相对分子质量之差是16的整数倍 D、含相同碳原子数的各化合物,其相对分子质量之差是18的整数倍9. 过氧化氢分子中含有过氧键(﹣O﹣O﹣).有机化合物A的相对分子质量为120.经分析,其中氧的质量分数为0.5334,其余为碳和氢,则A分子中过氧键数最多为( )A、1 B、2 C、3 D、410. 鲨鱼是世界上唯一不患癌症的动物,科学研究表明,鲨鱼体内含有一种角鲨烯,具有抗癌性。实验测得角鲨烯分子是链状结构,分子中含有30个碳原子,且碳、氢元素质量比为7.2∶1,下列说法中不正确的是( )A、角鲨烯分子式为C30H50 B、角鲨烯完全加氢后为C30H60 C、1 mol角鲨烯最多可与6 mol溴单质加成 D、角鲨烯与分子式为C29H48的物质可能属于同系物11. 麻黄素有平喘作用,我国药物学家从中药麻黄中提取麻黄素作为平喘药。某实验兴趣小组用李比希法、现代仪器等测定麻黄素的分子式,测得含C、H、O、N四种元素中的若干种,其中含氮8.48%;同时将5.0g麻黄素完全燃烧可得 , , 据此,判断麻黄素的分子式为A、 B、 C、 D、12. 由乙炔()、苯()、乙醛()组成的混合物,经测定其中碳的质量分数为72%。则混合物中氧的质量分数为( )A、19.6% B、22% C、24.9% D、无法确定13. 洋川芎内酯J具有抗炎镇痛的功效,其结构简式如图所示。下列有关洋川芎内酯J的说法错误的是( ) A、分子式为 B、含有三种官能团 C、能使酸性高锰酸钾溶液褪色 D、不能与溶液发生反应14. 某烷烃 X分子中碳与氢的质量比为 36∶7。现取两支试管,分别加入适量溴水,实验操作及现象如下:
A、分子式为 B、含有三种官能团 C、能使酸性高锰酸钾溶液褪色 D、不能与溶液发生反应14. 某烷烃 X分子中碳与氢的质量比为 36∶7。现取两支试管,分别加入适量溴水,实验操作及现象如下:
有关 X 的说法正确的是( )
A、相同条件下,X 的密度比水大 B、X的分子式为C6H14 , X的同分异构体共有 6 种 C、X 能与 Br2发生加成反应使溴水褪色 D、试验后试管 2 中的有机层是上层还是下层,可通过加水确定二、多选题
-
15. 扁桃酸的衍生物a、b、c均为重要的医药中间体。下列说法正确的是( )
 A、一定条件下,a可与HCHO发生缩聚反应 B、可用NaHCO3溶液区别a、b C、b与浓溴水混合可制备c D、1molc最多可与2molNaOH反应16. 将15.1g某芳香族化合物样品置于氧气流中完全燃烧,测得有关数据如下(实验前系统内的空气已排除,各步均吸收完全):
A、一定条件下,a可与HCHO发生缩聚反应 B、可用NaHCO3溶液区别a、b C、b与浓溴水混合可制备c D、1molc最多可与2molNaOH反应16. 将15.1g某芳香族化合物样品置于氧气流中完全燃烧,测得有关数据如下(实验前系统内的空气已排除,各步均吸收完全):燃烧产物 增重8.1g 增重35.2g 氮气1.12L(标况)
已知该有机物相对分子质量为151,且为天然蛋白质水解产物。下列关于该有机物的说法正确的是( )
A、分子式为C8H9N2O B、结构简式为 C、含有1个手性碳原子
D、既可与强酸反应又可与强碱反应
17. 某气态烷烃和一气态单烯烃组成的混合气体在同温、同压下对氢气的相对密度为13,取标准状况下此混合气体4.48L,通入足量的溴水,溴水的质量增加2.8g,此2种烃是( )A、甲烷和丙烯 B、甲烷和2﹣丁烯 C、甲烷和2﹣甲基丙烯 D、乙烯和1﹣丁烯
C、含有1个手性碳原子
D、既可与强酸反应又可与强碱反应
17. 某气态烷烃和一气态单烯烃组成的混合气体在同温、同压下对氢气的相对密度为13,取标准状况下此混合气体4.48L,通入足量的溴水,溴水的质量增加2.8g,此2种烃是( )A、甲烷和丙烯 B、甲烷和2﹣丁烯 C、甲烷和2﹣甲基丙烯 D、乙烯和1﹣丁烯三、非选择题
-
18. 元素分析是有机化合物的表征手段之一。按下图实验装置(部分装置略)对有机化合物进行C、H元素分析。
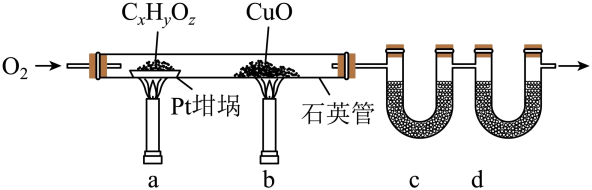
回答下列问题:
(1)、将装有样品的Pt坩埚和CuO放入石英管中,先 , 而后将已称重的U型管c、d与石英管连接,检查。依次点燃煤气灯 , 进行实验。(2)、O2的作用有。CuO的作用是(举1例,用化学方程式表示)。(3)、c和d中的试剂分别是、(填标号)。c和d中的试剂不可调换,理由是。A.CaCl2 B.NaCl C.碱石灰(CaO+NaOH) D.Na2SO3
(4)、Pt坩埚中样品CxHyOz反应完全后,应进行操作:。取下c和d管称重。(5)、若样品CxHyOz为0.0236g,实验结束后,c管增重0.0108g,d管增重0.0352g。质谱测得该有机物的相对分子量为118,其分子式为。19. 将3.00g某有机物(仅含C、H、O元素,相对分子质量为150)样品置于燃烧器中充分燃烧,依次通过吸水剂、CO2吸收剂,燃烧产物被完全吸收。实验数据如下表:吸水剂
CO2吸收剂
实验前质量/g
20.00
26.48
实验后质量/g
21.08
30.00
请回答:
(1)、燃烧产物中水的物质的量为mol。(2)、该有机物的分子式为(写出计算过程)。20.化合物G是治疗高血压的药物“比索洛尔”的中间体,一种合成G的路线如下:

已知以下信息:
①A的核磁共振氢谱为单峰;B的核磁共振氢谱为三组峰,峰面积比为6:1:1.
②D的苯环上仅有两种不同化学环境的氢;1molD可与1mol NaOH或2mol Na反应.
回答下列问题:
(1)、A的结构简式为 .(2)、B的化学名称为 .(3)、C与D反应生成E的化学方程式为 .(4)、由E生成F的反应类型为 .(5)、G是分子式为 .(6)、L是D的同分异构体,可与FeCl3溶液发生显色反应,1mol的L可与2mol的Na2CO3反应,L共有种;其中核磁共振氢谱为四组峰,峰面积比为3:2:2:1的结构简式为、 .21. 室温时,20mL某气态烃与过量的氧气混合,将完全燃烧后的产物通过浓硫酸,再恢复至室温,气体体积减少了50mL。将剩余的气体再通过足量氢氧化钠溶液后干燥,体积又减少了40mL。(1)、该气态烃的分子式。(2)、写出简要计算过程 。22. AigialomycinD是从海生红树林菌类中分离出来的一种具有重要生理活性的物质,具有极强的抗癌活性和抗疟疾活性。一种合成路线为:
已知:①已知,Et为乙基,Ph为苯基
②

回答下列问题:
(1)、AigialomycinD中含氧官能团的名称是 , C分子的核磁共振氢谱中有组峰。(2)、C→D的化学方程式为 , D→E的反应类型为。(3)、F的分子式为。(4)、符合下列条件的D的同分异构体有种①含有苯环且有四个羟基与苯环直接相连
②苯环上无氢原子
(5)、官能团的保护是有机合成中的重要步骤,写出制备AigialomycinD中引入保护基的步骤(例如X→Y)(6)、写出以 为原料制备
为原料制备 的合成路线(其他试剂任选,注明反应条件)。 23. 博苏替尼(化合物I)是一种抗肿瘤药物,某课题组设计的合成路线如图(部分反应条件已省略):
的合成路线(其他试剂任选,注明反应条件)。 23. 博苏替尼(化合物I)是一种抗肿瘤药物,某课题组设计的合成路线如图(部分反应条件已省略):
已知:
 (1)、下列说法不正确的是____。A、化合物A能消耗 B、化合物D可以和溶液发生显色反应 C、化合物F既可以和酸反应,又可以和碱反应 D、H的分子式为(2)、化合物E的结构简式为 , 流程中 , 而不是由A直接与反应生成C的原因是。(3)、写出化合物C转化为D的化学方程式。(4)、写出符合下列条件的化合物B的同分异构体。
(1)、下列说法不正确的是____。A、化合物A能消耗 B、化合物D可以和溶液发生显色反应 C、化合物F既可以和酸反应,又可以和碱反应 D、H的分子式为(2)、化合物E的结构简式为 , 流程中 , 而不是由A直接与反应生成C的原因是。(3)、写出化合物C转化为D的化学方程式。(4)、写出符合下列条件的化合物B的同分异构体。①能使溶液显色;
②可以发生银镜反应;
③谱显示只有4种不同化学环境的氢原子。
(5)、写出以邻硝基苯甲酸为原料合成 的合成路线。 24. 化合物X由4种元素组成。某兴趣小组按如图流程进行实验(每一步反应均充分进行):
的合成路线。 24. 化合物X由4种元素组成。某兴趣小组按如图流程进行实验(每一步反应均充分进行):
请回答:
(1)、组成X的4种元素是(填元素符号)。(2)、无色溶液D中的溶质是(填化学式)。(3)、无色气体A中的气体分子有(填化学式)。(4)、气态X分子中,H原子与2种元素的原子形成共价键,但红外光谱和1H核磁共振谱均显示固态X晶体中的H原子化学环境完全相同。且熔点明显高于相对分子量接近的分子晶体,原因是。(5)、X能与氯酸钾在水溶液中反应,得到无色溶液F和无色气体C。①写出该反应的化学方程式:。
②设计实验验证该无色溶液F中的阴离子:。
25. 常温下,青蒿素为无色针状晶体,难溶于水,易容有机溶剂,熔点为156-157℃。青蒿素是一种有效的抗疟药,某化学兴趣小组对青蒿素的提取和组成进行如下的探究。Ⅰ.提取青高素的方法之一是乙醚浸取法,提取流程如下:
 (1)、对青蒿进行破碎的目的是(2)、操作Ⅰ用到的玻璃仪器是 , 操作Ⅱ的名称是(3)、Ⅱ.燃烧法测定青蒿素的最简式:
(1)、对青蒿进行破碎的目的是(2)、操作Ⅰ用到的玻璃仪器是 , 操作Ⅱ的名称是(3)、Ⅱ.燃烧法测定青蒿素的最简式:利用下列实验装置,将28.2g青蒿素放在燃烧管C中充分燃绕,测出生成的CO2和H2O的质量后,计算得出青蒿素的最简式。

主要实验步骤如下:
①组装仪器,并检查装置的气密性。
②先将A装置的药品反应一会后,再将C装置通电反应。
③称量有关装置的实验前后的质量。
请回答下列问题:
仪器各接口的连接顺序从左到右依次为(每个装置限用一次)。
(4)、①装置B中的试剂为 , 其作用是。②装置C中CuO的作用是。
③装置D中的试剂为 , 其作用是。
④装置E中的试剂为 , 其作用是。
⑤装置F中的试剂为 , 其作用是。
(5)、已知青蒿素是烃的含氧衍生物,用合理连接后的装置进行实验,测量数据如表:装置质量
实验前/g
实验后/g
B
22.6
42.4
E
80.2
146.2
则青蒿素的最简式为 .
26. 肉桂酸甲酯(H)是常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精。它的分子式为C10H10O2 , 且分子中只含有1个苯环,苯环上只有一个取代基。利用红外光谱仪可初步检测有机化合物中的某些基团,现测得H分子的红外光谱如下图所示:
又知J为肉桂酸甲酯的一种同分异构体,其分子结构模型如下图所示(图中球与球之间的连线表示单键或双键等化学键)。

试回答下列问题:
(1)、肉桂酸甲酯(H)的结构简式为。(2)、现测出A的核磁共振氢谱图有6个峰,且面积之比为1∶2∶2∶2∶1∶2。用芳香烃A为原料合成H的路线如下(部分反应物和反应条件已略去):
①化合物F中的官能团有(填名称)。
②F→G的反应类型是。
③书写下列化学方程式:
F→I:。
G→H:。
④其中F的同分异构体甚多,其中有一类可用通式
 表示(其中X、Y均不为氢原子),试写出符合上述通式且能发生银镜反应的四种物质的结构简式:。27. 某小组欲研究烷烃的某些性质设计下图实验装置。回答下列问题:
表示(其中X、Y均不为氢原子),试写出符合上述通式且能发生银镜反应的四种物质的结构简式:。27. 某小组欲研究烷烃的某些性质设计下图实验装置。回答下列问题:Ⅰ.烷烃可以发生取代反应。
向下图的B中通入一定量的氯气和甲烷气体,混合均匀后通入C中硬质玻璃管中,夹紧C两端弹簧夹,用强光照射硬质玻璃管。
 (1)、将实验室制得的先通过饱和食盐水的目的是。(2)、写出装置C中与反应生成氯仿的化学方程式。(3)、一段时间后,C中玻璃管内的实验现象、。(4)、若2 mol 与发生取代反应,测得生成4种有机取代产物的物质的量相等,则消耗的氯气的物质的量是mol。(5)、某丁烷与氯气发生反应的产物之一为 , 则分子式为的同分异构体有种。
(1)、将实验室制得的先通过饱和食盐水的目的是。(2)、写出装置C中与反应生成氯仿的化学方程式。(3)、一段时间后,C中玻璃管内的实验现象、。(4)、若2 mol 与发生取代反应,测得生成4种有机取代产物的物质的量相等,则消耗的氯气的物质的量是mol。(5)、某丁烷与氯气发生反应的产物之一为 , 则分子式为的同分异构体有种。Ⅱ.烷烃可以发生氧化反应。
将一定量的某烷烃在足量氧气中充分燃烧,并使产生的气体全部通入下图装置,得到如表所列的实验数据(U形管中干燥剂只吸收水蒸气且假设产生的气体完全被吸收)。

实验前
实验后
实验前实验后(干燥剂+U形管)的质量
101.1g
102.9g
(石灰水+广口瓶)的质量
312.0g
315.3g
(6)、试写出该烷烃分子式为。28. 按系统命名法给下列有机物命名:(1)、 的名称是。 (2)、有A、B、C三种烃,已知:
的名称是。 (2)、有A、B、C三种烃,已知:①B完全燃烧的产物;
②C为饱和链烃,通常状况下呈气态,其二氯代物有三种;
③A是B分子中的氢原子全部被甲基取代后的产物;A遇的溶液不褪色,其一氯代物只有一种。
请回答下列问题:
(Ⅰ)B的最简式为 , 分子式为 , 其二溴代物有种。
(Ⅱ)C的三种二氯代物的结构简式分别为、、。
(Ⅲ)A的结构简式为 , 名称为。
29. 如图所示装置是用燃烧法确定有机物化学式常用的装置,这种方法是电炉加热时用纯氧氧化管内样品,根据产物的质量确定有机物的组成。回答下列问题: (1)、A装置中发生反应的化学方程式是。(2)、E装置中所盛放试剂的名称是。(3)、若实验中所取样品只含C、H、O三种元素中的两种或三种,准确称取0.44g样品,经充分反应后,D管质量增加0.36g,E管质量增加0.88g,已知该物质的相对分子质量为44,则该样品的化学式为。(4)、若符合下列条件,则该有机物的结构简式为。
(1)、A装置中发生反应的化学方程式是。(2)、E装置中所盛放试剂的名称是。(3)、若实验中所取样品只含C、H、O三种元素中的两种或三种,准确称取0.44g样品,经充分反应后,D管质量增加0.36g,E管质量增加0.88g,已知该物质的相对分子质量为44,则该样品的化学式为。(4)、若符合下列条件,则该有机物的结构简式为。①环状化合物
②核磁共振氢谱图中只有一组峰
(5)、某同学认为E和空气相通,会影响测定结果准确性,应在E后再增加一个装置F,其主要目的是。30. 某化合物X由三种元素组成,其转化关系如下图所示:
已知:无色气体3在空气中转变为红棕色气体1。
回答以下问题:
(1)、在元素周期表中的位置;(2)、步骤②的化学反应方程式是;(3)、气体1与水发生反应的离子反应方程式;(4)、鉴别红棕色气体1与蒸气的下列方法中,合理的是____A、通入水中观察溶液的颜色变化 B、直接观察两种气体的颜色 C、分别通入溶液中观察有否沉淀 D、用湿润的淀粉试纸检验是否变蓝色(5)、化合物X的化学式为31. 乳酸乙酯(A)是一种食用香料。由淀粉或D为原料合成乳酸乙酯的流程图如下:
已知:①D的产量可用于衡量一个国家石油化学工业的发展水平;
②乳酸的结构简式为
 。
。回答下列问题:
(1)、乳酸中所含的官能团名称为 , C→A的反应类型为 , A的分子式为。(2)、B是否能发生银镜反应(填“是”或“否)。(3)、D通过加聚反应形成高分子化合物的化学方程式为。(4)、下列与乳酸互为同分异构体的物质是(填序号)。①CH3CH2OH②CH3COOH③
 ④
④ ⑤
⑤ ⑥
⑥ (5)、1mol乳酸分别与足量Na、反应,消耗二者的物质的量之比为。32. 已知烃A其产量可以用来衡量一个国家石油化工发展水平。A、B、D、E、F、G转化关系如下(以下变化中,有些反应条件及产物未标明)。其中G是天然有机高分子化合物,E分子具有浓郁的果香味,其相对分子质量为88。
(5)、1mol乳酸分别与足量Na、反应,消耗二者的物质的量之比为。32. 已知烃A其产量可以用来衡量一个国家石油化工发展水平。A、B、D、E、F、G转化关系如下(以下变化中,有些反应条件及产物未标明)。其中G是天然有机高分子化合物,E分子具有浓郁的果香味,其相对分子质量为88。 (1)、写出A分子的电子式:;F的分子式:。(2)、A在一定条件下发生加聚反应的化学方程式为 , B→乙醛的化学方程式:。(3)、写出B+D→E的化学方程式: , 反应类型为。(4)、E的同分异构体中,能与NaHCO3溶液反应生成气体的物质是(用结构简式书写一种即可)。33. 某种烷烃完全燃烧后生成了8.8gCO2和5.4gH2O,据此推测其分子式。34. 46 g某无色液体CxHyOH (纯净物)与足量钠完全反应,得到11.2 L氢气(标准状况),通过计算确定CxHyOH的结构简式。35. 实验室用燃烧法测定某固体有机物A的分子组成,测定装置如图所示(夹持仪器、酒精灯等已略去)。
(1)、写出A分子的电子式:;F的分子式:。(2)、A在一定条件下发生加聚反应的化学方程式为 , B→乙醛的化学方程式:。(3)、写出B+D→E的化学方程式: , 反应类型为。(4)、E的同分异构体中,能与NaHCO3溶液反应生成气体的物质是(用结构简式书写一种即可)。33. 某种烷烃完全燃烧后生成了8.8gCO2和5.4gH2O,据此推测其分子式。34. 46 g某无色液体CxHyOH (纯净物)与足量钠完全反应,得到11.2 L氢气(标准状况),通过计算确定CxHyOH的结构简式。35. 实验室用燃烧法测定某固体有机物A的分子组成,测定装置如图所示(夹持仪器、酒精灯等已略去)。
取17.1gA放入装置中,通入过量 燃烧,请回答下列有关问题:
(1)、C装置的作用是 , E装置的作用是。当燃烧完全后,还要继续通入一段时间 的目的是。(2)、若A的摩尔质量为342g/mol,C装置增重9.9g,D装置增重26.4g,则A的分子式。(3)、A燃烧的化学方程式为。A可发生水解反应,1molA可水解生成2种互为同分异构体的产物,则A在催化剂作用下水解的化学方程式为。36. 有机物A的相对分子质量大于130,小于180。碳元素和氢元素的质量分数之和为60%;其余为氧元素。(1)、该有机物的相对原子质量为(要求写出必要的计算过程)(2)、该有机物分子中最多含有碳氧双键的个数为。