广东省广州市2023年中考三模化学试题
试卷更新日期:2023-07-31 类型:中考模拟
一、单选题
-
1. 下列广东美食中富含淀粉的是( )A、客家豆腐 B、广式腊肠 C、岭南荔枝 D、陈村米粉2. 科技带来进步。下列物质使用的材料中,属于有机合成材料的是( )A、“奋斗者”号潜水艇载人舱的抗压材料—新型钛合金 B、北京冬奥会使用的冰球—合成橡胶 C、航天服的内衣舒适层材料(质地柔软、吸湿性和透气性良好)—棉针织品 D、我国自主研发的纯电动跑车使用的减重材料—碳纤维复合材料3. 下列有关说法正确的是( )A、工业上从空气中分离出氧气属于化学变化 B、用石灰浆刷墙壁,干燥后墙面变硬发生了化学变化 C、石油分馏后得到汽油、煤油、柴油等属于化学变化 D、干冰升华是化学变化4. 下列物质属于纯净物的是( )
①酒精;②天然气;③冰醋酸;④消毒酒精;⑤石灰水;⑥石油;⑦甲醇;⑧金刚石。
A、①③⑦⑧ B、①④⑧ C、①②④⑧ D、②④⑥5. 空气是一种宝贵的资源,下列关于空气的说法正确的是( )A、空气中的氧气约占总质量的21% B、空气中的氧气能做燃料 C、空气中各成分的含量相对比较稳定 D、空气中的二氧化碳过量排放会造成酸雨6. 2018年和2019年我国电力能源结构如图所示,下列说法不正确的是( ) A、水能、风能、太阳能都是清洁能源 B、减少煤的使用有利于防止温室效应进一步增强 C、煤燃烧产生的CO2和SO2都是形成酸雨的污染物 D、我国电力能源结构的变化体现了“低碳”理念7. 丁酸乙酯(C6H12O2)常用作食品、饮料的调香剂。关于它的叙述正确的是( )A、丁酸乙酯的相对分子质量为20 B、丁酸乙酯中含有20个原子 C、一个丁酸乙酯分子中,碳、氢、氧原子的个数比为3:6:2 D、丁酸乙酯中碳、氢、氧元素的质量比为18:3:88. 下列有关物质—性质—用途的叙述中,用途与性质不相关的是( )
A、水能、风能、太阳能都是清洁能源 B、减少煤的使用有利于防止温室效应进一步增强 C、煤燃烧产生的CO2和SO2都是形成酸雨的污染物 D、我国电力能源结构的变化体现了“低碳”理念7. 丁酸乙酯(C6H12O2)常用作食品、饮料的调香剂。关于它的叙述正确的是( )A、丁酸乙酯的相对分子质量为20 B、丁酸乙酯中含有20个原子 C、一个丁酸乙酯分子中,碳、氢、氧原子的个数比为3:6:2 D、丁酸乙酯中碳、氢、氧元素的质量比为18:3:88. 下列有关物质—性质—用途的叙述中,用途与性质不相关的是( )物质
性质
用途
A
氧气
助燃性
火箭燃料
B
一氧化碳
还原性
冶炼金属
C
稀有气体
化学性质不活泼
保护气
D
活性炭
吸附性
防毒面具
A、A B、B C、C D、D9. “宏观一微观一符号”三重表征是化学独特的表示物质及其变化的方法。某化学反应的微观示意图如图所示,下列说法正确的是( ) A、从反应价值看:该反应能获取清洁能源,延缓温室效应 B、从物质分类看:该反应涉及2种氧化物 C、从微观构成看:只有3种物质由分子构成 D、从表示方法看:该反应的化学方程式为2CO2+4H2O2CH4+3O210. 如图为Na2SO4与NaCl的溶解度曲线,下列说法正确的是( )
A、从反应价值看:该反应能获取清洁能源,延缓温室效应 B、从物质分类看:该反应涉及2种氧化物 C、从微观构成看:只有3种物质由分子构成 D、从表示方法看:该反应的化学方程式为2CO2+4H2O2CH4+3O210. 如图为Na2SO4与NaCl的溶解度曲线,下列说法正确的是( ) A、30℃时,Na2SO4的溶解度为41 B、P点表示该温度下,两饱和溶液中溶质质量相等 C、20℃时,Na2SO4饱和溶液的溶质质量分数为19.5% D、40℃时,等质量的Na2SO4和NaCl的饱和溶液分别降温到10℃,获得晶体较多的是Na2SO411. 下列的物质性质和用途,有直接联系的是( )A、浓硫酸有腐蚀性,在实验室中可用作干燥剂 B、熟石灰溶于水呈碱性,可用于改良酸性土壤 C、碳酸氢铵受热易分解,可用作化肥 D、金刚石无色透明,可用于制作钻头12. 下列实验方案中,能达到目的的是( )
A、30℃时,Na2SO4的溶解度为41 B、P点表示该温度下,两饱和溶液中溶质质量相等 C、20℃时,Na2SO4饱和溶液的溶质质量分数为19.5% D、40℃时,等质量的Na2SO4和NaCl的饱和溶液分别降温到10℃,获得晶体较多的是Na2SO411. 下列的物质性质和用途,有直接联系的是( )A、浓硫酸有腐蚀性,在实验室中可用作干燥剂 B、熟石灰溶于水呈碱性,可用于改良酸性土壤 C、碳酸氢铵受热易分解,可用作化肥 D、金刚石无色透明,可用于制作钻头12. 下列实验方案中,能达到目的的是( )选项
实验目的
实验方案
A
除去盐酸中的少量硫酸
加入过量Ba(NO3)2溶液后过滤
B
除去MgCl2溶液中的少量盐酸
加入过量MgO后过滤
C
鉴别NH4Cl和K2CO3固体
取样,加入CaCl2粉末,研磨、闻气味
D
鉴别NaCl和Na2SO4溶液
取样,滴加Mg(NO3)2溶液,观察现象
A、A B、B C、C D、D13. 由下列实验及现象可出相应结论的是( )选项
实验
现象
结论
A
检验氢气的纯度

点燃氢气时发出尖锐爆鸣声
氢气较纯
B
称量盐酸和碳酸钠粉末反应前后的质量

反应前后称量结果不同
参加该反应的反应物质量总和不等于生成物质量总和
C
检验某混合气体的成分
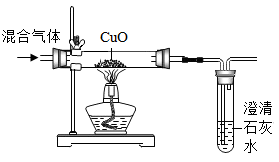
黑色粉末变红,澄清石灰水变浑浊
混合气体中可能含有CO
D
在酒精灯火焰上方罩一个冷而干燥的烧杯

烧杯内壁有无色液滴产生
酒精中含有碳元素和氢元素
A、A B、B C、C D、D二、多选题
-
14. 下列关于金属或合金的说法中,不正确的是( )A、合金一般比组成他们的纯金属硬度大、抗腐蚀性强、熔点高 B、铁制品表面刷漆或镀耐腐蚀性金属都可以防止铁制品锈蚀 C、铝锅上的污垢可以用砂纸或钢丝球打磨 D、回收利用废旧电池中的铅、汞等可减少对环境的污染
三、实验题
-
15. 盐酸是实验室中最常用的化学试剂之一。某校学生利用如图所示实验探究酸的性质。
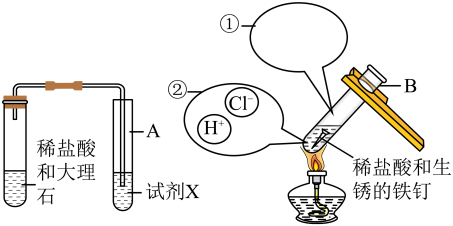 (1)、试管A中试剂X由澄清变浑浊,则试剂X为(写化学式)溶液。(2)、试管B中观察到铁钉变得光亮,表面有少量气泡产生,溶液变成色。将此时溶液中和液面上方存在的微观粒子的种类在图中补充完整(粒子数目不作要求,不考虑空气、水及水蒸气)。但实际生产中用稀盐酸除铁锈时不能长期将铁制品浸在盐酸中,理由是。(3)、将上述两个实验产生的废液收集到一个烧杯中并处理,先要测定溶液的酸碱性,请写出用pH试纸测量该废液酸碱度的操作。
(1)、试管A中试剂X由澄清变浑浊,则试剂X为(写化学式)溶液。(2)、试管B中观察到铁钉变得光亮,表面有少量气泡产生,溶液变成色。将此时溶液中和液面上方存在的微观粒子的种类在图中补充完整(粒子数目不作要求,不考虑空气、水及水蒸气)。但实际生产中用稀盐酸除铁锈时不能长期将铁制品浸在盐酸中,理由是。(3)、将上述两个实验产生的废液收集到一个烧杯中并处理,先要测定溶液的酸碱性,请写出用pH试纸测量该废液酸碱度的操作。四、科普阅读题
-
16. 阅读下面科普短文,回答问题。
材料一:无处安放的“核废水”
2011年3月11日,日本东北太平洋地区发生里氏9筑地震,继而引发海啸。福岛第一核电站因海水灌入发生断电,其4个核反应堆中有3个先后发生爆炸和堆芯熔毁,发生爆炸的主要原因是裸露的燃料包壳锆(Zr)和水蒸气在高温条件下生成二氧化锆和氢气,大量氢气和空气混合后被引爆。后期处理中,为了降低核反应堆的温度,须向反应堆内注入大量冷却水。冷却水中含有现有技术无法有效去除的放射性氚(质子数为1,中子
数为2的一种原子),含氚污染水被存储在大型储水罐内。十年过去了,核废水越来越多,到了快装不下的程度,所以,日本政府决定将核废水排入大海,但遭到了国际社会的强烈反对。
材料二:为世界和平与发展贡献更多中国智慧、中国方案、中国力量,化学功不可没!2021年5月15日,天问一号探测器携“祝融号”火星车成功着陆于火星,中国成为第二个成功派出探测器登陆火星的国家。其运载火箭长征五号B采用液氢、液氧作推进剂。
(1)、放射性氚属于(填写元素名称)元素。(2)、海水能够导电,是因为海水中含有氯化钠、氯化镁等物质,写出上述物质中含有的阴离子的符号。(3)、写出锆和水蒸气在高温条件下生成二氧化锆和氢气的化学方程式。(4)、国际社会普遍反对日本向大海排放“核废水”的原因是。(5)、长征五号B采用的燃料是液氢,助燃剂是液氧。液氢燃烧的化学方程式为 , 为使推进剂恰好完全反应,则加注液氢和液氧的质量比为(填最简整数比)。五、填空题
-
17. 磷酸钙[ ]是一种白色晶体或无定形粉末,难溶于水,易溶于稀盐酸和硝酸。磷酸钙的工业用途广泛,在食品工业中可用作抗结剂、营养增补剂、缓冲剂、pH 值调节剂等。(1)、磷酸钙含有的阴离子是(填离子符号),其中磷元素的化合价是价。(2)、磷酸钙易溶于稀盐酸和硝酸,是因为磷酸钙会与盐酸或硝酸反应,生成易溶于水的(填物质类别)和磷酸。磷酸的化学式是。(3)、依据各类物质之间的反应规律,设计两种制备 的方案(要求依据两种不同的反应规律)。完成表:
方案
原料1
原料2
预测反应的方程式
依据的反应规律
①
Na3PO4溶液
两种盐反应生成两种新盐,生成物中有沉淀
②
六、流程题
-
18. 胆矾(CuSO4·5H2O)具有广泛的应用价值。以下是某学习小组用工业废铜焙烧得到的粗CuO(杂质为铁的氧化物及泥沙)为原料与稀硫酸反应制备胆矾的工业流程图,回答下列问题:

【查阅资料】胆矾是蓝色晶体,易溶于水,难溶于乙醇:已知:Fe3+、Fe2+、Cu2+转化为相应的碱时,开始沉淀和沉淀完全时的pH如表:
Fe3+
Fe2+
Cu2+
开始沉淀时的pH
2.7
7.6
5.2
完全沉淀时的pH
3.7
9.6
6.4
(1)、工业废铜焙烧前,为了使反应充分进行,可事先把废铜进行处理。(2)、向粗CuO中加入稍过量的稀硫酸,形成的滤液1中的溶质有FeSO4、、等(任写2种),写出该步骤其中的一个反应方程式。(3)、操作1用到的的铁制仪器是。操作2包含系列操作步骤有蒸发浓缩、、过滤、洗涤、干燥等步骤。(4)、往粗硫酸铜溶液中通入氧气,目的是把溶液中的FeSO4氧化为Fe2(SO4)3 , 再滴加稀氨水,是为了调节pH,分析表中数据,该步骤调节pH的范围为 , 滤渣Ⅱ的成分是。(5)、往滤液2中滴加稀硫酸后的操作2中过滤得到胆矾晶体后应用洗涤晶体。七、综合应用题
-
19. 我国将力争2060年前实现碳中和。CO2的捕捉是减少碳排放的措施之一、(1)、一种利用NaOH溶液捕捉回收CO2的过程如图所示。

①捕捉室中NaOH溶液常喷成雾状,优点是。
②“反应分离”环节发生的复分解反应是(写化学方程式)。
③“反应分离”环节分离物质采用的方法是。
④CO2用途广泛,写出一种用途:。
(2)、CaO固体也可以捕捉回收CO2.研究表明CaC2O4·H2O热分解制得的CaO疏松多孔,具有良好的CO2捕捉性能。取1.46g CaC2O4·H2O进行加热,固体质量随温度变化如下图。
①写出400~600℃范围内分解反应的化学方程式:。(CaC2O4·H2O的相对分子质量:146)
②据图分析,CaO捕捉CO2的反应温度应(填“高于”或“低于”)800℃。
八、科学探究题
-
20. 随着世界人口的增长,人类对农产品需求量增大,增施化肥逐渐成为农作物增产的最有力措施。 NH4HCO3、NH4Cl、K2SO4、KCl都是常见的化肥。(1)、化肥能为农作物补充的营养元素主要有三种,上述化肥含有的两种营养元素是。(2)、有一包用剩的肥料,可能含有上述四种化肥中的一种或几种,为确定其成分,进行了如下实验:
a 取少量肥料样品于研钵中,加入少量熟石灰混合研磨,有刺激性气味
b 取少量肥料样品于烧杯中,加水溶解,得到无色溶液A。
c 取少量溶液A于试管中,滴加AgNO3溶液,有白色沉淀产生
d 取少量溶液A于试管中,滴加BaCl2溶液,无明显现象
e 取少量溶液A于试管中,滴加稀盐酸,无明显现象。
①分析上述实验过程,关于该肥料的成分可以得到的结论是。
②实验a~e中,不必要进行的一项是(填标号)。
③设计实验方案进一步确定该肥料的成分,完成下表。
(已知: )
实验操作
预期现象与结论
若 , 则该肥料的成分是。
若 , 则该肥料的成分是。
-
-
-
-
-
-