2023-2024 学年 浙教版科学八年级上册 1.5 物质的溶解 同步练习
试卷更新日期:2023-07-31 类型:同步测试
一、单选题
-
1. 室温时,对100毫升氯化钠不饱和溶液甲进行如图①②③操作,分析正确的是( )
 A、操作③前后氯化钠的溶解度不变 B、丙溶液的溶质质量分数一定小于丁溶液 C、乙、丁溶液一定饱和,丙溶液一定不饱和 D、甲溶液和乙溶液相比,甲溶液属于浓溶液2. 20℃时硝酸钾溶解实验的部分数据如表。下列分析不正确的是( )
A、操作③前后氯化钠的溶解度不变 B、丙溶液的溶质质量分数一定小于丁溶液 C、乙、丁溶液一定饱和,丙溶液一定不饱和 D、甲溶液和乙溶液相比,甲溶液属于浓溶液2. 20℃时硝酸钾溶解实验的部分数据如表。下列分析不正确的是( )实验序号
水的质量/g
所加硝酸钾质量/g
所得溶液质量/g
①
10
2.5
12.5
②
10
3
13
③
10
3.5
m
④
10
4
13.2
A、表中m的值为13.2 B、20℃时,硝酸钾的溶解度为32克 C、③、④实验所得溶液均为饱和溶液 D、实验④中所得溶液的溶质质量分数大于实验③3. 20℃时,氯化钠的溶解度为36克。则下图中能正确表示该温度下,饱和氯化钠溶液中的溶质和溶剂比例的是( )A、 B、
B、 C、
C、 D、
D、 4. 固体甲、乙、丙在不同温度下的溶解度如表所示,甲、乙、丙从溶液中析出的晶体不含结晶水。下列说法正确的是( )
4. 固体甲、乙、丙在不同温度下的溶解度如表所示,甲、乙、丙从溶液中析出的晶体不含结晶水。下列说法正确的是( )温度/℃
0
20
40
60
80
溶解度/g
甲
0.18
0.16
0.14
0.12
0.09
乙
35.7
36.0
36.6
37.3
38.4
丙
13.3
31.6
63.9
110
169
A、固体甲的溶解度随温度的升高而增大 B、20℃时,丙溶液中溶质和溶剂质量比为31.6: 100 C、分别将等质量的乙、丙饱和溶液由60℃降温到20℃,溶液中溶质质量大小:丙>乙. D、分别将等质量的甲、丙饱和溶液由60℃降温到20℃,溶液中溶剂质量大小:甲>丙5. 向盛有等质量水的甲、乙、丙三个烧杯中分别加入18g、40g、40g某种固体,充分搅拌后静置,现象如图所示。下列说法正确的是( ) A、该固体的溶解度随温度的升高而减小 B、甲、丙烧杯中的溶液一定属于不饱和溶液 C、乙烧杯中溶液的溶质质量分数一定大于甲 D、乙烧杯中溶液的溶质质量分数一定小于丙6. 如图所示,一定温度下,将盛有饱和石灰水的小试管放入盛水的烧杯中,然后向烧杯水中加入某固体物质后,试管中有固体析出,判断加入的某物质可能是( )
A、该固体的溶解度随温度的升高而减小 B、甲、丙烧杯中的溶液一定属于不饱和溶液 C、乙烧杯中溶液的溶质质量分数一定大于甲 D、乙烧杯中溶液的溶质质量分数一定小于丙6. 如图所示,一定温度下,将盛有饱和石灰水的小试管放入盛水的烧杯中,然后向烧杯水中加入某固体物质后,试管中有固体析出,判断加入的某物质可能是( ) A、硝酸铵固体 B、氢氧化钠固体 C、氯化钠固体 D、蔗糖固体7. 小德在做蔗糖的溶解实验时,他发现室温下烧杯中的蔗糖怎么也溶解不了,如图甲所示,于是他加入了一定量的热水后,如图乙所示。则所得溶液与原溶液相比,下列判断一定正确的是( )
A、硝酸铵固体 B、氢氧化钠固体 C、氯化钠固体 D、蔗糖固体7. 小德在做蔗糖的溶解实验时,他发现室温下烧杯中的蔗糖怎么也溶解不了,如图甲所示,于是他加入了一定量的热水后,如图乙所示。则所得溶液与原溶液相比,下列判断一定正确的是( )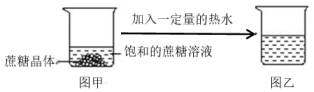 A、所得溶液是饱和溶液 B、溶质的质量增加 C、溶质的质量分数减小 D、溶质的溶解度不变8. 在一定温度下,小明用硝酸钾晶体(KNO3)和溶质质量分数为20%的硝酸钾溶液配制一定质量分数的硝酸钾溶液。如图所示,则如图溶液中,一定是饱和溶液的是( )
A、所得溶液是饱和溶液 B、溶质的质量增加 C、溶质的质量分数减小 D、溶质的溶解度不变8. 在一定温度下,小明用硝酸钾晶体(KNO3)和溶质质量分数为20%的硝酸钾溶液配制一定质量分数的硝酸钾溶液。如图所示,则如图溶液中,一定是饱和溶液的是( ) A、①② B、②③ C、①②③ D、②③④9. 如图所示,给饱和澄清石灰水加热。下列叙述错误的是( )
A、①② B、②③ C、①②③ D、②③④9. 如图所示,给饱和澄清石灰水加热。下列叙述错误的是( ) A、溶液由澄清变浑浊 B、氢氧化钙的溶解度随温度的升高而增大 C、溶液仍为饱和溶液 D、溶液中溶质的质量分数减小10. 生活中的下列现象不能说明气体溶解能力随温度升高而减弱的是( )A、烧开水时,沸腾前有气泡溢出 B、开启啤酒瓶盖, 有大量气泡溢出 C、夏季黄昏时, 池塘里的鱼浮出水面 D、阳光充足时,盛满水的鱼缸壁上有小气泡11. 你见过冬天能自发热,夏天能自制冷的罐装饮料吗,如图1是“玛吉克牌”一摇冰功能饮料,根据所给资料回答:“一摇冰”饮料在炎热的夏天解渴,其罐底的固体是( )
A、溶液由澄清变浑浊 B、氢氧化钙的溶解度随温度的升高而增大 C、溶液仍为饱和溶液 D、溶液中溶质的质量分数减小10. 生活中的下列现象不能说明气体溶解能力随温度升高而减弱的是( )A、烧开水时,沸腾前有气泡溢出 B、开启啤酒瓶盖, 有大量气泡溢出 C、夏季黄昏时, 池塘里的鱼浮出水面 D、阳光充足时,盛满水的鱼缸壁上有小气泡11. 你见过冬天能自发热,夏天能自制冷的罐装饮料吗,如图1是“玛吉克牌”一摇冰功能饮料,根据所给资料回答:“一摇冰”饮料在炎热的夏天解渴,其罐底的固体是( ) A、氢氧化钠 B、硝酸铵 C、氯化钠 D、氢氧化钙12. 在配制食盐溶液的过程中,下列操作既能改变食盐的溶解速度又能改变其溶解性的是( )A、搅拌 B、加水 C、加食盐 D、酒精灯加热13. 有一固体物质(不含结晶水)的溶液甲,在一定温度下经历如下变化,下列说法正确的是( )
A、氢氧化钠 B、硝酸铵 C、氯化钠 D、氢氧化钙12. 在配制食盐溶液的过程中,下列操作既能改变食盐的溶解速度又能改变其溶解性的是( )A、搅拌 B、加水 C、加食盐 D、酒精灯加热13. 有一固体物质(不含结晶水)的溶液甲,在一定温度下经历如下变化,下列说法正确的是( ) A、该温度下,固体物质的溶解度是30g B、溶液乙一定是不饱和溶液 C、溶液丙再蒸发10g水,析出晶体质量一定大于3g D、溶液乙和溶液丙中的溶质质量分数可能相等14. 如图所示,甲、乙试管中分别盛有硝酸钾、氢氧化钙的饱和溶液,试管底部均有未溶解的固体。向烧杯中加入一定质量的氢氧化钠固体后,下列分析正确的是( )
A、该温度下,固体物质的溶解度是30g B、溶液乙一定是不饱和溶液 C、溶液丙再蒸发10g水,析出晶体质量一定大于3g D、溶液乙和溶液丙中的溶质质量分数可能相等14. 如图所示,甲、乙试管中分别盛有硝酸钾、氢氧化钙的饱和溶液,试管底部均有未溶解的固体。向烧杯中加入一定质量的氢氧化钠固体后,下列分析正确的是( ) A、甲试管溶液中的溶质量减少 B、甲试管中未溶解固体的量增加 C、乙试管溶液中的溶质量增加 D、乙试管中未溶解固体的量增加15. 已知硫酸溶液密度大于1,且浓度越大、密度越大。某硫酸的质量分数为W,取等量的两份硫酸溶液分别进行下列操作:
A、甲试管溶液中的溶质量减少 B、甲试管中未溶解固体的量增加 C、乙试管溶液中的溶质量增加 D、乙试管中未溶解固体的量增加15. 已知硫酸溶液密度大于1,且浓度越大、密度越大。某硫酸的质量分数为W,取等量的两份硫酸溶液分别进行下列操作:⑴蒸发溶液后恢复至室温,溶液质量减为原来一半,此时溶液的质量分数为W1
⑵蒸发溶液后恢复至室温,溶液体积减为原来一半,此时溶液的质量分数为W2
则下列关系正确的是( )
A、W1﹥W2 B、W1﹤W2 C、W1=W2 D、W2﹥2W二、填空题
-
16. 如图所示,将同一枚鸡蛋先后放在含食盐量不同的溶液中,出现三种不同的浮沉状态,等鸡蛋静止后,三种液体中鸡蛋受到的浮力FA、FB、Fc的大小关系为;B中液体的溶质质量分数C中液体的溶质质量分数(选填“大于”、“等于”或“小于”)。
 17. 向图甲装有水的小试管中加入一定量的氢氧化钠固体,出现如图乙现象,则此时瓶内气压(选填“大于”、“等于”或“小于”)外界大气压,说明氢氧化钠溶于水(选填“吸热”或“放热”)。
17. 向图甲装有水的小试管中加入一定量的氢氧化钠固体,出现如图乙现象,则此时瓶内气压(选填“大于”、“等于”或“小于”)外界大气压,说明氢氧化钠溶于水(选填“吸热”或“放热”)。 18. 硝酸钾的溶解度随温度升高而增大。如图所示是对硝酸钾溶液的实验操作及变化情况,以及同一小球在三种溶液中的浮沉情况。请回答下列问题:
18. 硝酸钾的溶解度随温度升高而增大。如图所示是对硝酸钾溶液的实验操作及变化情况,以及同一小球在三种溶液中的浮沉情况。请回答下列问题: (1)、操作I可能是 (选填字母)。A、降低温度 B、加入硝酸钾 C、蒸发水分(2)、小球所受的浮力F①、F②、F③的大小关系正确的是 。A、F①<F②=F③ B、F①<F②<F③ C、F①>F②=F③ D、F①=F②=F③(3)、从②到③,烧杯底析出硝酸钾晶体5克,整个装置总质量减少了20克,可知②中的溶质质量分数是。19. 在一定温度下,向100g水中依次加入一定质量的氯化钾固体,充分溶解。加入氯化钾的质量与得到相应溶液质量的关系如图所示:
(1)、操作I可能是 (选填字母)。A、降低温度 B、加入硝酸钾 C、蒸发水分(2)、小球所受的浮力F①、F②、F③的大小关系正确的是 。A、F①<F②=F③ B、F①<F②<F③ C、F①>F②=F③ D、F①=F②=F③(3)、从②到③,烧杯底析出硝酸钾晶体5克,整个装置总质量减少了20克,可知②中的溶质质量分数是。19. 在一定温度下,向100g水中依次加入一定质量的氯化钾固体,充分溶解。加入氯化钾的质量与得到相应溶液质量的关系如图所示: (1)、该温度下氯化钾的溶解度为g。(2)、烧杯①②③中,溶质的质量分数分别为a、b、c,则它们的大小关系是。(用“>”“<”或“=”表示)其中属于饱和溶液的是烧杯(填序号)20. 下表是 A、B、C 三种固体物质在不同温度时的溶解度。
(1)、该温度下氯化钾的溶解度为g。(2)、烧杯①②③中,溶质的质量分数分别为a、b、c,则它们的大小关系是。(用“>”“<”或“=”表示)其中属于饱和溶液的是烧杯(填序号)20. 下表是 A、B、C 三种固体物质在不同温度时的溶解度。温度/℃
0
20
40
60
80
100
溶解度/g
A
13.3
31.6
63.9
110
169
246
B
35.7
36.0
36.6
37.3
38.4
39.8
C
0.18
0.16
0.14
0.11
0.09
0.07
(1)、若 A 中混有少量 B,提纯 A 所采用的方法是。(2)、20℃时,100gB饱和溶液中含 B 物质的质量(填“>”“=”“<”)36.0g。(3)、将 40℃时,A,B,C 三种物质的饱和溶液降温至 20℃,溶液中溶质的质量分数保持不变的是。21. 如图所示, 广口瓶中盛有少量饱和石灰水, 小试管和 U 型管中均有适量水,请回答 (1)、向小试管中放入氢氧化钠固体,可观察到饱和澄清石灰水;(2)、向小试管中加入下列物质,能使U型管中a液面上升,b液面下降的是____ (选填序号)。A、浓硫酸 B、硝酸铵 C、氯化钠 D、生石灰22. 小刚同学在做一定溶质质量分数的氯化钠溶液的配制实验时,其配制过程如图所示.
(1)、向小试管中放入氢氧化钠固体,可观察到饱和澄清石灰水;(2)、向小试管中加入下列物质,能使U型管中a液面上升,b液面下降的是____ (选填序号)。A、浓硫酸 B、硝酸铵 C、氯化钠 D、生石灰22. 小刚同学在做一定溶质质量分数的氯化钠溶液的配制实验时,其配制过程如图所示.试回答下列问题:
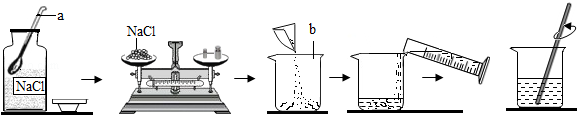 (1)、图示实验中有一处明显的错误是;图示实验中玻璃棒的作用是(2)、小刚同学要配制90g质量分数为10%的氯化钠溶液,应称取氯化钠的质量为g23. “天气瓶”和“彩球温度计”是两款不同的现代居家饰品,都可以获知气温变化。
(1)、图示实验中有一处明显的错误是;图示实验中玻璃棒的作用是(2)、小刚同学要配制90g质量分数为10%的氯化钠溶液,应称取氯化钠的质量为g23. “天气瓶”和“彩球温度计”是两款不同的现代居家饰品,都可以获知气温变化。 (1)、图甲为“天气瓶”,当外界温度降低时,瓶中晶体增多。由此推测瓶中晶体的溶解度随温度降低而。(2)、图乙为“彩球温度计”,当温度降低到小球所标注的温度值时,该小球会浮起。某时,彩球的沉浮情况如乙图所示(“20℃”、“18℃”的小球沉底),则此时的气温范围为。(3)、图乙中漂浮的“24℃”小球重5克,则其所受浮力为牛。24. 甲是60℃的蔗糖溶液,按如图所示进行操作。
(1)、图甲为“天气瓶”,当外界温度降低时,瓶中晶体增多。由此推测瓶中晶体的溶解度随温度降低而。(2)、图乙为“彩球温度计”,当温度降低到小球所标注的温度值时,该小球会浮起。某时,彩球的沉浮情况如乙图所示(“20℃”、“18℃”的小球沉底),则此时的气温范围为。(3)、图乙中漂浮的“24℃”小球重5克,则其所受浮力为牛。24. 甲是60℃的蔗糖溶液,按如图所示进行操作。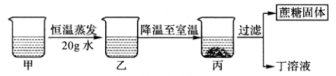 (1)、“甲乙丙丁”四种溶液中,一定属于不饱和溶液的是 。(2)、“甲乙丙丁”四种溶液中,溶质质量分数一定相等的是。25. 图甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题.
(1)、“甲乙丙丁”四种溶液中,一定属于不饱和溶液的是 。(2)、“甲乙丙丁”四种溶液中,溶质质量分数一定相等的是。25. 图甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题. (1)、t1℃时,甲、乙、丙的溶解度由大到小的顺序是。(2)、P点的含义 。(3)、t3℃时,在150g水中加入100g甲,形成溶液的质量为 g。(4)、t2℃时,甲、乙、丙三种物质的饱和溶液升温至t3℃后,三种溶液的溶质质量分数由大到小的顺序是。
(1)、t1℃时,甲、乙、丙的溶解度由大到小的顺序是。(2)、P点的含义 。(3)、t3℃时,在150g水中加入100g甲,形成溶液的质量为 g。(4)、t2℃时,甲、乙、丙三种物质的饱和溶液升温至t3℃后,三种溶液的溶质质量分数由大到小的顺序是。三、实验探究题
-
26. 小科欲配制80克5%的氯化钠溶液,该实验的部分操作如图所示。
 (1)、需要称取氯化钠的质量 克。称量时出现了右盘略低的现象,如图甲,接下来的具体操作是 。(2)、量取水时,选用规格为 (选填“100”或“200”)毫升的量筒更加合理。(3)、丙中玻璃棒的作用是 。(4)、下列操作会导致配制的氯化钠溶液质量分数偏小的有 ____。A、砝码磨损 B、氯化钠固体不纯 C、按照图乙的方法读数 D、将量筒中的水倒入烧杯时,有水洒出27. 某化学兴趣小组探究氯化铵、氯化钙、氯化钠三种物质溶于水过程中的热量变化。
(1)、需要称取氯化钠的质量 克。称量时出现了右盘略低的现象,如图甲,接下来的具体操作是 。(2)、量取水时,选用规格为 (选填“100”或“200”)毫升的量筒更加合理。(3)、丙中玻璃棒的作用是 。(4)、下列操作会导致配制的氯化钠溶液质量分数偏小的有 ____。A、砝码磨损 B、氯化钠固体不纯 C、按照图乙的方法读数 D、将量筒中的水倒入烧杯时,有水洒出27. 某化学兴趣小组探究氯化铵、氯化钙、氯化钠三种物质溶于水过程中的热量变化。【药品器材】水、氯化铵、氯化钙、氯化钠;烧杯、药匙、玻璃棒、量筒、温度计等。
【实验探究】三种物质各取1药匙于烧杯分别溶于水,另还有一个烧杯只加水,用温度计测量液体温度,并记录有关数据如下:
实验
水的体积
所加物质
测量液体温度(℃)
实验1
50mL
氯化铵
15
实验2
50mL
氯化钙
28
实验3
X
氯化钠
21
实验4
50mL
无
22
(1)、表中X为mL。(2)、比较实验2与实验4,可获得的结论是。(3)、如果要生产一种“冰袋”用于冷敷,上述三种物质中最合适的是。(4)、经讨论认为本实验操作中存在缺陷,它是 (填选项,可多选)。A、实验操作过程没有采取较为严格的保温措施 B、加入物质的质量可能不相等 C、加入物质的种类不一样。28. 如图是配制50g质量分数为10%的氯化钠溶液的操作过程示意图。试回答: (1)、要配制 1 000 毫升这种氯化钠溶液( 密度为1克/厘米 3),需氯化钠克;(2)、按B图所示称量时,配制的氯化钠溶液中溶质的质量分数10%(填“等于、大于或小于”);(3)、如图是某学生用氯化钠固体和水配制氯化钠溶液的部分操作过程,该同学在称量氯化钠时,先在两个托盘上各放一张质量相同的纸,然后把药品直接放在纸上称量。
(1)、要配制 1 000 毫升这种氯化钠溶液( 密度为1克/厘米 3),需氯化钠克;(2)、按B图所示称量时,配制的氯化钠溶液中溶质的质量分数10%(填“等于、大于或小于”);(3)、如图是某学生用氯化钠固体和水配制氯化钠溶液的部分操作过程,该同学在称量氯化钠时,先在两个托盘上各放一张质量相同的纸,然后把药品直接放在纸上称量。下列操作中导致溶质质量分数偏高的是 。
A、操作中砝码和氯化钠放错盘 B、c 中烧杯用水洗涤后未干燥就使用 C、d 操作中平视量筒凹液面最低处读数 D、e 操作中有少量水溅出。29. 图1是配制溶质质量分数为10%的食盐溶液的实验操作示意图: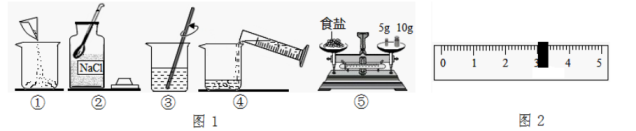 (1)、用图1的序号表示配制溶液的正确操作顺序:。(2)、称量食盐时,天平平衡后的状态如图1⑤所示,游码标尺示数见图2,则需要量取水的
(1)、用图1的序号表示配制溶液的正确操作顺序:。(2)、称量食盐时,天平平衡后的状态如图1⑤所示,游码标尺示数见图2,则需要量取水的体积是 mL。
(3)、经检测,配制出来的食盐溶液溶质质量分数偏大,其原因可能是(填序号)。①氯化钠固体有杂质②称量时左盘垫纸片,右盘未垫纸片③量取水时,俯视读数
30. 某同学配制 50g 6%氯化钠溶液, 整个操作过程如图所示, 回答下列问题:
 (1)、配制溶液的正确操作顺序为②①(填序号,下同),其中操作错误的是。(2)、纠正错误操作后,用托盘天平称量所需的氯化钠,若发现托盘天平的指针偏向左盘, 则 接下来应该进行的操作是 (填字母) 。A、适量增加砝码 B、适量减少适量氯化钠固体 C、 向右调节平衡螺母(3)、在配制溶液的过程中,若该同学量取水时俯视读数,则配制的溶液溶质质量分数将偏。(4)、将配制好的溶液装入 中 (选填“广口瓶”或“细口瓶”) ,盖好瓶塞并贴标签。
(1)、配制溶液的正确操作顺序为②①(填序号,下同),其中操作错误的是。(2)、纠正错误操作后,用托盘天平称量所需的氯化钠,若发现托盘天平的指针偏向左盘, 则 接下来应该进行的操作是 (填字母) 。A、适量增加砝码 B、适量减少适量氯化钠固体 C、 向右调节平衡螺母(3)、在配制溶液的过程中,若该同学量取水时俯视读数,则配制的溶液溶质质量分数将偏。(4)、将配制好的溶液装入 中 (选填“广口瓶”或“细口瓶”) ,盖好瓶塞并贴标签。四、解答题
-
31. “过氧乙酸”消毒液广泛用于教室、食堂、寝室等场所的卫生消毒。某品牌“过氧乙酸”消毒液标签如下表所示。
过氧乙酸(1L)
溶质质量分数
20%
密度
1.2 g/cm3
强腐蚀性、阴冷处存放
(1)、取该消毒液1L,其中含过氧乙酸克。(2)、取12g该溶液配制成溶质质量分数为0.5%的过氧乙酸溶液用来消毒,请计算需要加入水的质量?32. 如图甲是天宫课堂中航天员王亚平给我们演示的“冰雪”实验,通过航天员的小科同学知道了这里所用的溶液是过饱和的乙酸钠溶液。一定温度、压力下,当溶液中溶质的质量已超过该温度、压力下该溶质的溶解度,而溶质仍不析出的现象叫过饱和现象。在这种溶液中只要有点结晶核颗粒或振动,就能迅速打破原本的过饱和状态,析出大量的晶体,同时还会释放出大量的热量。根据题中信息,回答下列问题: (1)、液体结晶后外观看起来像“冰雪球”,实为“热球”,原因是:。(2)、市面上有一种掰热暖宝宝(里面装有过饱和的乙酸钠溶液)如图乙所示,只需要用力掰动袋中金属片,袋中溶液就会结晶放热,掰动金属片的目的是 。(3)、下表是乙酸钠的溶解度,小科先在100摄氏度水中配制其饱和溶液,一定条件下,降温到40摄氏度,此时并没有晶体析出,求此时溶液中溶质的质量分数。(结果保留一位小数)
(1)、液体结晶后外观看起来像“冰雪球”,实为“热球”,原因是:。(2)、市面上有一种掰热暖宝宝(里面装有过饱和的乙酸钠溶液)如图乙所示,只需要用力掰动袋中金属片,袋中溶液就会结晶放热,掰动金属片的目的是 。(3)、下表是乙酸钠的溶解度,小科先在100摄氏度水中配制其饱和溶液,一定条件下,降温到40摄氏度,此时并没有晶体析出,求此时溶液中溶质的质量分数。(结果保留一位小数)温度/℃
0
20
40
60
80
100
溶解度/克
33
46.5
65.5
139
153
170
33. 氯化钠俗名食盐,是工业生产和生活的一种重要原料,也是实验室里常见的一种药品。下表是20℃时,氯化钠溶解于水的实验数据,请分析回答:实验序号
水的质量/g
加入氯化钠的质量/g
溶液的质量/g
①
20
4
24
②
20
6
26
③
20
8
27.2
④
20
10
m
(1)、表中m=。(2)、由表中数据可知,20℃时氯化钠的溶解度为。(3)、将100克溶质质量分数为20%的氯化钠溶液稀释成5%的氯化钠溶液,需加入水多少毫升?34. 小德在生物实验室观察到很多生物标本浸泡在某种液体中,后来得知该液体为福尔马林。他上网查阅资料发现福尔马林是浓度为35%—40%的甲醛溶液。(1)、实验室中,要配制100克质量分数为40%的福尔马林溶液,需要甲醛的质量为多少?(2)、如果将该溶液稀释为35%的溶液,需要加入多少毫升的水?(结果保留一位小数)五、综合说理题
-
35. 如图所示, 室温下的饱和食盐水中放了一个塑料小球。(ρ球<ρ水)
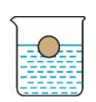 (1)、现加入少量食盐晶体,充分搅拌和静置后, 在温度不变的情况下,小球在液面沉浮情况有何变化?(2)、若在原饱和食盐水中加入少量的水,溶液温度保持不变,小球在液面沉浮情况有何变化?(3)、若要在不用外力的情况下使小球略上浮,你准备采取的具体方法是什么?(4)、若保持原溶液温度不变,蒸发溶剂,小球在液面沉浮情况有何变化?
(1)、现加入少量食盐晶体,充分搅拌和静置后, 在温度不变的情况下,小球在液面沉浮情况有何变化?(2)、若在原饱和食盐水中加入少量的水,溶液温度保持不变,小球在液面沉浮情况有何变化?(3)、若要在不用外力的情况下使小球略上浮,你准备采取的具体方法是什么?(4)、若保持原溶液温度不变,蒸发溶剂,小球在液面沉浮情况有何变化?