高考二轮复习知识点:化学反应中能量的转化4
试卷更新日期:2023-07-30 类型:二轮复习
一、选择题
-
1.
下列图示与对应的叙述不相符合的是( )
 A、图甲表示燃料燃烧反应的能量变化 B、图乙表示酶催化反应的反应速率随反应温度的变化 C、图丙表示弱电解质在水中建立电离平衡的过程 D、图丁表示强碱滴定强酸的滴定曲线2. 理论研究表明,在101kPa和298K下, 异构化反应过程的能量变化如图所示。下列说法错误的是( )
A、图甲表示燃料燃烧反应的能量变化 B、图乙表示酶催化反应的反应速率随反应温度的变化 C、图丙表示弱电解质在水中建立电离平衡的过程 D、图丁表示强碱滴定强酸的滴定曲线2. 理论研究表明,在101kPa和298K下, 异构化反应过程的能量变化如图所示。下列说法错误的是( ) A、HCN比HNC稳定 B、该异构化反应的 C、正反应的活化能大于逆反应的活化能 D、使用催化剂,可以改变反应的反应热3. 某反应由两步反应构成,其反应能量变化曲线如图所示,下列叙述正确的是( )
A、HCN比HNC稳定 B、该异构化反应的 C、正反应的活化能大于逆反应的活化能 D、使用催化剂,可以改变反应的反应热3. 某反应由两步反应构成,其反应能量变化曲线如图所示,下列叙述正确的是( ) A、两步反应均为吸热反应 B、的反应一定需要加热 C、A与C的能量差为 , 发生反应时,会向环境释放能量 D、三种物质中C最不稳定4. 科学家利用过渡金属氮化物(TMNS)在常温下催化实现氨的合成,其反应机理如图所示。下列说法正确的是( )
A、两步反应均为吸热反应 B、的反应一定需要加热 C、A与C的能量差为 , 发生反应时,会向环境释放能量 D、三种物质中C最不稳定4. 科学家利用过渡金属氮化物(TMNS)在常温下催化实现氨的合成,其反应机理如图所示。下列说法正确的是( ) A、TMNS大大降低了合成氨反应的活化能,提高了合成氨的转化率 B、TMNS表面N2分子被氧化为氨分子 C、TMNS表面上氨脱附产生的空位有利于吸附N2 D、高温有利于提高TMNS催化氨的合成效率5. 我国科研人员提出了由小分子X、Y转化为高附加值产品M的催化反应历程。该历程可用示意图表示如下,下列说法正确的是( )
A、TMNS大大降低了合成氨反应的活化能,提高了合成氨的转化率 B、TMNS表面N2分子被氧化为氨分子 C、TMNS表面上氨脱附产生的空位有利于吸附N2 D、高温有利于提高TMNS催化氨的合成效率5. 我国科研人员提出了由小分子X、Y转化为高附加值产品M的催化反应历程。该历程可用示意图表示如下,下列说法正确的是( ) A、由X、Y生成M的总反应原子利用率为100% B、①→②过程属于吸热反应 C、X、Y、M分别为甲烷、二氧化碳和乙醇 D、反应过程中有C-H键、C-C键、O-H键生成6. 将溶质物质的量相同的酸溶液与碱溶液相混合,a:盐酸和氢氧化钠,b:醋酸和氢氧化钠,c:醋酸和氨水。其所放出热量比较,正确的是( )A、a>b>c B、c>b>a C、b>c>a D、a=b=c7. 由X、Y转化为M的反应历程如图所示,下列说法错误的是( )
A、由X、Y生成M的总反应原子利用率为100% B、①→②过程属于吸热反应 C、X、Y、M分别为甲烷、二氧化碳和乙醇 D、反应过程中有C-H键、C-C键、O-H键生成6. 将溶质物质的量相同的酸溶液与碱溶液相混合,a:盐酸和氢氧化钠,b:醋酸和氢氧化钠,c:醋酸和氨水。其所放出热量比较,正确的是( )A、a>b>c B、c>b>a C、b>c>a D、a=b=c7. 由X、Y转化为M的反应历程如图所示,下列说法错误的是( ) A、①→②的总过程放热 B、M是CH3COOH C、反应过程中形成C-H键 D、反应X+Y→M的原子利用率为100%8. Cu-Ce-Ox固溶体作为金属催化剂,能有效促进电化学还原,反应产生CH4和C2H4的共同中间体,•CO在催化剂表面的反应机理如图所示。下列说法错误的是( )
A、①→②的总过程放热 B、M是CH3COOH C、反应过程中形成C-H键 D、反应X+Y→M的原子利用率为100%8. Cu-Ce-Ox固溶体作为金属催化剂,能有效促进电化学还原,反应产生CH4和C2H4的共同中间体,•CO在催化剂表面的反应机理如图所示。下列说法错误的是( )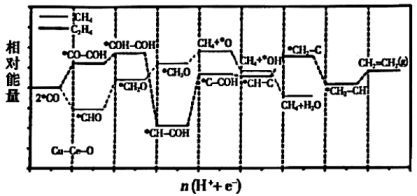 A、Cu-Ce-Ox固溶体催化剂对生成CH4有较高选择性 B、制约CO2还原为C2H4反应速率的是•CH-COH→•C-COH C、由•CO生成•OH的反应为•CO+5H++5e-=CH4+•OH D、•CH3O→CH4+•O只有化学键的形成9. 在25℃、下,氢气燃烧生成气态水的能量变化如下图所示,已知:2H2(g) + O2(g)→2H2O(g) , 下列有关说法正确的是( )
A、Cu-Ce-Ox固溶体催化剂对生成CH4有较高选择性 B、制约CO2还原为C2H4反应速率的是•CH-COH→•C-COH C、由•CO生成•OH的反应为•CO+5H++5e-=CH4+•OH D、•CH3O→CH4+•O只有化学键的形成9. 在25℃、下,氢气燃烧生成气态水的能量变化如下图所示,已知:2H2(g) + O2(g)→2H2O(g) , 下列有关说法正确的是( ) A、O-H键的键能为930kJ·mol-1 B、a= 249 C、物质所具有的总能量大小关系为:甲>乙>丙 D、1molH2O(l)分解为2molH与1molO时吸收930kJ热量10. 最近科学家采用真空封管法制备的磷化硼纳米颗粒,作与合成[]反应的催化剂,在发展非金属催化剂实现电催化还原制备甲醇方向取得重要进展,该反应历程如图所示(部分物质未画出)。
A、O-H键的键能为930kJ·mol-1 B、a= 249 C、物质所具有的总能量大小关系为:甲>乙>丙 D、1molH2O(l)分解为2molH与1molO时吸收930kJ热量10. 最近科学家采用真空封管法制备的磷化硼纳米颗粒,作与合成[]反应的催化剂,在发展非金属催化剂实现电催化还原制备甲醇方向取得重要进展,该反应历程如图所示(部分物质未画出)。
下列说法正确的是( )
A、与生成和的反应为放热反应 B、上述反应生成的副产物中,比多(相同条件下) C、在合成甲醇的过程中,降低能量变化,可提高反应速率 D、反应过程中有极性键和非极性键的断裂和生成11. 研究表明I-可以作为水溶液中SO2歧化反应的催化剂,3SO2(g)+2H2O(l)→2H2SO4(aq)+S(s),该过程一般通过如下步骤来实现:①SO2(g)+4I-(aq)+4H+(aq)→S(s)+2I2(g)+2H2O(l)+Q1(Q1<0)
②I2(g)+2H2O(l)+SO2(g)→SO(aq)+4H+(aq)+2I-(aq)+Q2(Q2>0)
上述反应过程中能量变化不可能是下列示意图中的( )
A、 B、
B、 C、
C、 D、
D、 12. 近日,我国科研团队设计了一种表面锂掺杂的锡纳米粒子催化剂s-SnLi可提高电催化制甲酸盐的产率,同时释放电能,实验原理如图所示。下列说法错误的是( )
12. 近日,我国科研团队设计了一种表面锂掺杂的锡纳米粒子催化剂s-SnLi可提高电催化制甲酸盐的产率,同时释放电能,实验原理如图所示。下列说法错误的是( ) A、使用催化剂能有效减少副产物CO的生成;使用s-SnLi催化剂,中间产物更不稳定 B、充电时,阳极电极周围pH降低 C、放电时,每生成1 mol HCOO- , 转移1 mol电子 D、放电时,负极电极反应式为Zn+4OH--2e-=13. 单原子催化剂具有良好的电催化性能,催化转化 的历程如下。
A、使用催化剂能有效减少副产物CO的生成;使用s-SnLi催化剂,中间产物更不稳定 B、充电时,阳极电极周围pH降低 C、放电时,每生成1 mol HCOO- , 转移1 mol电子 D、放电时,负极电极反应式为Zn+4OH--2e-=13. 单原子催化剂具有良好的电催化性能,催化转化 的历程如下。
下列说法错误的是( )
A、 催化转化的产物是 和 B、过程②→③涉及化学键的断裂与生成 C、反应过程中,C的杂化方式未发生改变 D、生成 ,需要 电子14. 氢气是一种清洁能源,下图是 和 反应生成 的能量变化示意图,由图可知( ) A、 B、生成 需要吸收 的能量 C、 和 具有的总能量比 所具有的总能量高 D、 ,断键吸收的能量小于成键释放的能量15. 以Pd纳米粒子为核、空心多孔碳球为壳的封装型催化剂将H2和O2直接合成 的机理如图(a)所示。电催化还原O2时的两种可能转化路径如图(b)所示(其中吸附在催化剂表面的物种用*标注)。下列说法错误的是( )
A、 B、生成 需要吸收 的能量 C、 和 具有的总能量比 所具有的总能量高 D、 ,断键吸收的能量小于成键释放的能量15. 以Pd纳米粒子为核、空心多孔碳球为壳的封装型催化剂将H2和O2直接合成 的机理如图(a)所示。电催化还原O2时的两种可能转化路径如图(b)所示(其中吸附在催化剂表面的物种用*标注)。下列说法错误的是( ) A、直接合成法中,步骤②吸收能量,步骤④释放能量 B、电催化还原法制备H2O2的优点之一是避免了H2和O2共存的易爆环境 C、电催化还原时,2e-路径的步骤少,反应速率快 D、若催化剂表面对*OOH吸附过强,则易生成O* , 导致 的产率降低16. 下图是计算机模拟的在催化剂表面上水煤气变化的反应历程。吸附在催化剂表面的物种用“*”标注。
A、直接合成法中,步骤②吸收能量,步骤④释放能量 B、电催化还原法制备H2O2的优点之一是避免了H2和O2共存的易爆环境 C、电催化还原时,2e-路径的步骤少,反应速率快 D、若催化剂表面对*OOH吸附过强,则易生成O* , 导致 的产率降低16. 下图是计算机模拟的在催化剂表面上水煤气变化的反应历程。吸附在催化剂表面的物种用“*”标注。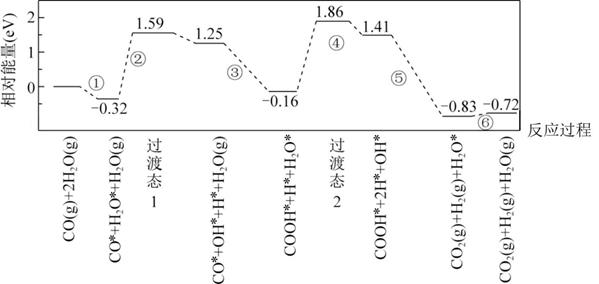
下列说法正确的是( )
A、①表示CO和H2O从催化剂表面脱离的过程 B、②和④中化学键变化相同,因此吸收的能量相同 C、由图可知CO(g)+H2O(g)=CO2(g)+H2(g)为吸热反应 D、本历程中的催化剂通过改变水煤气变化反应的焓变,来实现改变其反应速率17. CO与N2O在铁催化剂表面进行如下两步反应:第一步:Fe*+N2O=FeO*+N2
第二步:FeO*+CO=Fe*+CO2
其相对能量与反应历程如下图所示,下列说法错误的是( )
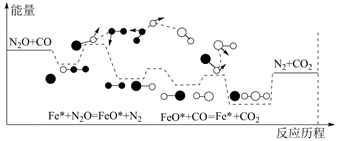 A、总反应是放热反应,化学方程式为CO+N2O CO2+N2 B、在反应过程中,有极性键和非极性键的断裂和生成 C、总反应的反应速率由第一步反应决定 D、Fe*为反应的催化剂,FeO*为中间产物
A、总反应是放热反应,化学方程式为CO+N2O CO2+N2 B、在反应过程中,有极性键和非极性键的断裂和生成 C、总反应的反应速率由第一步反应决定 D、Fe*为反应的催化剂,FeO*为中间产物二、多选题
-
18. 1,3-丁二烯与HBr发生加成反应分两步:第一步H+进攻1,3-丁二烯生成碳正离子(
 );第二步Br -进攻碳正离子完成1,2-加成或1,4-加成。反应进程中的能量变化如下图所示。已知在0℃和40℃时,1,2-加成产物与1,4-加成产物的比例分别为70:30和15:85。下列说法正确的是( )
);第二步Br -进攻碳正离子完成1,2-加成或1,4-加成。反应进程中的能量变化如下图所示。已知在0℃和40℃时,1,2-加成产物与1,4-加成产物的比例分别为70:30和15:85。下列说法正确的是( )  A、1,4-加成产物比1,2-加成产物稳定 B、与0℃相比,40℃时1,3-丁二烯的转化率增大 C、从0℃升至40℃,1,2-加成正反应速率增大,1,4-加成正反应速率减小 D、从0℃升至40℃,1,2-加成正反应速率的增大程度小于其逆反应速率的增大程度19. 下列判断正确的是( )
A、1,4-加成产物比1,2-加成产物稳定 B、与0℃相比,40℃时1,3-丁二烯的转化率增大 C、从0℃升至40℃,1,2-加成正反应速率增大,1,4-加成正反应速率减小 D、从0℃升至40℃,1,2-加成正反应速率的增大程度小于其逆反应速率的增大程度19. 下列判断正确的是( ) A、图1可表示电解200 mL 0.1 mol·L-1 NaCl溶液过程中,产生氢气体积(标准状况)与转移电子物质的量的关系曲线 B、图2可表示常温下0.1 mol·L-1盐酸滴加到40 mL 0.1 mol·L-1 NaOH溶液的滴定曲线 C、高温下能自发进行的反应CO2(g)+H2(g) CO(g)+H2O(g)的能量变化如图3所示,则该反应的ΔS>0 D、图4可表示反应N2(g)+3H2(g) 2NH3(g)在t1时刻扩大容器体积时,v逆随时间的变化曲线20. 初始温度为t ℃,向三个密闭的容器中按不同方式投入反应物,发生反应:4HCl(g)+O2(g) 2Cl2(g)+2H2O(g);ΔH=-116 kJ·mol-1 , 测得反应的相关数据如下:
A、图1可表示电解200 mL 0.1 mol·L-1 NaCl溶液过程中,产生氢气体积(标准状况)与转移电子物质的量的关系曲线 B、图2可表示常温下0.1 mol·L-1盐酸滴加到40 mL 0.1 mol·L-1 NaOH溶液的滴定曲线 C、高温下能自发进行的反应CO2(g)+H2(g) CO(g)+H2O(g)的能量变化如图3所示,则该反应的ΔS>0 D、图4可表示反应N2(g)+3H2(g) 2NH3(g)在t1时刻扩大容器体积时,v逆随时间的变化曲线20. 初始温度为t ℃,向三个密闭的容器中按不同方式投入反应物,发生反应:4HCl(g)+O2(g) 2Cl2(g)+2H2O(g);ΔH=-116 kJ·mol-1 , 测得反应的相关数据如下:容
器
容器类型
初始
体积
初始压
强/Pa
反应物投入量/mol
平衡时Cl2的
物质的量/mol
HCl
O2
Cl2
H2O
Ⅰ
恒温恒容
1 L
2×105
4
1
0
0
1
Ⅱ
绝热恒容
1 L
p2
0
0
2
2
a
Ⅲ
恒温恒压
2 L
p3
8
2
0
0
b
下列说法正确的是( )
A、反应4HCl(g)+O2(g)⇌2Cl2(g)+2H2O(l)的ΔH>-116 kJ·mol-1 B、a>1, b>2 C、p2=1.6×105 Pa, p3=4×105 Pa D、若起始向容器Ⅰ中充入0.5 mol HCl、0.5 mol O2、0.5 mol Cl2和0.5 mol H2O,则反应向逆反应方向进行21. 利用含碳化合物合成燃料是解决能源危机的重要方法,已知煤液化过程中有反应 CO(g)+2H2(g) =CH3OH(g),其反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是( )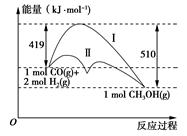 A、该反应的反应热ΔH=+91 kJ·mol-1 B、加入催化剂后,该反应的ΔH变小 C、反应物的总能量大于生成物的总能量 D、从图中可以看出,使用催化剂降低了该反应的活化能22. 下列说法正确的是( )A、化学键的断裂和形成是化学反应能量变化的主要原因 B、伴有能量变化的物质变化都是化学变化 C、在一个确定的化学反应中,反应物的总能量与生成物的总能量一定不同 D、在一个确定的化学反应中,反应物的总能量总是高于生成物的总能量23. 利用新型催化剂在太阳光的作用下将进行分解,反应过程如图所示。下列有关说法正确的是( )
A、该反应的反应热ΔH=+91 kJ·mol-1 B、加入催化剂后,该反应的ΔH变小 C、反应物的总能量大于生成物的总能量 D、从图中可以看出,使用催化剂降低了该反应的活化能22. 下列说法正确的是( )A、化学键的断裂和形成是化学反应能量变化的主要原因 B、伴有能量变化的物质变化都是化学变化 C、在一个确定的化学反应中,反应物的总能量与生成物的总能量一定不同 D、在一个确定的化学反应中,反应物的总能量总是高于生成物的总能量23. 利用新型催化剂在太阳光的作用下将进行分解,反应过程如图所示。下列有关说法正确的是( ) A、反应Ⅰ中形成了两种新的化学键 B、中间产物
A、反应Ⅰ中形成了两种新的化学键 B、中间产物 的电子式:
的电子式: C、总反应中1mol氮气和3mol氢气的总键能大于2mol氨气的总键能
D、通过该催化反应,实现了太阳能向化学能的转化
24. N2与O2生成NO是自然界固氮的重要方式之一,下图显示了该反应中的能量变化。
C、总反应中1mol氮气和3mol氢气的总键能大于2mol氨气的总键能
D、通过该催化反应,实现了太阳能向化学能的转化
24. N2与O2生成NO是自然界固氮的重要方式之一,下图显示了该反应中的能量变化。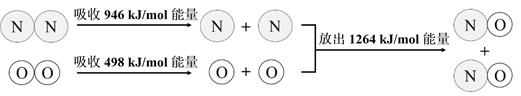
下列说法正确的是( )
A、N≡N键的键能大于O=O键的键能 B、完全断开1mol NO中的化学键需吸收1264kJ能量 C、该反应中产物所具有的总能量高于反应物所具有的总能量 D、生成1mol NO气体反应吸收180kJ能量25. 常温下,1mol化学键形成(或断裂)的能量变化用E表示。下列说法正确的是化学键
H—H
Cl—Cl
H—Cl
436
243
431
A、H(g)和Cl(g)形成HCl(g)的过程要放出能量 B、 C、该反应过程中,断开化学键吸收的总能量大于形成化学键释放的总能量 D、和的总能量高于2mol HCl(g)的总能量三、非选择题
-
26. 对烟道气中的 进行回收再利用具有较高的社会价值。(1)、大气中 含量过高会导致雨水中含有(填化学式)而危害植物和建筑物。工厂排放的 尾气用饱和 溶液吸收可得到重要化工原料 ,反应的化学方程式为。由 过饱和溶液结晶脱水可制得 。写出该过程的化学方程式。(2)、 可用作食品的抗氧化剂。在滴定某葡萄酒中 残留量时,取 葡萄酒样品,用 的碘标准液滴定至终点,消耗 碘液。补全该滴定反应的离子方程式: ,;该样品中 的残留量为 (以 计)。(3)、一定条件下,由SO2和CO反应生成S和CO2的能量变化如图所示,每生成16gS(s),该反应(选填“放出”或“吸收”)的热量为。
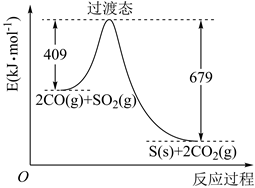 (4)、在绝对隔热恒容的密闭容器中,进行该反应的平衡常数表达式为 , 对此反应下列说法正确的是。
(4)、在绝对隔热恒容的密闭容器中,进行该反应的平衡常数表达式为 , 对此反应下列说法正确的是。a.若混合气体密度保持不变,则已达到平衡状态
b.从反应开始到平衡,容器内气体的压强保持不变
c.达平衡后若再充入一定量CO2 , 平衡常数保持不变
d.分离出少量S粉,正、逆反应速率均保持不变
27. 采用光电催化法或化学吸收法处理含硫化氢的废液废气,既可防止环境污染又可回收硫资源等。回答下列问题:(1)、利用二氧化锰修饰的活性炭(MnO2-AC)作光催化剂分解废水中H2S制氢气的原理如下图所示。在催化作用下,MnO2-AC自动将电子集中至导带,空穴(用h*表示)集中至价带,从而进一步分解H2S。图中能量转化形式是 , 已 知在催化剂表面总反应为:2HS-=H2↑+S ,价带上发生的半反应为 (半反应相当于电极反应)。 (2)、利用CaCO3吸收烟气中H2S包括:CaCO3的分解、H2S的吸收与CaS的生成以及CaS的氧化。
(2)、利用CaCO3吸收烟气中H2S包括:CaCO3的分解、H2S的吸收与CaS的生成以及CaS的氧化。①高温下反应CaCO3(s)=CaO(s)+CO2(g)能自发进行, 则△H0,∆S0(填“大于”或“小于”)。
②恒温恒容密闭容器中进行吸收H2S反应为CaO(s)+H2S(g) CaS(s)+H2O(g),能说明该反应已达到平衡状态的是 (填标号)。
A.气体的总压强不再随时间变化
B.气体的密度不再随时间变化
C.单位时间内断裂H-S与生成H-O键数相等
D.气体的分压p(H2S)/p(H2O)不再随时间变化
③CaS的氧化涉及如下反应:
(I) CaS(s)+O2(g) CaSO4(s) ∆H1
(II) CaS(s)+O2(g) CaO(s)+ SO2(g) △H2
(III )CaSO4(s)+ CaS(s) CaO(s)+ SO2(g) ∆H3
在恒压(总压为akPa)密闭容器中反应时,各反应的lgKp(Kp为以分压表示的平衡常数)与温度的关系如图:

由图可知: ∆H>0的反应是 ( 填标号);∆H3=(用∆H1、∆H2表示);N点时,分压p(SO2)=kPa,M点时,分压p(O2)=kPa
28. 氮及其化合物的研究对于生态环境保护和工农业生产发展非常重要。请回答下列问题:(1)、煤燃烧产生的烟气中含有氮的氧化物NOx , 用CH4催化还原NOx可消除氮氧化物的污染。已知:①CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-865.0 kJ·mol-1
②2NO(g)+O2(g)=2NO2(g) △H=-112.5 kJ·mol-1
③适量的N2和O2完全反应,每生成2.24 L(标准状况下)NO时,吸收8.9 kJ的热量。
则CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=kJ·mol-1。
(2)、已知合成氨反应N2(g)+3H2(g) 2NH3(g) △H=-92 kJ·mol-1①合成氨需要选择合适的催化剂,分别选用A、B、C三种催化剂进行实验,所得结果如图1所示(其他条件相同),则实际生产中适宜选择的催化剂是(填“A”、“B”或“C”),理由是。
 ②科研小组模拟不同条件下的合成氨反应,向刚性容器中充人10.0 mol N2和20.0 mol H2 , 不同温度下平衡混合物中氨气的体积分数与总压强(p)的关系如图2,T1、T2、T3由小到大的排序为;在T2、50MPa条件下,A点v正v逆(填“>”、“<”或“=”);在温度T2压强50 MPa时,平衡常数Kp=MPa-2(列出表达式,分压=总压×物质的量分数)。
②科研小组模拟不同条件下的合成氨反应,向刚性容器中充人10.0 mol N2和20.0 mol H2 , 不同温度下平衡混合物中氨气的体积分数与总压强(p)的关系如图2,T1、T2、T3由小到大的排序为;在T2、50MPa条件下,A点v正v逆(填“>”、“<”或“=”);在温度T2压强50 MPa时,平衡常数Kp=MPa-2(列出表达式,分压=总压×物质的量分数)。③合成氨反应在催化剂作用下的反应历程为(*表示吸附态):
第一步N2(g)→2N*;H2(g)→2H*(慢反应)
第二步N*+H* NH*;NH*+H* NH2*;NH2*+H* NH3*;(快反应)
第三步NH3* NH3(g)(快反应)
i.第一步反应的活化能E1与第二步反应的活化能E2相比:E1>E2 , 请写出判断理由。
ii.关于合成氨工艺的下列理解,正确的有(填写字母编号)。
A.控制温度远高于室温,是为了保证尽可能高的平衡转化率和加快的反应速率
B.合成氨反应在不同温度下的△H和△S都小于零
C.NH3易液化,不断将液氨移去,利于反应正向进行
D.原料气中N2由分离空气得到,H2由天然气与水蒸气反应生成,原料气需要经过净化处理,以防催化剂中毒和安全事故发生
29. 一定条件下 能氧化 制 ,这对资源综合利用有重要意义。相关的化学反应如下:I.
II.
(1)、已知反应的能量变化如图1所示。
①当生成等物质的量的 时,反应(填“I”或“II”)吸收的热量更多。
② 生成 的热化学方程式为。
(2)、反应II不利于乙烯的生成的原因是。(3)、有研究表明,在催化剂作用下,反应I分两步进行,其反应过程及能量变化如图2所示。①决定反应I的反应速率的步骤是(填“第一步”或“第二步”),原因是。
②第一步的化学方程式为。
(4)、在恒容密闭的容器中充入一定量的 和 ,保持其他条件不变,控制反应温度分别为 和 ,测得 随时间 的变化曲线如图3所示,则 (填“大于”或“小于”) ,原因是。(5)、温度为T时,向一密闭容器中通入 和 ,一段时间后,反应Ⅰ和反应Ⅱ均达到平衡, 的转化率为50%, 的选择性为60%,此时容器容积为 ,则该温度下反应I的平衡常数 。30. 甲醇是有机化工中重要的合成原料,在催化剂的作用下利用甲醇合成乙烯和丙烯的技术被称为 技术。该技术涉及的主要反应为:i.
ii.
请回答下列问题:
(1)、反应 的反应热 kJ/mol;(2)、在特定催化剂条件下,两反应存在竞争关系,其反应进程中能量的变化如图所示。该催化剂条件下生成的选择性更高(填化学式),理由为; (3)、TK时,在体积为1L的恒容密闭容器中充入1molCH3OH(g)发生反应i和反应ii,5min后压强不再改变,此时测得H2O(g)的物质的量浓度为0.8mol/L。
(3)、TK时,在体积为1L的恒容密闭容器中充入1molCH3OH(g)发生反应i和反应ii,5min后压强不再改变,此时测得H2O(g)的物质的量浓度为0.8mol/L。①5min内H2O(g)的生成速率为 mol⋅L-1⋅min-1;
②升高温度后,C2H4的平衡产率反而提高,分析原因为。
31. 二氧化碳的捕集与资源化利用是实现碳减排的重要途径。(1)、 的电子式是。(2)、下列物质理论上可以作为 捕集吸收剂的是。(填序号)a.稀 b.氨水c. 溶液d. 溶液
(3)、工业上以 、 为原料生产尿素 ,该反应分为二步进行:第一步:
第二步:
①写出上述合成尿素的热化学方程式。
②某实验小组模拟工业上合成尿素,在一定体积的密闭容器中投入 和 ,实验测得反应中各组分物质的量随时间的变化如图所示:

已知总反应的快慢由慢的一步反应决定,则合成尿素总反应的快慢由第步反应决定,总反应进行到min时到达平衡。
(4)、 较稳定、能量低。为实现 的资源化利用,下列研究方向合理的是(填序号)。a.选择低能量的反应物和 反应获得高能量的生成物
b.利用电能、光能或热能活化 分子
c.选择高效的催化剂
32. CH4-CO2重整反应[CH4(g)+CO2(g)=2CO(g)+2H2(g) △H=+247kJ/mol]在大力推进生态文明建设、“碳达峰”、“碳中和”的时代背景下,受到更为广泛的关注。(1)、I.该反应以两种温室气体为原料,可以生成合成气。如何减少反应过程中的催化剂积炭,是研究的热点之一、某条件下,发生主反应的同时,还发生了积炭反应:CO歧化:2CO(g)=CO2(g)+C(s) △H=-172kJ/mol
CH4裂解:CH4(g)=C(s)+2H2(g) △H=+75kJ/mol
对积炭反应进行计算,得到以下温度和压强对积炭反应中平衡炭量的影响图,其中表示温度和压强对CH4裂解反应中平衡炭量影响的是(选填序号) , 理由是。
 (2)、实验表明,在重整反应中,低温、高压时会有显著积炭产生,由此可推断,对于该重整反应而言,其积炭主要由反应产生。
(2)、实验表明,在重整反应中,低温、高压时会有显著积炭产生,由此可推断,对于该重整反应而言,其积炭主要由反应产生。综合以上分析,为抑制积炭产生,应选用高温、低压条件。
(3)、II.该重整反应也可用于太阳能、核能、高温废热等的储存,储能研究是另一研究热点。该反应可以储能的原因是。
某条件下,除发生主反应外,主要副反应为CO2(g)+H2(g)=CO(g)+H2O(g) △H=+41kJ/mol。研究者研究反应物气体流量、CH4/CO2物质的量比对CH4转化率(XCH4)、储能效率的影响,部分数据如下所示。
(4)、(资料)储能效率:热能转化为化学能的效率,用ηchem表示。ηchem=Qchem/Q。其中,Qchem是通过化学反应吸收的热量,Q是设备的加热功率。序号
加热温度/℃
反应物气体流量/L·min-1
CH4/CO2
XCH4/%
ηchem/%
①
800
4
2:2
79.6
52.2
②
800
6
3:3
64.2
61.9
③
800
6
2:4
81.1
41.6
气体流量越大,CH4转化率越低,原因是:随着流量的提高,反应物预热吸热量增多,体系温度明显降低,。
(5)、对比实验(填序号),可得出结论:CH4/CO2越低,CH4转化率越高。(6)、对比②、③发现,混合气中CO2占比越低,储能效率越高,原因可能是(该条件下设备的加热功率视为不变)。33. 铝及其合金可用作材料、铝热剂等,在环境修复等方面也有着巨大的应用潜力。(1)、铝的冶炼、提纯的方法很多。①高温碳热歧化氯化法冶铝包含的反应之一为:Al2O3(s)+AlCl3(g)+3C(s) 3CO(g)+3AlCl(g),其平衡常数表达式为K=。
②碳热还原Al2O3冶铝的部分反应如下:
Ⅰ.2Al2O3(s)+9C(s)=Al4C3(s)+6CO(g) △H1=akJ/mol
Ⅱ. 4Al2O3(s)+Al4C3(s)=3Al4O4C(s) △H2=bkJ/mol
Ⅲ. Al4O4C(s)+Al4C3(s)=8Al(g)+4CO(g) △H3=ckJ/mol
反应Al2O3(s)+3C(s)=2Al(g)+3CO(g)的△H=kJ/mol
③用离子液体AICb-BMIC(阳离子为EMIM+、阴离子为AlCl4-、Al2Cl7-)作电解质,可实现电解精炼铝。粗铝与外电源的极(填“正”或“负")相连;工作时,阴极的电极反应式为。
(2)、真空条件及1173K时,可用铝热还原Li5AlO4制备金属锂(气态),写出该反应的化学方程式:。(3)、用Al、Fe或Al-Fe合金还原脱除水体中的硝态氮(NO3--N),在45℃,起始c(KNO3-N)为50mg·L-1、维持溶液呈中性并通入Ar等条件下进行脱除实验。结果如图所示(c0为起始浓度、c为剩余浓度):
①纯Al在0~3h时,NO3-几乎没有被脱除,其原因是;写出3h后NO3-被还原为N2的离子方程式:。
②Al-Fe合金1~2h比纯Al 3~4h的脱除速率快得多的可能原因是。
34. SO2在生产、生活中有着广泛的用途。(1)、请你列举一个SO2在生活中的用途:。(2)、SO2在工业上常用于硫酸生产:2SO2(g)+O2(g) 2SO3(g),该反应在一定条件下进行时的热效应如图所示,则其逆反应的活化能为。 (3)、上图中L、X表示物理量温度或压强,依据题中信息可判断:
(3)、上图中L、X表示物理量温度或压强,依据题中信息可判断:①X表示的物理量是 ,
②L1(填“>”“<”或“=”)L2。
(4)、在容积固定的密闭容器中,起始时充入0.2molSO2和0.1molO2 , 反应体系起始总压强为0.1MPa。反应在一定的温度下达到平衡时SO2的转化率为90%。该反应的压强平衡常数Kp=(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。(5)、利用原电池原理,也可用SO2和O2来制备硫酸,该电池用多孔材料作电极。请写出该电池负极的电极反应式:。35. 氮氧化物是大气的主要污染物之一,能形成酸雨、雾霾。大气中的氮氧化物主要来源于燃料的燃烧。(1)、已知:N2(g)+ O2(g) 2NO(g) ΔH= -180.5kJ·mol-1。N≡N键能941kJ·mol-1、O=O键能499 kJ·mol-1 , 则NO中N≡O键的键能为 kJ·mol-1。(2)、T℃时,向1L恒容密闭容器中充入1molN2O3和1molO2 , 发生反应;N2O3(g)+O2(g) N2O5(g) ΔH= -62kJ·mol-1。若平衡时N2O3和N2O5的体积分数相等,则T℃时,该反应的平衡常数K=。(3)、用活化后的N2O5作催化剂,氨气可将NO和O2还原成N2和H2O。若参加反应的NH3和NO的物质的量相等,则该反应的化学方程式为。已知该反应的平衡常数与温度的关系为lg K=5.08+ 。若该反应在t℃下达到平衡,升高温度时,平衡(填“正向“逆向“或“不”)移动,逆反应速率将(填“增大”“减小”或“不变”)。(4)、图I是用食盐水作电解液电解烟气脱氮的一种原理图,NO 被阳极产生的氧化性物质氧化为NO3- , 尾气经氢氧化钠溶液吸收后再排入空气中。电流密度和溶液pH对烟气脱氮的影响如图II。
①处理后的尾气中,一定含有的气体单质是(填化学式)。
②溶液的pH对NO除去率有影响的原因是。
③若电极板面积为10cm2 , 实验烟气含NO的体积分数为1.5%,流速为0.070 L·s-1(气体体积已折算成标准状况,且烟气中无其他气体被氧化),测得电流密度为1.0A·cm-2。实验中NO除去率为(法拉第常数为96500C·mol-1))。