高考二轮复习知识点:金属的通性
试卷更新日期:2023-07-29 类型:二轮复习
一、选择题
-
1. 《天工开物》中记载:“凡乌金纸由苏、杭造成,其纸用东海巨竹膜为质。用豆油点灯,闭塞周围,只留针孔通气,熏染烟光而成此纸,每纸一张打金箔五十度……”下列说法错误的是( )A、“乌金纸”的“乌”与豆油不完全燃烧有关 B、“巨竹膜”为造纸的原料,主要成分是纤维素 C、豆油的主要成分油脂属于天然高分子化合物 D、打金成箔,说明金具有良好的延展性2. 下列有关金属及其化合物的不合理的是( )A、将废铁屑加入 溶液中,可用于除去工业废气中的 B、铝中添加适量钾,制得低密度、高强度的铝合金,可用于航空工业 C、盐碱地(含较多 等)不利于作物生长,可施加熟石灰进行改良 D、无水 呈蓝色,吸水会变为粉红色,可用于判断变色硅胶是否吸水3. 中华文化源远流长、博大精深,陕西历史博物馆馆藏文物是中华文化的重要代表。下列物品主要是由金属材料制成的是
A.白瓷马蹬壶
B.东汉青铜奔马
C.液晶显示屏
D.西夏文佛经纸本



 A、A B、B C、C D、D4. 金属表面的电子在光线照射下逸出产生电流的现象称为光电效应。以下碱金属中最容易发生光电效应的是( )A、Na B、K C、Rb D、Cs5. 中国诗词深受众人喜爱,针对下列一些诗词,从化学角度解读正确的是A、王安石的《梅花》 “遥知不是雪,为有暗香来”描述了物质发生化学变化过程中既有状态变化又有气味的产生 B、庾信的《杨柳歌》“独忆飞絮鹅毛下,非复青丝马尾垂”从化学成分分析现实生活中“飞絮”“鹅毛”主要成分都是蛋白质 C、赵孟頫的《烟火诗》“纷纷灿烂如星陨,赫赫喧虺似火攻”描述了颜色反应的现象 D、刘禹锡的《浪淘沙》“千淘万漉虽辛苦,吹尽狂沙始到金”,说明金在自然界中以游离态存在,其化学性质稳定6. 我国在科技领域取得重大突破。下列说法错误的是( )A、与传统光纤(SiO2)相比,冰光纤(H2O)具有灵活弯曲和高效导光等优点 B、“海宁II号”刷新世界钻探深度,钻头采用硬质合金材料,其硬度低于组分金属 C、“嫦娥五号”运载火箭用液氧液氢做推进剂,产物对环境无污染 D、以CO2和H2为原料人工合成淀粉的过程中发生了氧化还原反应7. 下列方案设计、现象和结论都正确的是( )
A、A B、B C、C D、D4. 金属表面的电子在光线照射下逸出产生电流的现象称为光电效应。以下碱金属中最容易发生光电效应的是( )A、Na B、K C、Rb D、Cs5. 中国诗词深受众人喜爱,针对下列一些诗词,从化学角度解读正确的是A、王安石的《梅花》 “遥知不是雪,为有暗香来”描述了物质发生化学变化过程中既有状态变化又有气味的产生 B、庾信的《杨柳歌》“独忆飞絮鹅毛下,非复青丝马尾垂”从化学成分分析现实生活中“飞絮”“鹅毛”主要成分都是蛋白质 C、赵孟頫的《烟火诗》“纷纷灿烂如星陨,赫赫喧虺似火攻”描述了颜色反应的现象 D、刘禹锡的《浪淘沙》“千淘万漉虽辛苦,吹尽狂沙始到金”,说明金在自然界中以游离态存在,其化学性质稳定6. 我国在科技领域取得重大突破。下列说法错误的是( )A、与传统光纤(SiO2)相比,冰光纤(H2O)具有灵活弯曲和高效导光等优点 B、“海宁II号”刷新世界钻探深度,钻头采用硬质合金材料,其硬度低于组分金属 C、“嫦娥五号”运载火箭用液氧液氢做推进剂,产物对环境无污染 D、以CO2和H2为原料人工合成淀粉的过程中发生了氧化还原反应7. 下列方案设计、现象和结论都正确的是( )方案设计
现象
结论
A
取一段长铝条,伸入 溶液
铝条表面无明显变化
铝活泼性比铜弱
B
向2mL碘水中加入4mL ,振荡后静置
下层显紫红色
在 中的溶解度大于在水中的溶解度
C
向碳酸钠溶液中加少量稀酸HA溶液
无明显气泡逸出
HA的酸性比碳酸的酸性弱
D
向装2mLNaOH浓溶液的试管中加入几滴溴苯,充分振荡
试管内液体分层,下层为无色油状液体
常温下溴苯不易发生水解反应
A、A B、B C、C D、D8. 我国四川广汉的三星堆遗址距今已有3000~5000年历史,2021年3月20日,三星堆遗址新出土了多达500多件重要文物,如黄金面具、丝绸“黑炭”、青铜神树、陶瓷碎片等。下列有关叙述错误的是( )A、考古时利用 C测定文物的年代, C的中子数为8 B、黄金面具、青铜神树的成分均为纯金属 C、丝绸转化为“黑炭”的过程涉及化学变化 D、三星堆中含有大量的陶瓷碎片,属于无机非金属材料9. 化学与生活、社会发展息息相关。下列说法错误的是( )A、将生活垃圾分类投放,分类处理 B、“世间丝、麻、裘皆具素质……”,这里丝、麻的主要成分是蛋白质 C、三星堆发现的金箔,体现了金属的延展性 D、“霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应10. 下列金属单质,不能在特定条件下和水反应的是( )A、镁 B、钠 C、铁 D、银11. 不能通过单质间化合直接制取的是( )
A、CuO B、Cu2S C、Fe3O4 D、Fe2S312. 三星堆遗址被誉为20世纪人类最伟大的考古发现之一。下列叙述错误的是( )选项
出土文物
叙述
A
绝美的黄金面具
自然界中存在游离态的金
B
高大的青铜神像
青铜比纯铜熔点高、硬度大
C
精美的陶器
陶器由黏土经高温烧结而成
D
古蜀国的丝绸遗痕
丝绸的主要成分是蛋白质
A、A B、B C、C D、D13. 下列说法错误的是A、自然界中存在游离态的金属单质 B、金属活动性不同,冶炼方法也有所不同 C、地球上金属矿物资源是取之不尽的,因此,应加大开采金属矿物的速度,以满足经济发展的需要 D、废旧金属的回收利用,有利于环境保护14. 下列关于我国飞机所用的材料中,主要成分属于金属材料的是( ) A、座椅滑轨——铝锂合金 B、轮胎——橡胶 C、尾翼主盒——碳纤维 D、风挡——玻璃15. 手工制作工艺在我国有着悠久的历史,是中华民族文化艺术的瑰宝。下列手工艺品用金属材料制成的是( )
A、座椅滑轨——铝锂合金 B、轮胎——橡胶 C、尾翼主盒——碳纤维 D、风挡——玻璃15. 手工制作工艺在我国有着悠久的历史,是中华民族文化艺术的瑰宝。下列手工艺品用金属材料制成的是( )



A.北京糖人
B.山东面塑
C.芜湖铁画
D.东阳木雕
A、A B、B C、C D、D16. 类推的思维方法在化学学习与研究中有时会产生错误结论,因此类推的结论最终要经过实践的检验,才能决定其正确与否,下列几种类推结论中,正确的是( )A、钠与水反应生成NaOH和H2;所有金属与水反应都生成碱和H2 B、铁露置在空气中一段时间后就会生锈;性质更活泼的铝不能稳定存在于空气中 C、化合物NaCl的焰色为黄色;Na2CO3的焰色也为黄色 D、密度为1.1 g·cm-3与密度为1.2 g·cm-3的NaCl溶液等体积混合,所得NaCl溶液的密度介于1.1 g·cm-3与1.2 g·cm-3之间; Na-K合金的熔点应介于Na和K熔点之间17. 下列有关金属的用途与相应性质不对应的是( )A、用金做饰物是因为金的化学性质稳定、不褪色 B、用钨做白炽灯灯丝是因为其熔点高、导电性好 C、用镁合金做汽车部件是因为镁的密度小,化学性质活泼 D、用铝做包装用的铝箔是因为其延展性好,表面有钝化膜18. 等质量的两份锌粉a、b中分别加入过量的稀硫酸,同时向a中加入少量的CuSO4溶液,下列各图表示的是产生H2的体积V与时间t的关系,其中正确的是( )A、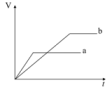 B、
B、 C、
C、 D、
D、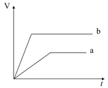 19. 金属的下列性质中,与自由电子无关的是( )A、延展性好 B、容易导电 C、密度大小 D、易导热20. 金属和金属材料与人们的日常生活密不可分,下列认识错误的是( )A、一般用铜而不用银作导线,主要是由于考虑价格的因素 B、铁制品比铝制品容易腐蚀,是由于铁的化学性质比铝活泼 C、用盐酸可区分假黄金,是由于金不能与盐酸反应,而锌能与盐酸反应 D、用硫酸铜配制的波尔多液不能用铁制容器盛放,是因为铁能与硫酸铜发生反应21. 下列单质既能跟氯气直接反应,又能跟稀盐酸反应,且产物不相同的是( )A、Al B、Cu C、Fe D、Zn22. 金属的下列性质中,不能用金属的电子气理论加以解释的是( )A、易导电 B、易导热 C、易腐蚀 D、有延展性23. 化学与生产、生活及社会发展密切相关。下列有关说法错误的是( )A、司母戊鼎、飞机外壳和石灰石均属于合金 B、高纯度的硅单质广泛用于制作半导体材料和太阳能电池 C、铁盐和铝盐均可用于净水 D、利用焰色反应可制成节日烟花24. 下列关于金属及其化合物的说法正确的是( )A、已知CCl4不可燃且不与Na反应,故少量的Na可保存在CCl4液体中 B、向紫色石蕊试液中加入较多Na2O2粉末,溶液变为蓝色并有气泡产生 C、还原铁粉与水蒸气在高温下反应生成有磁性的氧化亚铁 D、胃酸过多的病人,可以服用适量含有氢氧化铝的胃药25. 下列说法错误的是( )A、用激光笔照射Fe(OH)3胶体,可产生“丁达尔效应” B、14N与考古中常用到的14C互称为同位素 C、金刚石、石墨和C60都是碳元素的同素异形体 D、合金的性能可以通过所添加的合金元素的种类、含量和生成合金的条件等加以调节26. 某化学研究小组以“使用金属材料的利与弊”为题进行小组讨论,下列观点不科学的是( )A、金属材料大多有延展性,可以加工成各种形状 B、金属材料中的纯金属可以回收再利用,但合金不可以 C、金属材料中不仅含有金属元素,还可能含有非金属元素 D、金属材料大多有美丽的光泽,可以加工为工艺品27. 2020 年 12 月 17 日嫦娥五号返回器携带月球样品成功返回地面。下列所涉及的材料属于金属材料的是( )
19. 金属的下列性质中,与自由电子无关的是( )A、延展性好 B、容易导电 C、密度大小 D、易导热20. 金属和金属材料与人们的日常生活密不可分,下列认识错误的是( )A、一般用铜而不用银作导线,主要是由于考虑价格的因素 B、铁制品比铝制品容易腐蚀,是由于铁的化学性质比铝活泼 C、用盐酸可区分假黄金,是由于金不能与盐酸反应,而锌能与盐酸反应 D、用硫酸铜配制的波尔多液不能用铁制容器盛放,是因为铁能与硫酸铜发生反应21. 下列单质既能跟氯气直接反应,又能跟稀盐酸反应,且产物不相同的是( )A、Al B、Cu C、Fe D、Zn22. 金属的下列性质中,不能用金属的电子气理论加以解释的是( )A、易导电 B、易导热 C、易腐蚀 D、有延展性23. 化学与生产、生活及社会发展密切相关。下列有关说法错误的是( )A、司母戊鼎、飞机外壳和石灰石均属于合金 B、高纯度的硅单质广泛用于制作半导体材料和太阳能电池 C、铁盐和铝盐均可用于净水 D、利用焰色反应可制成节日烟花24. 下列关于金属及其化合物的说法正确的是( )A、已知CCl4不可燃且不与Na反应,故少量的Na可保存在CCl4液体中 B、向紫色石蕊试液中加入较多Na2O2粉末,溶液变为蓝色并有气泡产生 C、还原铁粉与水蒸气在高温下反应生成有磁性的氧化亚铁 D、胃酸过多的病人,可以服用适量含有氢氧化铝的胃药25. 下列说法错误的是( )A、用激光笔照射Fe(OH)3胶体,可产生“丁达尔效应” B、14N与考古中常用到的14C互称为同位素 C、金刚石、石墨和C60都是碳元素的同素异形体 D、合金的性能可以通过所添加的合金元素的种类、含量和生成合金的条件等加以调节26. 某化学研究小组以“使用金属材料的利与弊”为题进行小组讨论,下列观点不科学的是( )A、金属材料大多有延展性,可以加工成各种形状 B、金属材料中的纯金属可以回收再利用,但合金不可以 C、金属材料中不仅含有金属元素,还可能含有非金属元素 D、金属材料大多有美丽的光泽,可以加工为工艺品27. 2020 年 12 月 17 日嫦娥五号返回器携带月球样品成功返回地面。下列所涉及的材料属于金属材料的是( ) A、超声电机的心脏——压电陶瓷 B、主体框架——钛合金、铝合金 C、国旗旗面——芳纶纤维 D、发动机包裹材料——碳纤维28. 关于金属元素的特征,下列叙述正确的是( )
A、超声电机的心脏——压电陶瓷 B、主体框架——钛合金、铝合金 C、国旗旗面——芳纶纤维 D、发动机包裹材料——碳纤维28. 关于金属元素的特征,下列叙述正确的是( )①金属元素的原子只有还原性,离子只有氧化性②金属元素在化合物中一般显正价 ③金属性越强的元素相应的低价离子氧化性越弱④价电子越多的金属原子的金属性越强
A、①② B、②③ C、①④ D、③④二、非选择题
-
29. 醋酸亚铬[( CH3 COO)₂Cr·2H₂O]为砖红色晶体,难溶于冷水,易溶于酸,在气体分析中用作氧气吸收剂,一般制备方法是先在封闭体系中利用金属锌作还原剂,将三价铬还原为二价铬;二价铬再与醋酸钠溶液作用即可制得醋酸亚铬。实验装置如图所示,回答下列问题:
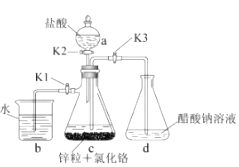 (1)、实验中所用蒸馏水均需经煮沸后迅速冷却,目的是 , 仪器a的名称是。(2)、将过量锌粒和氯化铬固体置于c中,加入少量蒸馏水,按图连接好装置,打开
(1)、实验中所用蒸馏水均需经煮沸后迅速冷却,目的是 , 仪器a的名称是。(2)、将过量锌粒和氯化铬固体置于c中,加入少量蒸馏水,按图连接好装置,打开K1 , K2 , 关闭K3。
①c中溶液由绿色逐渐变为亮蓝色,该反应的离子方程式为。
②同时c中有气体产生,该气体的作用是。
(3)、打开K3 , 关闭K1和K2。c中亮蓝色溶液流入d,其原因是;d中析出砖红色沉淀,为使沉淀充分析出并分离,需采用的操作是、、洗涤、干燥。(4)、指出装置d可能存在的缺点。30. 钛铁矿主要成分为FeTiO3(含有少量MgO、SiO2等杂质),Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿来制备,工艺流程如下: (1)、钛铁矿在预处理时需要进行粉碎,其原因是。(2)、过程①中反应的离子方程式是: FeTiO3 +4H++4Cl-= Fe2++ TiOCl42-+ 2H2O、。(3)、过程①中,铁的浸出率结果如图1所示。由图可知,当铁的浸出率为80%时,所采用的实验条件是。
(1)、钛铁矿在预处理时需要进行粉碎,其原因是。(2)、过程①中反应的离子方程式是: FeTiO3 +4H++4Cl-= Fe2++ TiOCl42-+ 2H2O、。(3)、过程①中,铁的浸出率结果如图1所示。由图可知,当铁的浸出率为80%时,所采用的实验条件是。 (4)、过程②中固体TiO2与双氧水、氨水反应转化成(NH4)2Ti5O15溶液时,Ti元素的浸出率与反应温度的关系如图2所示,反应温度过高时,Ti元素浸出率下降的原因是。(5)、在滤液B转化为FePO4沉淀过程中发生以下反应,请配平:
(4)、过程②中固体TiO2与双氧水、氨水反应转化成(NH4)2Ti5O15溶液时,Ti元素的浸出率与反应温度的关系如图2所示,反应温度过高时,Ti元素浸出率下降的原因是。(5)、在滤液B转化为FePO4沉淀过程中发生以下反应,请配平:Fe2+ + + H3PO4 =FePO4 + +
(6)、过程③中由FePO4制备LiFePO4的化学方程式是。31. 根据所学知识回答下列问题:(1)、常温下镁、铝都具有较强的抗腐蚀性,主要原因是。(2)、标准状况下,与同条件下含有相同的氢原子数。(3)、标准状况下,的质量为g。(4)、实验室用与100mL足量的浓盐酸制取氯气,发生反应:(浓)。当完全反应时,参加反应的HCl的物质的量为 , 假设反应后溶液的体积仍为100mL,则反应后的溶液中生成的的物质的量浓度为mol/L。(5)、实验室需配制溶液,实际应称量绿矾()的质量为。配制时,其正确的操作顺序是(填标号,每个标号只能用一次)。①用水洗涤烧杯内壁和玻璃棒2~3次,洗涤液均注入容量瓶,摇匀
②将准确称量的绿矾倒入烧杯中,再加适量水溶解
③将已冷却的溶液沿玻璃棒注入容量瓶中
④将容量瓶盖紧,反复上下颠倒,摇匀
⑤改用胶头滴管加水,使溶液凹面恰好与刻度线相切
⑥继续往容量瓶内小心加水,直到液面接近刻度线下处
32. 2021年是国际化学年十周年纪念,中国的宣传口号是“化学一我们的生活,我们的未来”。(1)、高纯度单晶硅是典型的无机非金属材料,它的发现和使用曾引起计算机的一场“革命”。下列有关硅材料的说法正确的是____(填字母)。A、晶体硅用于制作半导体材料 B、硅在常温下化学性比较活泼 C、玻璃属于硅酸盐材料 D、玛瑙的主要成分是硅单质(2)、工业上常用金属钠冶炼钛,是利用金属钠的强性。(3)、常温下,可用铁或铝制器皿盛放浓硝酸,是因为。(4)、纯碱和小苏打均为常见的厨房用品。兴趣小组同学用如图装置比较纯碱(Na2CO3)和小苏打(NaHCO3)的热稳定性。实验过程中可以观察到烧杯(填“I”或“II”)中澄清石灰水变浑浊。加热后试管中发生反应的化学方程式为。 (5)、智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘:NaIO3+NaHSO3→NaHSO4+Na2SO4+I2+H2O未配平)。配平并用单线桥法标出上述反应中电子转移的方向和数目。33. 自然界存在及人工合成的金属元素多达90多种。回答下列问题(1)、大多数金属元素在地壳中以(填“游离态”或“化合态”)存在,含量最多的金属是(填元素符号)。人类使用的金属材料包括纯金属和 , 青铜、生铁和硬铝都属后者。(2)、常见金属原子最外层电子数较少,单质在化学反应中常表现出性,请画出金属钠的离子结构示意图。(3)、Na极易被氧化,将金属Na放在坩埚中加热,观察到Na先 , 然后剧烈燃烧,生成淡黄色固体,向该固体中通入CO2 , 反应过程中(填“放出”或“吸收”)热量。(4)、镁片和沸水反应置换出H2该反应的化学方程式为。。
(5)、智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘:NaIO3+NaHSO3→NaHSO4+Na2SO4+I2+H2O未配平)。配平并用单线桥法标出上述反应中电子转移的方向和数目。33. 自然界存在及人工合成的金属元素多达90多种。回答下列问题(1)、大多数金属元素在地壳中以(填“游离态”或“化合态”)存在,含量最多的金属是(填元素符号)。人类使用的金属材料包括纯金属和 , 青铜、生铁和硬铝都属后者。(2)、常见金属原子最外层电子数较少,单质在化学反应中常表现出性,请画出金属钠的离子结构示意图。(3)、Na极易被氧化,将金属Na放在坩埚中加热,观察到Na先 , 然后剧烈燃烧,生成淡黄色固体,向该固体中通入CO2 , 反应过程中(填“放出”或“吸收”)热量。(4)、镁片和沸水反应置换出H2该反应的化学方程式为。。