高考二轮复习知识点:浓硫酸的性质
试卷更新日期:2023-07-28 类型:二轮复习
一、选择题
-
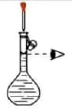
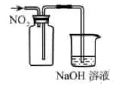
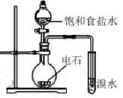
1. 下列实验操作或装置能达到目的的是( )
A
B
C
D
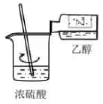
混合浓硫酸和乙醇
配制一定浓度的溶液
收集 气体
证明乙炔可使溴水褪色
A、A B、B C、C D、D2. 下列实验装置(夹持装置略)及操作正确的是( ) A、装置甲气体干燥 B、装置乙固液分离 C、装置丙Cl2制备 D、装置丁pH测试3. 宏观辨识与微观探析是化学学科核心素养之一。下列物质性质实验对应的反应方程式书写正确的是( )A、 放入水中: B、 通过灼热铁粉: C、铜丝插入热的浓硫酸中: D、 通入酸性 溶液中:4. 实验室制备下列气体的方法可行的是( )
A、装置甲气体干燥 B、装置乙固液分离 C、装置丙Cl2制备 D、装置丁pH测试3. 宏观辨识与微观探析是化学学科核心素养之一。下列物质性质实验对应的反应方程式书写正确的是( )A、 放入水中: B、 通过灼热铁粉: C、铜丝插入热的浓硫酸中: D、 通入酸性 溶液中:4. 实验室制备下列气体的方法可行的是( )气体
方法
A
氨气
加热氯化铵固体
B
二氧化氮
将铝片加到冷浓硝酸中
C
硫化氢
向硫化钠固体滴加浓硫酸
D
氧气
加热氯酸钾和二氧化锰的混合物
A、A B、B C、C D、D5. 关于非金属含氧酸及其盐的性质,下列说法正确的是( )A、浓H2SO4具有强吸水性,能吸收糖类化合物中的水分并使其炭化 B、NaClO、KClO3等氯的含氧酸盐的氧化性会随溶液的pH减小而增强 C、加热NaI与浓H3PO4混合物可制备HI,说明H3PO4比HI酸性强 D、浓HNO3和稀HNO3与Cu反应的还原产物分别为NO2和NO,故稀HNO3氧化性更强6. 下列操作规范且能达到实验目的的是( )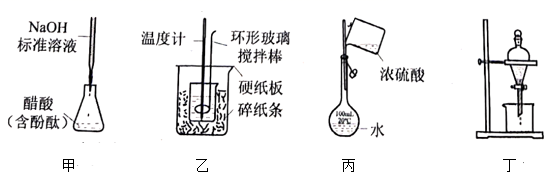 A、图甲测定醋酸浓度 B、图乙测定中和热 C、图丙稀释浓硫酸 D、图丁萃取分离碘水中的碘7. 下列有关化学反应的叙述正确的是( )A、室温下,Na在空气中反应生成Na2O2 B、室温下,Al与4.0 mol﹒L-1NaOH溶液反应生成NaAlO2 C、室温下,Cu与浓HNO3反应放出NO气体 D、室温下,Fe与浓H2SO4反应生成FeSO48. 化学与日常生活密切相关,下列说法错误的是( )A、碘酒是指单质碘的乙醇溶液 B、84消毒液的有效成分是NaClO C、浓硫酸可刻蚀石英制艺术品 D、装饰材料释放的甲醛会造成污染9. 劳动开创未来。下列劳动项目与所述的化学知识有关联的是
A、图甲测定醋酸浓度 B、图乙测定中和热 C、图丙稀释浓硫酸 D、图丁萃取分离碘水中的碘7. 下列有关化学反应的叙述正确的是( )A、室温下,Na在空气中反应生成Na2O2 B、室温下,Al与4.0 mol﹒L-1NaOH溶液反应生成NaAlO2 C、室温下,Cu与浓HNO3反应放出NO气体 D、室温下,Fe与浓H2SO4反应生成FeSO48. 化学与日常生活密切相关,下列说法错误的是( )A、碘酒是指单质碘的乙醇溶液 B、84消毒液的有效成分是NaClO C、浓硫酸可刻蚀石英制艺术品 D、装饰材料释放的甲醛会造成污染9. 劳动开创未来。下列劳动项目与所述的化学知识有关联的是选项
劳动项目
化学知识
A
工厂用铁罐车运输浓硫酸
浓硫酸很难电离出H+ , 与铁不反应
B
将铁闸门与直流电源的负极相连
利用牺牲阳极法保护铁闸门不被腐蚀
C
陶瓷表面上釉
隔绝空气,防止陶瓷被氧化
D
消防演练用泡沫灭火器灭火
Al3+与发生了双水解反应
A、A B、B C、C D、D10. 将蘸有浓硫酸的温度计置于空气中,片刻后,温度计读数升高,说明浓硫酸具有( ) A、吸水性 B、脱水性 C、强酸性 D、氧化性11. 下列实验操作及现象、实验目的或结论均正确的是
A、吸水性 B、脱水性 C、强酸性 D、氧化性11. 下列实验操作及现象、实验目的或结论均正确的是选项
实验操作及现象
目的或结论
A
向盛有蔗糖的烧杯中滴加适量浓硫酸并用玻璃棒迅速搅拌,蔗糖变黑,体积膨胀,产生有刺激性气味的气体
浓硫酸具有吸水性、脱水性和强氧化性
B
向少量酸性溶液中滴加溶液,无明显现象,再向溶液中滴加溶液,溶液变为红色。
该溶液已经完全变质
C
用托盘天平称取1.0g固体,在烧杯中加少量蒸馏水溶解转移至250mL容量瓶中定容
配制250mL的溶液
D
用pH试纸测定和溶液的pH,
F元素非金属性强于Cl元素
A、A B、B C、C D、D12. 下列关于元素及其化合物的性质说法错误的是A、碳和浓硫酸反应可生成 B、实验室用氯化铵分解制氨气 C、Al可溶于NaOH溶液生成偏铝酸钠 D、高温下碳可还原生成硅13. 劳动开创未来。下列劳动项目与所述的化学知识正确的是选项
劳动项目
化学知识
A
工厂用铁罐车运输浓硫酸
浓硫酸很难电离出 , 与铁不反应
B
消防演练用泡沫灭火器灭火
与互相促进使水解反应正向进行
C
陶瓷表面上釉
隔绝空气,防止陶瓷被氧化
D
用苯酚和甲醛制备酚醛树脂
酚醛树脂为高分子化合物,该过程发生了加聚反应
A、A B、B C、C D、D14. 下列选项中,陈述Ⅰ、Ⅱ的化学原理相同的是陈述Ⅰ
陈述Ⅱ
A
不能用浓硫酸干燥NH3
不能用浓硫酸干燥H2S
B
高温时用Na与TiCl4反应制Ti
高温时用Na与KCl反应制K
C
用FeS处理含Cu2+的废水
用含氟牙膏预防龋齿
D
向NaHCO3溶液中滴加AlCl3溶液,产生白色沉淀
向NaHCO3溶液中滴加CaCl2溶液,产生白色沉淀
A、A B、B C、C D、D15. 下列实验中硫酸的作用与其他三项不同的是A、蔗糖中加入浓硫酸产生黑“面包” B、亚硫酸钠与硫酸制取 C、配制溶液时加入稀硫酸 D、海带提碘时硫酸与双氧水混加16. 下列有关物质性质与应用之间具有对应关系的有几种?①浓具有脱水性,可用于干燥氯气
②二氧化氯具有强氧化性,可用作饮用水消毒
③能与盐酸反应,可用作胃酸中和剂
④石英坩埚耐高温,可用来加热熔化烧碱、纯碱等固体
⑤锌的金属活泼性比铁强,可在海轮外壳上装若干锌块以减缓其腐蚀
A、2 B、3 C、4 D、517. 在指定条件下,下列选项所示的物质间的转化能够实现的是( )A、 B、 C、 D、18. 将碳与浓硫酸反应产生的气体分别通入下列溶液后,所得溶液一定澄清的是( )A、品红溶液 B、石灰水 C、氢硫酸 D、硝酸钡溶液19. 北京冬奥会吉祥物“冰墩墩”深受人们的喜爱,一夜间晋级为顶流爆款。据设计团队透露:“冰墩墩”的最初创意灵感来自“冰糖葫芦”,“冰墩墩”的冰晶外壳以硅胶制成,然后再套入毛绒玩具。以下说法正确的是( )A、冬奥会上谷爱凌的滑板、高亭宇的冰刀所用材料的主体成分都是有机高分子材料 B、冰糖成分为蔗糖,其与浓硫酸混合搅拌会生成有毒气体 C、硅胶不与任何酸、碱反应,也不易燃烧 D、真熊猫与熊猫玩具的“毛”主体成分相同,都是纤维素20. 根据下列实验操作和现象,所得到的实验结论正确的是( )选项
实验操作和现象
实验结论
A
将浓硫酸滴到蔗糖表面,固体变黑膨胀
浓硫酸具有吸水性和强氧化性
B
向NaI溶液中滴加少量氯水和CCl4 , 振荡、静置,下层溶液显紫色
还原性:I->Cl-
C
加热盛有NH4Cl固体的试管,试管底部固体消失,试管口有晶体凝结
NH4Cl固体可以升华
D
向某溶液中滴加几滴新制氯水,振荡,再加入少量KSCN溶液,溶液变为红色
该溶液中一定含有Fe2+
A、A B、B C、C D、D21. 下列推断合理的是( )A、明矾在水中能形成胶体,可用作净水剂 B、金刚石是自然界中硬度最大的物质,不能与氧气发生反应 C、浓硫酸具有强氧化性,不能用于干燥 D、将通入品红溶液中,品红溶液褪色后加热恢复原色;将通入溴水中,溴水褪色后加热也能恢复原色22. 下列操作或装置正确并能达到实验目的的是( )


 A、图①用于比较二氧化锰和氧化铁的催化效果 B、图②用此装置可制CaCO3沉淀 C、图③用于检验铜与浓硫酸反应后的混合液中是否含有Cu2+ D、图④用于制备Fe(OH)2沉淀23. 下图所示的实验装置中,实验开始一段时间后,观察到的现象错误的是( )
A、图①用于比较二氧化锰和氧化铁的催化效果 B、图②用此装置可制CaCO3沉淀 C、图③用于检验铜与浓硫酸反应后的混合液中是否含有Cu2+ D、图④用于制备Fe(OH)2沉淀23. 下图所示的实验装置中,实验开始一段时间后,观察到的现象错误的是( ) A、苹果块会干瘪 B、胆矾晶体表面有“白斑” C、小试管内有晶体析出 D、pH试纸变红24. 下列说法错误的是( )A、碳酸氢钠固体受热分解产物均为含氧化合物 B、氯化铝溶液中滴入过量氨水可得到白色沉淀 C、加热条件下铜能与浓硫酸发生反应 D、二氧化硫漂白纸浆是利用了其氧化性25. 陈述Ⅰ和陈述Ⅱ均正确,且具有因果关系的是( )
A、苹果块会干瘪 B、胆矾晶体表面有“白斑” C、小试管内有晶体析出 D、pH试纸变红24. 下列说法错误的是( )A、碳酸氢钠固体受热分解产物均为含氧化合物 B、氯化铝溶液中滴入过量氨水可得到白色沉淀 C、加热条件下铜能与浓硫酸发生反应 D、二氧化硫漂白纸浆是利用了其氧化性25. 陈述Ⅰ和陈述Ⅱ均正确,且具有因果关系的是( )选项
陈述Ⅰ
陈述Ⅱ
A
钠金属性比钾强
可用和熔融在高温下反应制备
B
有导电性
可用于制备光导纤维
C
的熔点高
可用氧化铝坩埚熔化固体
D
浓硫酸具有吸水性
用浓硫酸干燥
A、A B、B C、C D、D26. 下列说法正确的是( )A、谷物发酵酿酒的过程中涉及氧化还原反应 B、向Na2S固体中滴加浓硫酸,发生复分解反应生成H2S C、室温下,将铁片加到浓硝酸中,可制得二氧化氮气体 D、NO2与H2O发生反应生成HNO3 , NO2为酸性氧化物27. 下列说法正确的是( )A、银镜反应实验后附有银的试管,可用稀H2SO4清洗 B、验证氯气是否收集满,可取一片淀粉碘化钾试纸后,放在集气瓶口检验 C、乙酰水杨酸粗产品中加入足量碳酸氢钠溶液,充分反应后过滤,可去除聚合物杂质 D、浓硫酸不能用于干燥NH3、SO2、H2S等气体二、多选题
-
28. 一定条件下,一种反应物过量,另一种反应物仍不能完全反应的是( )A、过量的氢气与氮气 B、过量的浓盐酸与二氧化锰 C、过量的铜与浓硫酸 D、过量的锌与18 mol/L硫酸29. 下列说法正确的是( )A、向乙醇中加入绿豆大小的金属钠有气体产生,说明乙醇中含有H2O B、向蔗糖中加入浓硫酸,蔗糖变黑后膨胀,说明浓硫酸具有吸水性和强氧化性 C、向NaHCO3溶液中滴加紫色石蕊试液,溶液变蓝,说明Kw > Ka1(H2CO3)·Ka2(H2CO3) D、向苯酚稀溶液中逐滴加入饱和溴水有白色沉淀产生,说明羟基对苯环性质产生影响
三、非选择题
-
30. 环己烯是重要的化工原料。其实验室制备流程如下:
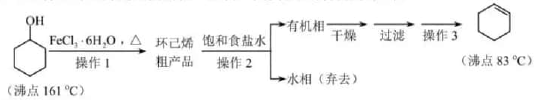
回答下列问题:
(1)、Ⅰ.环己烯的制备与提纯原料环己醇中若含苯酚杂质,检验试剂为 , 现象为。
(2)、操作1的装置如图所示(加热和夹持装置已略去)。
①烧瓶A中进行的可逆反应化学方程式为 , 浓硫酸也可作该反应的催化剂,选择 而不用浓硫酸的原因为(填序号)。
a.浓硫酸易使原料碳化并产生
b. 污染小、可循环使用,符合绿色化学理念
c.同等条件下,用 比浓硫酸的平衡转化率高
②仪器B的作用为。
(3)、操作2用到的玻璃仪器是。(4)、将操作3(蒸馏)的步骤补齐:安装蒸馏装置,加入待蒸馏的物质和沸石, , 弃去前馏分,收集83℃的馏分。(5)、Ⅱ.环己烯含量的测定在一定条件下,向 环己烯样品中加入定量制得的 ,与环己烯充分反应后,剩余的 与足量 作用生成 ,用 的 标准溶液滴定,终点时消耗 标准溶液 (以上数据均已扣除干扰因素)。
测定过程中,发生的反应如下:
①

②
③
滴定所用指示剂为。样品中环己烯的质量分数为(用字母表示)。
(6)、下列情况会导致测定结果偏低的是(填序号)。a.样品中含有苯酚杂质
b.在测定过程中部分环己烯挥发
c. 标准溶液部分被氧化