浙江省绍兴市上虞区2022-2023学年九年级上册科学期末试卷
试卷更新日期:2023-07-26 类型:期末考试
一、选择题(本题共15小题,每小题4分,共60分。下列各小题只有一个选项符合题意)
-
1. 下列事例中,不是通过化学反应提供能量的是( )A、
 B、
B、 C、
C、 D、
D、 2. 分类是化学学习和研究的重要方法之一。下列有关物质的分类错误的是( )A、冰单质 B、石油混合物 C、MnO2氧化物 D、Na2CO3盐3.
2. 分类是化学学习和研究的重要方法之一。下列有关物质的分类错误的是( )A、冰单质 B、石油混合物 C、MnO2氧化物 D、Na2CO3盐3.如图为某文化衫图案,你的美(Mg)偷走我的心(Zn)能发生,是由于镁的( )
 A、延展性好 B、导电性好 C、导热性好 D、金属活动性比锌强4. 在化学反应2HCl+BaCO3=BaCl2+CO2↑+H2O中,没有涉及到的物质类别是( )A、酸 B、碱 C、盐 D、氧化物5. 下列物质的名称、化学式、俗称不一致的是( )A、碳酸钠、Na2CO3、纯碱 B、氯化钠、NaCl、食盐 C、氧化钙、CaO、消石灰 D、氢氧化钠、NaOH、烧碱6. 某智能百叶窗的叶片上贴有太阳能板,在光照时发电,给电动机供电以调节百叶窗的开合。该过程中发生的能量转换是( )A、电能→机械能→光能 B、光能→机械能→电能 C、光能→电能→机械能 D、机械能→电能→光能7. 如图是磷酸二氢钾(KH2PO4)化肥包装上的部分信息,对该化肥叙述不正确的是( )
A、延展性好 B、导电性好 C、导热性好 D、金属活动性比锌强4. 在化学反应2HCl+BaCO3=BaCl2+CO2↑+H2O中,没有涉及到的物质类别是( )A、酸 B、碱 C、盐 D、氧化物5. 下列物质的名称、化学式、俗称不一致的是( )A、碳酸钠、Na2CO3、纯碱 B、氯化钠、NaCl、食盐 C、氧化钙、CaO、消石灰 D、氢氧化钠、NaOH、烧碱6. 某智能百叶窗的叶片上贴有太阳能板,在光照时发电,给电动机供电以调节百叶窗的开合。该过程中发生的能量转换是( )A、电能→机械能→光能 B、光能→机械能→电能 C、光能→电能→机械能 D、机械能→电能→光能7. 如图是磷酸二氢钾(KH2PO4)化肥包装上的部分信息,对该化肥叙述不正确的是( ) A、属于复合肥料 B、易溶于水 C、是纯净物 D、主要含有四种元素8. 如图是自然界中碳、氧循环简图(X为H2CO3 , Y为C6H12O6)。下列说法不正确的是( )
A、属于复合肥料 B、易溶于水 C、是纯净物 D、主要含有四种元素8. 如图是自然界中碳、氧循环简图(X为H2CO3 , Y为C6H12O6)。下列说法不正确的是( ) A、图一中的转化1是酸雨形成的主要原因 B、图二中可实现有机物与无机物的相互转化 C、绿色植物通过光合作用,将太阳能转化成化学能 D、碳循环和氧循环有利于维持大气中氧气和二氧化碳含量的相对稳定9. 频闪照相机是研究物体运动的重要手段之一,图所示的频闪照片记录了竖直下落的小球每隔相等时间的位置,不计空气阻力,在小球下落的过程中,下列说法正确的是( )
A、图一中的转化1是酸雨形成的主要原因 B、图二中可实现有机物与无机物的相互转化 C、绿色植物通过光合作用,将太阳能转化成化学能 D、碳循环和氧循环有利于维持大气中氧气和二氧化碳含量的相对稳定9. 频闪照相机是研究物体运动的重要手段之一,图所示的频闪照片记录了竖直下落的小球每隔相等时间的位置,不计空气阻力,在小球下落的过程中,下列说法正确的是( ) A、小球的重力势能逐渐增大 B、小球的机械能逐渐减小 C、小球的重力在ab段做功比在cd段多 D、小球的重力在ab段做功比在cd段慢10. 下列物质间的转化关系,不能实现的是( )A、H2O2→H2O→H2CO3 B、Mg→MgO→MgSO4 C、KCl→KNO3→K2SO4 D、Cu(OH)2→CuSO4→CuCl211. 用括号内的物质不能区分的一组是( )A、NaCl、NaOH、CaCO3三种固体(水) B、K2CO3、Na2SO4、BaCl2三种溶液(稀硫酸) C、铁粉、碳粉、氧化铜粉末(稀盐酸) D、NaOH、NaCl、Na2SO4三种溶液(酚酞)12. 证据推理是化学学科核心素养的重要内容。下列推理正确的是( )A、碱性溶液能使酚酞变红,能使酚酞变红的溶液一定是碱性溶液 B、活泼金属和酸反应能生成气体,和酸反应生成气体的物质一定是金属 C、有机物中一定含有碳元素,含有碳元素的物质一定是有机物 D、金属能导电,能导电的物质一定是金属13. 某化学小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法错误的是( )
A、小球的重力势能逐渐增大 B、小球的机械能逐渐减小 C、小球的重力在ab段做功比在cd段多 D、小球的重力在ab段做功比在cd段慢10. 下列物质间的转化关系,不能实现的是( )A、H2O2→H2O→H2CO3 B、Mg→MgO→MgSO4 C、KCl→KNO3→K2SO4 D、Cu(OH)2→CuSO4→CuCl211. 用括号内的物质不能区分的一组是( )A、NaCl、NaOH、CaCO3三种固体(水) B、K2CO3、Na2SO4、BaCl2三种溶液(稀硫酸) C、铁粉、碳粉、氧化铜粉末(稀盐酸) D、NaOH、NaCl、Na2SO4三种溶液(酚酞)12. 证据推理是化学学科核心素养的重要内容。下列推理正确的是( )A、碱性溶液能使酚酞变红,能使酚酞变红的溶液一定是碱性溶液 B、活泼金属和酸反应能生成气体,和酸反应生成气体的物质一定是金属 C、有机物中一定含有碳元素,含有碳元素的物质一定是有机物 D、金属能导电,能导电的物质一定是金属13. 某化学小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法错误的是( ) A、该实验是将氢氧化钠溶液滴入稀盐酸中 B、a点所示溶液中,溶质只有NaCl C、b点表示稀盐酸和氢氧化钠溶液恰好完全反应 D、向点c所示溶液中滴加紫色石蕊溶液,溶液变蓝色14. 取碳和氧化铜的混合物ag在一定条件下恰好完全反应,相关量的变化如下图,下列说法正确的是( )
A、该实验是将氢氧化钠溶液滴入稀盐酸中 B、a点所示溶液中,溶质只有NaCl C、b点表示稀盐酸和氢氧化钠溶液恰好完全反应 D、向点c所示溶液中滴加紫色石蕊溶液,溶液变蓝色14. 取碳和氧化铜的混合物ag在一定条件下恰好完全反应,相关量的变化如下图,下列说法正确的是( ) A、M点对应的固体物质只有两种 B、N点对应的固体为黑色 C、反应后产生气体的总质量为(a-b)g D、0~t2min内,固体中铜元素的质量分数不变15. 如图,在光滑的水平台面上,将一轻弹簧左端固定。右端连接一金属小球,O点是弹簧保持原长时小球的位置。压缩弹簧使小球至A位置,然后释放小球,小球就在AB间做往复运动(已知AO=OB)。小球从A位置运动到B位置的过程中,下列判断正确的是( )
A、M点对应的固体物质只有两种 B、N点对应的固体为黑色 C、反应后产生气体的总质量为(a-b)g D、0~t2min内,固体中铜元素的质量分数不变15. 如图,在光滑的水平台面上,将一轻弹簧左端固定。右端连接一金属小球,O点是弹簧保持原长时小球的位置。压缩弹簧使小球至A位置,然后释放小球,小球就在AB间做往复运动(已知AO=OB)。小球从A位置运动到B位置的过程中,下列判断正确的是( ) A、小球的动能不断增加 B、弹簧的弹性势能不断减少 C、小球运动到O点时的动能与此时弹簧的弹性势能相等 D、在任一位置弹簧的弹性势能和小球的动能之和保持不变
A、小球的动能不断增加 B、弹簧的弹性势能不断减少 C、小球运动到O点时的动能与此时弹簧的弹性势能相等 D、在任一位置弹簧的弹性势能和小球的动能之和保持不变二、填空题(本题共7小题,每空2分,共40分)
-
16. 社会发展让人们的出行更加方便,汽车逐渐走进寻常百姓家。回答有关问题:
 (1)、如图汽车的部件中主要由有机合成材料制成的是。(2)、汽车表面的烤漆不仅美观,还能起到的作用。(3)、化石燃料的大量使用,带来了环境的污染和资源的枯竭等问题。我市自2018年开始推广使用车用乙醇汽油,到2019年实现全市全覆盖。乙醇(C2H5OH)燃烧的化学方程式是。(4)、在实验室中探究铝、铜的金属活动性顺序,除铝、铜外,还需要用到的试剂是。(填一种即可)17. 如图所示是神舟十三号载人飞船起飞加速上升阶段的火箭。上升过程的火箭内部的新型返回舱的动能(填“增大”、“减小”或“不变”,下同),火箭整体的机械能。
(1)、如图汽车的部件中主要由有机合成材料制成的是。(2)、汽车表面的烤漆不仅美观,还能起到的作用。(3)、化石燃料的大量使用,带来了环境的污染和资源的枯竭等问题。我市自2018年开始推广使用车用乙醇汽油,到2019年实现全市全覆盖。乙醇(C2H5OH)燃烧的化学方程式是。(4)、在实验室中探究铝、铜的金属活动性顺序,除铝、铜外,还需要用到的试剂是。(填一种即可)17. 如图所示是神舟十三号载人飞船起飞加速上升阶段的火箭。上升过程的火箭内部的新型返回舱的动能(填“增大”、“减小”或“不变”,下同),火箭整体的机械能。 18. 现有三瓶失去标签的无色溶液盐酸、氯化钠溶液和澄清石灰水,(1)、往三种无色溶液中加入某种指示剂即可区别它们,该指示剂可选用。(2)、装澄清石灰水的试剂瓶口常出现白膜,白膜主要成分的化学式是。(3)、上述溶液中属于盐溶液的是。19. 某同学为了探究相关金属的化学性质,做了下列实验:
18. 现有三瓶失去标签的无色溶液盐酸、氯化钠溶液和澄清石灰水,(1)、往三种无色溶液中加入某种指示剂即可区别它们,该指示剂可选用。(2)、装澄清石灰水的试剂瓶口常出现白膜,白膜主要成分的化学式是。(3)、上述溶液中属于盐溶液的是。19. 某同学为了探究相关金属的化学性质,做了下列实验: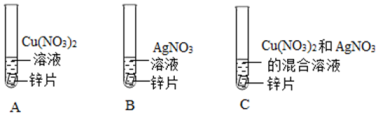 (1)、A试管中实验现象是。(2)、只通过A和B实验尚不能证明铜、银两种金属的活动性强弱,需补充一个实验来证明,补充实验所用试剂合理的是______(填字母)。A、Cu、Ag、稀盐酸 B、Cu、AgNO3溶液(3)、实验C中物质充分反应后,某同学对试管中固体的成分提出以下四种猜想:这四种猜想中明显不合理的是______(填字母)。A、Zn、Cu、Ag B、Zn、Cu C、Cu、Ag D、Ag20. 将氢氧化钠溶液逐滴滴入盐酸和氯化铜的混合溶液中,并根据观察到的现象绘制了如图曲线,根据图示回答问题:
(1)、A试管中实验现象是。(2)、只通过A和B实验尚不能证明铜、银两种金属的活动性强弱,需补充一个实验来证明,补充实验所用试剂合理的是______(填字母)。A、Cu、Ag、稀盐酸 B、Cu、AgNO3溶液(3)、实验C中物质充分反应后,某同学对试管中固体的成分提出以下四种猜想:这四种猜想中明显不合理的是______(填字母)。A、Zn、Cu、Ag B、Zn、Cu C、Cu、Ag D、Ag20. 将氢氧化钠溶液逐滴滴入盐酸和氯化铜的混合溶液中,并根据观察到的现象绘制了如图曲线,根据图示回答问题: (1)、请解释OA段的反应是缘故。(2)、请写出AB段发生反应的化学方程式。(3)、C点处溶液的pH7(填“>”、“=”或“<”)。21. 小明用20N的水平推力,将重为150N的购物车沿水平地面向前推动了10m , 在此过程中,推力对购物车做功J , 支持力对购物车做功J。22. A~F是初中化学常见的六种物质,它们分别是单质、氧化物、有机物、酸、碱、盐中的一种,且均能通过化学反应生成水,如“雪花”图案所示(部分反应物、生成物和反应条件已略去)。已知A是稀盐酸,B是铁锈的主要成分,A能与某些金属反应生成D,且能与E发生中和反应,F是碳酸钠。
(1)、请解释OA段的反应是缘故。(2)、请写出AB段发生反应的化学方程式。(3)、C点处溶液的pH7(填“>”、“=”或“<”)。21. 小明用20N的水平推力,将重为150N的购物车沿水平地面向前推动了10m , 在此过程中,推力对购物车做功J , 支持力对购物车做功J。22. A~F是初中化学常见的六种物质,它们分别是单质、氧化物、有机物、酸、碱、盐中的一种,且均能通过化学反应生成水,如“雪花”图案所示(部分反应物、生成物和反应条件已略去)。已知A是稀盐酸,B是铁锈的主要成分,A能与某些金属反应生成D,且能与E发生中和反应,F是碳酸钠。 (1)、D的化学式为。(2)、A与B发生反应的现象是。(3)、C属于上述物质类别中的。
(1)、D的化学式为。(2)、A与B发生反应的现象是。(3)、C属于上述物质类别中的。三、实验探究题(本题共4小题,每空3分,共45分)
-
23. 相关资料表明,大部分重大交通事故是因为汽车超载超速造成的。兴趣小组决定对超载超速问题进行一次模拟探究,经讨论后认为,可以用小球作为理想模型,代替汽车作为研究对象。如图,将小球从高度为h的同一斜面上由静止开始滚下,推动同一小木块向前移动一段距离s后停下。完成甲、乙、丙三次实验,其中h1=h3>h2 , mA=mB<mC。
 (1)、把小球放在同一高度由静止开始沿斜面滚下是为了控制相同;(2)、实验中超载超速带来的危害程度用表示;(3)、研究超载带来的危害时,选择甲、乙、丙三次实验中的进行比较;(4)、为比较超载超速带来的危害程度,兴趣小组利用上述器材进行定量研究。得到数据如下表:
(1)、把小球放在同一高度由静止开始沿斜面滚下是为了控制相同;(2)、实验中超载超速带来的危害程度用表示;(3)、研究超载带来的危害时,选择甲、乙、丙三次实验中的进行比较;(4)、为比较超载超速带来的危害程度,兴趣小组利用上述器材进行定量研究。得到数据如下表:小球
质量/克
高度/厘米
木块移动距离/厘米
A
10
5
10
B
20
5
18
C
30
5
29
D
10
10
38
E
10
15
86
请根据上表数据分析,货车超载20%与超速20%两者相比,潜在危害较大的是。
24. 常温下,铁在潮湿的空气中容易生锈,产物主要为Fe2O3·nH2O;铁丝在纯氧气中燃烧,产物为黑色的Fe3O4。【提出问题】铁在空气中用酒精灯加热时,是否与空气中氧气发生反应?产物是什么?
【查阅资料】①常见的铁的氧化物有三种:FeO、Fe2O3、Fe3O4 , 其中Fe3O4是磁性物质。
②FeCl3溶液呈黄色,FeCl2溶液呈浅绿色。
【探究】
①按图连接实验装置,检查★。向试管内加入铁粉,针筒活塞停在A刻度。

②加热铁粉的过程中,活塞发生移动。停止加热后,活塞逐渐向左移动,最终停在B刻度。
③用细线吊着洁净铁钉靠近加热后的固体粉末,发现没有粉末被铁钉吸上来。
④向试管内加入盐酸,发现有气泡产生,溶液立即出现黄色。
⑤另取一些未加热过的铁粉加入到盛有盐酸的
试管内,发现有气泡产生,溶液变为浅绿色。
经检验,步骤④、⑤产生的气体相同。
【实验结论与反思】
(1)、步骤①中“★”处应填:。(2)、步骤④、⑤中产生的气体是。(3)、本实验探究的结论是:铁粉在空气中用酒精灯加热时,与空气中氧气发生反应,产物是。(4)、结合已学知识和本次探究分析可得,铁与氧气反应的产物受反应温度、氧气的等因素影响。25. 小明在学习金属活动性顺序后,知道钾、钙、钠金属活动性特别强,能与水反应生成碱和氢气。他想镁紧排在钠后面,它是否也能与水反应呢?【提出问题】镁是否能与水反应?
【实验探究】在两个烧杯中,分别加入等量的冷水和镁条,用酚酞作指示剂。实验过程和现象如图

【反思和总结】
(1)、小明得出的实验结论是。(2)、小明发现B试管放置在空气中一会儿,溶液的红色会褪色,这说明溶液的碱性减弱了。于是他大胆做出了一个猜想并设计了验证方案:猜想
验证方案
可能是氢氧化镁的溶解度受温度的影响,温度降低,溶解度变小,从而导致溶液碱性减弱
将褪色后的溶液 , 如果溶液变红,说明小明的猜想正确
小明通过实验证明了自己的猜想是正确的。
(3)、一段时间后,小明观察到镁条在热水中无现象,这时,他想到实验室制取二氧化碳不能用稀硫酸与大理石反应时,便有了解释,他的解释是。26. 小敏研究影响锌与盐酸反应快慢的因素。
序号
盐酸溶液浓度
2分钟内产生氢气的体积
1
5%
10mL
2
15%
28mL
(1)、 图甲中A、B仪器可以组装一套测量气体体积的装置,利用该装置时A中的管接c。(2)、他选用2克完全相同的锌片分别和同体积5%、15%的稀盐酸进行实验。获得表格数据。由此推断实验是通过来体现反应快慢的。(3)、小敏分析数据得到如下结论:锌与盐酸反应快慢与盐酸浓度有关,盐酸浓度越大反应越快。其他同学认为结论不可靠,他们的依据是:。(4)、实验中小敏发现锌与稀盐酸反应时,一开始产生氢气速度并没有随盐酸浓度的减少而减慢,查阅资料得知化学反应中往往伴随着能量变化。由此作出猜想:锌与盐酸反应快慢还与有关。四、解答题(本题有6小题,共55分)
-
27. 在煤中加入适量的生石灰(CaO)制成供居民采暖用的“环保煤”,以减少二氧化硫的排放,减弱二氧化硫对空气的污染。燃烧时生石灰吸收二氧化硫的化学方程式为:
2CaO+mSO2+O2mCaSO4
请回答下列问题:
(1)、m值是。(2)、该反应属于基本反应类型中的。(3)、若煤厂一次共加入含氧化钙80%的生石灰1400吨,则理论上最多可吸收二氧化硫吨。
28. 2021年5月,我国“天问一号”着陆巡视器成功着陆于火星乌托邦平原(如图甲实现了我国首次地外行星着陆。图乙是其阶段Ⅲ着陆过程中的高度随时间的变化关系。 (1)、火星大气密度是地球的1%,大气中氧气含量为0.15%且没有液态水,表面平均温度为-55℃,绕日公转周期为687天。下列关于火星的说法不合理的是___________。A、表面平均温度比地球低 B、公转周期比地球长 C、大气中氧气含量比地球低 D、雨、雪天数比地球多(2)、图乙中t1~t2时段,着陆巡视器在竖直向上推力作用下,竖直下落的速度减小,该过程中推力F与重力G的大小关系是。(不计大气阻力)(3)、着陆巡视器在火星上总重为4888牛,其重力在t2~t4时段做功焦。29. 小李用下图气体发生装置来制取二氧化碳,老师给他提供了石灰石、无标签的稀盐酸和氯化钠水溶液各一瓶。
(1)、火星大气密度是地球的1%,大气中氧气含量为0.15%且没有液态水,表面平均温度为-55℃,绕日公转周期为687天。下列关于火星的说法不合理的是___________。A、表面平均温度比地球低 B、公转周期比地球长 C、大气中氧气含量比地球低 D、雨、雪天数比地球多(2)、图乙中t1~t2时段,着陆巡视器在竖直向上推力作用下,竖直下落的速度减小,该过程中推力F与重力G的大小关系是。(不计大气阻力)(3)、着陆巡视器在火星上总重为4888牛,其重力在t2~t4时段做功焦。29. 小李用下图气体发生装置来制取二氧化碳,老师给他提供了石灰石、无标签的稀盐酸和氯化钠水溶液各一瓶。 (1)、小李要把稀盐酸选出,可选用下列的______来检验。A、硝酸银溶液 B、酚酞试液 C、pH试纸(2)、小李把石灰石和100克稀盐酸装进发生器中,用天平称量发生器和里面物质的总质量,发现总质量的减小值m与反应时间t的关系如图所示,最后还有少量石灰石剩余。根据图象可知,最终生成二氧化碳的质量为克。(3)、所用稀盐酸的溶质质量分数是多少?(不计水蒸发和稀盐酸的挥发,写出计算过程)。30. 化学小组参与“铅蓄废电池中硫酸回收”的研究项目,回收时需要测定电池废液中硫酸的质量分数。向装有50g废液的锥形瓶中加入质量分数为20%的氢氧化钠溶液,并充分搅拌,利用温度传感器等设备采集信息并绘制成下图,请据图回答问题。(杂可溶但不参加反应)
(1)、小李要把稀盐酸选出,可选用下列的______来检验。A、硝酸银溶液 B、酚酞试液 C、pH试纸(2)、小李把石灰石和100克稀盐酸装进发生器中,用天平称量发生器和里面物质的总质量,发现总质量的减小值m与反应时间t的关系如图所示,最后还有少量石灰石剩余。根据图象可知,最终生成二氧化碳的质量为克。(3)、所用稀盐酸的溶质质量分数是多少?(不计水蒸发和稀盐酸的挥发,写出计算过程)。30. 化学小组参与“铅蓄废电池中硫酸回收”的研究项目,回收时需要测定电池废液中硫酸的质量分数。向装有50g废液的锥形瓶中加入质量分数为20%的氢氧化钠溶液,并充分搅拌,利用温度传感器等设备采集信息并绘制成下图,请据图回答问题。(杂可溶但不参加反应) (1)、该反应是(填“吸热”或“放热”)反应。(2)、恰好完全反应时,溶液的温度为℃。(填“t1”、“t2”或“t3”)。(3)、计算废液中硫酸的质量分数。(写出计算过程)(4)、配制上述实验所用的氢氧化钠溶液。
(1)、该反应是(填“吸热”或“放热”)反应。(2)、恰好完全反应时,溶液的温度为℃。(填“t1”、“t2”或“t3”)。(3)、计算废液中硫酸的质量分数。(写出计算过程)(4)、配制上述实验所用的氢氧化钠溶液。①氢氧化钠固体应放在玻璃器皿中称量的原因是;
②用量筒量水时仰视读数,会导致测定废液中硫酸的质量分数结果(填“偏大”、“偏小”或“不变”)。
31. 跳伞是一项极具挑战的运动,现在越来越受到人们的喜爱,在某次跳伞训练过程中,一体重为500N的运动员从空中悬停的直升机上由静止开始竖直跳下,其速度与时间的关系如图所示,经15s下落210m后,开始做匀速直线运动直至落地,整个过程用时30s,求在这个过程中: (1)、运动员通过的总路程。(2)、重力做的功。(3)、匀速下降时重力做功的功率。32. 铝箔是现代生活中常见的包装材料,放置久了,其银白色光泽会变暗淡,故又称假银箔。
(1)、运动员通过的总路程。(2)、重力做的功。(3)、匀速下降时重力做功的功率。32. 铝箔是现代生活中常见的包装材料,放置久了,其银白色光泽会变暗淡,故又称假银箔。 (1)、小柯用放置很久的铝箔与稀盐酸反应,产生氢气质量和反应时间关系如图所示。在0~t1时间段内,铝箔表面看不到明显的气泡,原因是。(2)、在t2~t3时间段产生气泡的速度逐渐放缓,直到反应停止时,铝箔还有大量剩余。t2~t3时间段产生气泡速度放缓的原因是。(3)、为进一步测量铝箔中单质铝的质量分数,小柯取1.9克铝箔样品与50.0克稀盐酸充分反应(2Al+6HCl=2AlCl3+3H2↑),铝箔完全溶解后剩余溶液的总质量为51.7克。计算样品中单质铝的质量分数。
(1)、小柯用放置很久的铝箔与稀盐酸反应,产生氢气质量和反应时间关系如图所示。在0~t1时间段内,铝箔表面看不到明显的气泡,原因是。(2)、在t2~t3时间段产生气泡的速度逐渐放缓,直到反应停止时,铝箔还有大量剩余。t2~t3时间段产生气泡速度放缓的原因是。(3)、为进一步测量铝箔中单质铝的质量分数,小柯取1.9克铝箔样品与50.0克稀盐酸充分反应(2Al+6HCl=2AlCl3+3H2↑),铝箔完全溶解后剩余溶液的总质量为51.7克。计算样品中单质铝的质量分数。