新疆维吾尔自治区喀什地区巴楚县2022-2023学年高一下学期7月化学期末试题
试卷更新日期:2023-07-19 类型:期末考试
一、单选题
-
1. 关于如图装置所示的两个实验,说法正确的是( )
 A、两个装置中都发生了化学变化,都由化学能转变为电能 B、装置②中电流方向是从Zn经导线流入Cu C、反应开始阶段,两个装置中均有氢气产生 D、电极反应式:阳极 2Cl—-2e-→Cl2↑正极 2H++2e-→H2↑2. 下列关系正确的是( )A、含氢量:苯>乙烯>甲烷 B、密度:H 2O >溴苯 >苯 C、沸点:戊烷>2-甲基丁烷>2,2-二甲基丙烷 D、等质量的下列物质燃烧耗O 2量:乙炔>乙烯>乙烷3. 下列能使湿润的红色石蕊试纸变蓝的气体是( )A、 B、 C、 D、4. 下列有关物质的性质与用途具有对应关系的是( )A、SO2具有还原性,可用作漂白剂 B、Fe粉有还原性,可用作食品抗氧化剂 C、明矾易溶于水,可作净水剂 D、氧化铝硬度大,可作耐火材料5. 下列物质的名称或俗名对应的化学式正确的是( )A、熟石膏: B、过氧化钠: C、生石灰:CaO D、纯碱:NaOH6. 分析下图的能量变化,确定该反应的热化学方程式书写正确的是( )
A、两个装置中都发生了化学变化,都由化学能转变为电能 B、装置②中电流方向是从Zn经导线流入Cu C、反应开始阶段,两个装置中均有氢气产生 D、电极反应式:阳极 2Cl—-2e-→Cl2↑正极 2H++2e-→H2↑2. 下列关系正确的是( )A、含氢量:苯>乙烯>甲烷 B、密度:H 2O >溴苯 >苯 C、沸点:戊烷>2-甲基丁烷>2,2-二甲基丙烷 D、等质量的下列物质燃烧耗O 2量:乙炔>乙烯>乙烷3. 下列能使湿润的红色石蕊试纸变蓝的气体是( )A、 B、 C、 D、4. 下列有关物质的性质与用途具有对应关系的是( )A、SO2具有还原性,可用作漂白剂 B、Fe粉有还原性,可用作食品抗氧化剂 C、明矾易溶于水,可作净水剂 D、氧化铝硬度大,可作耐火材料5. 下列物质的名称或俗名对应的化学式正确的是( )A、熟石膏: B、过氧化钠: C、生石灰:CaO D、纯碱:NaOH6. 分析下图的能量变化,确定该反应的热化学方程式书写正确的是( )
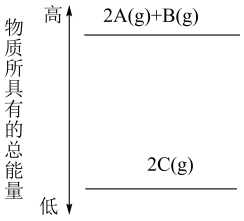 A、2A(g)+B(g)=2C(g) ΔH<0 B、2A(g)+B(g)=2C(g) ΔH>0 C、2A+B=2C ΔH<0 D、2C=2A+B ΔH<07. 汽车发生剧烈碰撞时,安全气囊中迅速发生反应:。下列说法正确的是( )A、该反应中是还原剂 B、氧化产物与还原产物的物质的量之比为15∶1 C、若设计成原电池,在负极上反应 D、每转移 , 可生成8. 、、、氯水都是常见的漂白剂,下列措施能够增强其漂白性的是( )A、向中滴加足量的稀盐酸 B、向的水溶液中滴加少量稀盐酸 C、向的水溶液中滴加氢氧化钠溶液 D、将、按照体积比为1:1的比例通入溶液中9. 书法是中华文化之瑰宝,其美尽在笔墨纸砚之间。下列关于传统文房四宝说法正确的是( )
A、2A(g)+B(g)=2C(g) ΔH<0 B、2A(g)+B(g)=2C(g) ΔH>0 C、2A+B=2C ΔH<0 D、2C=2A+B ΔH<07. 汽车发生剧烈碰撞时,安全气囊中迅速发生反应:。下列说法正确的是( )A、该反应中是还原剂 B、氧化产物与还原产物的物质的量之比为15∶1 C、若设计成原电池,在负极上反应 D、每转移 , 可生成8. 、、、氯水都是常见的漂白剂,下列措施能够增强其漂白性的是( )A、向中滴加足量的稀盐酸 B、向的水溶液中滴加少量稀盐酸 C、向的水溶液中滴加氢氧化钠溶液 D、将、按照体积比为1:1的比例通入溶液中9. 书法是中华文化之瑰宝,其美尽在笔墨纸砚之间。下列关于传统文房四宝说法正确的是( )A
B
C
D




制笔用的狼毫主要成分是蛋白质
墨汁是一种水溶液
宣纸是合成高分子材料
砚石的成分与水晶相同
A、A B、B C、C D、D10. 下列化学用语或分子结构模型表示正确的是( )A、F-的结构示意图: B、四氯甲烷的比例模型:
B、四氯甲烷的比例模型: C、乙醇的结构简式:C2H5OH
D、HClO的电子式:
C、乙醇的结构简式:C2H5OH
D、HClO的电子式: 11. 父亲节快到了!同学们议论着给父亲一个节日礼物,大家的提议集中在不锈钢领带别针、纯棉T恤、玻璃水杯和碳纤维增强网球拍.下列关于礼物材料的说法正确的是( )A、纯棉T恤是复合材料制品 B、不锈钢领带别针是有机材料制品 C、玻璃水杯是无机材料制品 D、碳纤维增强网球拍是无机材料制品12. 下列说法不正确的是( )A、环己烷与苯可用酸性溶液鉴别 B、煤气化生成的水煤气经过催化合成可以得到液体燃料 C、现代工业生产中芳香烃主要来源于石油的催化重整 D、在不同温度下,1,3-丁二烯与溴单质发生加成反应可得不同产物13. 在四个不同的容器中,在不同的条件下进行合成氨反应,根据下列在相同时间内测得的结果判断,生成氨的反应速率最快的是( )A、v(NH3)=0.3 mol·L-1·min-1 B、v(N2)=0.01 mol·L-1·s-1 C、v(N2)=0.2 mol·L-1·min-1 D、v(H2)=0.3 mol·L-1·min-114. 化学与生产、生活密切相关。下列叙述正确的是( )A、为推动生态文明建设,我国近年来大力发展核电、光电、风电、水电,电能属于一次能源 B、打印机墨粉中常加有 , 这是利用了其有颜色和具有磁性的特点,可用CuO替代 C、“天和”号核心舱上使用了目前世界上最先进的三结砷化镓太阳能电池翼,砷化镓属于半导体材料 D、煤经过气化和液化两个物理变化,可变为清洁能源15. 下列关于海水资源综合利用的说法中,正确的是( )A、可用海水晒盐的方法提取海水中的淡水资源 B、只通过物理变化即可提取海水中的溴单质 C、从海带灰中提取I- , 需加入CCl4萃取 D、利用海水、铝、空气发电是将化学能转化为电能16. 下列过程不涉及氧化还原反应的是( )A、金属的冶炼 B、湿润的红色布条遇到氯气褪色 C、明矾净水 D、刻蚀印刷电路板17. 下列各组离子在水溶液中一定能大量共存的是( )A、、、、 B、、、、 C、、、、 D、、、、18. 下列物质在一定条件下能够与硫黄发生反应,且硫作还原剂的是( )A、O2 B、Fe C、H2 D、Cu19. 某溶液中有和 四种离子,若向其中加入过量的 NaOH 溶液,微热并搅拌,再加入过量盐酸,溶液中大量减少的阳离子是( )A、 B、 C、 D、20. 如图为某化学反应的能量—反应进程图,由此可判断该反应为( )
11. 父亲节快到了!同学们议论着给父亲一个节日礼物,大家的提议集中在不锈钢领带别针、纯棉T恤、玻璃水杯和碳纤维增强网球拍.下列关于礼物材料的说法正确的是( )A、纯棉T恤是复合材料制品 B、不锈钢领带别针是有机材料制品 C、玻璃水杯是无机材料制品 D、碳纤维增强网球拍是无机材料制品12. 下列说法不正确的是( )A、环己烷与苯可用酸性溶液鉴别 B、煤气化生成的水煤气经过催化合成可以得到液体燃料 C、现代工业生产中芳香烃主要来源于石油的催化重整 D、在不同温度下,1,3-丁二烯与溴单质发生加成反应可得不同产物13. 在四个不同的容器中,在不同的条件下进行合成氨反应,根据下列在相同时间内测得的结果判断,生成氨的反应速率最快的是( )A、v(NH3)=0.3 mol·L-1·min-1 B、v(N2)=0.01 mol·L-1·s-1 C、v(N2)=0.2 mol·L-1·min-1 D、v(H2)=0.3 mol·L-1·min-114. 化学与生产、生活密切相关。下列叙述正确的是( )A、为推动生态文明建设,我国近年来大力发展核电、光电、风电、水电,电能属于一次能源 B、打印机墨粉中常加有 , 这是利用了其有颜色和具有磁性的特点,可用CuO替代 C、“天和”号核心舱上使用了目前世界上最先进的三结砷化镓太阳能电池翼,砷化镓属于半导体材料 D、煤经过气化和液化两个物理变化,可变为清洁能源15. 下列关于海水资源综合利用的说法中,正确的是( )A、可用海水晒盐的方法提取海水中的淡水资源 B、只通过物理变化即可提取海水中的溴单质 C、从海带灰中提取I- , 需加入CCl4萃取 D、利用海水、铝、空气发电是将化学能转化为电能16. 下列过程不涉及氧化还原反应的是( )A、金属的冶炼 B、湿润的红色布条遇到氯气褪色 C、明矾净水 D、刻蚀印刷电路板17. 下列各组离子在水溶液中一定能大量共存的是( )A、、、、 B、、、、 C、、、、 D、、、、18. 下列物质在一定条件下能够与硫黄发生反应,且硫作还原剂的是( )A、O2 B、Fe C、H2 D、Cu19. 某溶液中有和 四种离子,若向其中加入过量的 NaOH 溶液,微热并搅拌,再加入过量盐酸,溶液中大量减少的阳离子是( )A、 B、 C、 D、20. 如图为某化学反应的能量—反应进程图,由此可判断该反应为( ) A、放热反应 B、吸热反应 C、氧化反应 D、还原反应
A、放热反应 B、吸热反应 C、氧化反应 D、还原反应二、有机推断题
-
21. 乙烯的产量是衡量一个国家石油化工发展水平的标志,乙烯有如下转化关系。
 (1)、B所含官能团的名称为 , 反应③的反应类型为。(2)、反应①的化学方程式。(3)、反应②的化学方程式为。(4)、浓硫酸在反应中的作用是。
(1)、B所含官能团的名称为 , 反应③的反应类型为。(2)、反应①的化学方程式。(3)、反应②的化学方程式为。(4)、浓硫酸在反应中的作用是。三、实验题
-
22. 某化学兴趣小组的同学为探究二氧化硫的化学性质,设计了如下图所示的实验装置。

回答下列问题:
(1)、某同学拧开分液漏斗下面的活塞后发现浓硫酸开始时能流出,但一会儿就停止下流,请分析原因:。(2)、加入浓硫酸后,点燃酒精灯,烧瓶中发生反应的化学方程式为。(3)、反应开始后,观察到B、C两瓶中溶液均褪色,出现该实验现象分别是由于SO2具有性和性。指出实验装置设计的不足之处:。(4)、充分反应后,兴趣小组同学发现铜有剩余,其推测烧瓶中H2SO4是否消耗完,并说明理由:。23. 在实验室里,用加热铵盐和碱的混合物来制取氨气并验证氨气的某些性质。

Ⅰ. 图甲是实验室制取纯净、干燥氨气的装置图
(1)、按图甲组装整套装置后首先要进行的操作是。(2)、写出制备氨气的化学方程式。(3)、物质X是。Ⅱ.将收集到的氨气按图乙做“喷泉实验”,引发该实验的主要操作是。
四、填空题
-
24. 2L恒容密闭容器中,充入0.6molX气体和0.4mol Y气体,发生如下反应: , 5min末容器中W的物质的量为0.2mol。若测得前5min以Z浓度变化来表示的平均反应速率为 , 则:(1)、上述反应的化学方程式中Z的化学计量数n的值是____A、1 B、2 C、3 D、4(2)、上述反应在5min末时,已消耗掉Y的物质的量分数是____A、20% B、25% C、33% D、50%(3)、下列措施可以加快该反应速率的是____A、Y的物质的量减少为0.2mol B、将容器体积扩大至4L C、升高温度 D、向容器中充入与反应无关的氩气
-