广东省2023年中考化学真题
试卷更新日期:2023-07-18 类型:中考真卷
一、单选题
-
1. “夫礼之初,始诸饮食。”下列食物中富含蛋白质的是( )A、鸡蛋 B、苹果 C、青菜 D、白粥2. “粤绣”是国家级非物质文化遗产,以蚕丝线为绣线。下列与蚕丝同属天然材料的是( )A、塑料 B、棉花 C、玻璃 D、涤纶3. “有山千丈色如丹”。广东丹霞山是世界自然遗产,其岩石中含较多氧化铁。下列说法正确的是( )A、氧化铁呈黑色 B、氧化铁中铁元素为+2 价 C、铁元素是人体必需的微量元素 D、人体内缺铁会引起骨质疏松4. 发明联合制碱法,为纯碱工业发展作出杰出贡献的是( )A、张青莲 B、侯德榜 C、拉瓦锡 D、道尔顿5. 化学用语是学习化学的工具。下列表示两个氮原子的是( )A、2N B、N2 C、2NH3 D、N2O46. 下列物质均可用于杀菌消毒,其中属于氧化物的是( )A、O3 B、ClO2 C、NaClO D、C2H5OH7. 铪可用作航天材料,在元素周期表中的信息如图所示。下列有关给元素的说法正确的是( )
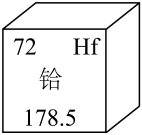 A、核电荷数为72 B、属于非金属元素 C、相对原子质量为 178.5g D、二氧化铪的化学式为O2Hf8. 梦天舱燃烧科学柜采用a作燃料成功实施首次在轨点火实验。a完全燃烧的反应微观示意图如图所示。下列说法错误的是( )
A、核电荷数为72 B、属于非金属元素 C、相对原子质量为 178.5g D、二氧化铪的化学式为O2Hf8. 梦天舱燃烧科学柜采用a作燃料成功实施首次在轨点火实验。a完全燃烧的反应微观示意图如图所示。下列说法错误的是( ) A、反应前后元素种类不变 B、反应前后分子个数不变 C、a分子中C、H原子个数比为1:4 D、反应生成c、d的质量比为 22:99. 下列劳动实践与所述的化学知识没有关联的是( )
A、反应前后元素种类不变 B、反应前后分子个数不变 C、a分子中C、H原子个数比为1:4 D、反应生成c、d的质量比为 22:99. 下列劳动实践与所述的化学知识没有关联的是( )选项
劳动实践
化学知识
A
用铅笔芯制作电极
石墨有导电性
B
用食醋除水垢
水垢能与食醋反应
C
回收铝制易拉罐
铝易与氧气反应
D
用洗涤剂去油污
洗涤剂能乳化油污
A、A B、B C、C D、D10. 下列实验设计能达到实验目的的是( )实验目的
探究 Fe、Cu、Ag的金属活动性强弱
验证质量守恒定律
探究铁锈蚀的条件
验证 MnO2的催化作用
实验设计
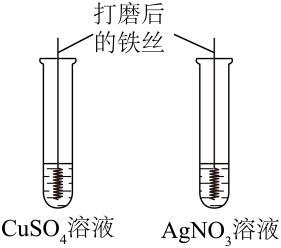
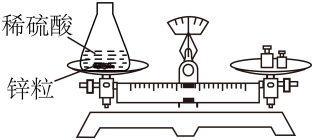
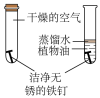

选项
A
B
C
D
A、A B、B C、C D、D二、选择题组
-
11. 项目学习小组在实验室将树叶放入溶质质量分数为10%的NaOH溶液中煮沸,叶肉变黄时取出,洗刷干净后制成叶脉书签,如图甲所示,回答下列问题。(1)、实验要有安全意识。下列行为正确的是( )
 A、在实验室吃零食 B、在实验室追打闹 C、穿实验服和护目镜 D、将药品带出实验室(2)、配制 NaOH 溶液不需用到的仪器是( )A、烧杯 B、量筒 C、漏斗 D、玻璃棒(3)、下列与制作叶脉书签项目有关的说法错误的是( )A、NaOH溶液可以腐蚀叶肉 B、制作过程涉及化学变化 C、制作完成后废液需回收处理 D、NaOH固体存放处应张贴如图乙所示标志12. “盐穴储气” 是一种地下储能技术、 储气时采集盐水, 注水时排天然气, 原理如图所示,回答下列题。(1)、下列说法正确的是( )
A、在实验室吃零食 B、在实验室追打闹 C、穿实验服和护目镜 D、将药品带出实验室(2)、配制 NaOH 溶液不需用到的仪器是( )A、烧杯 B、量筒 C、漏斗 D、玻璃棒(3)、下列与制作叶脉书签项目有关的说法错误的是( )A、NaOH溶液可以腐蚀叶肉 B、制作过程涉及化学变化 C、制作完成后废液需回收处理 D、NaOH固体存放处应张贴如图乙所示标志12. “盐穴储气” 是一种地下储能技术、 储气时采集盐水, 注水时排天然气, 原理如图所示,回答下列题。(1)、下列说法正确的是( ) A、天然气是可再生能源 B、天然气难溶于盐水 C、从m端进气可采集盐水 D、从n端进水可排天然气(2)、采集的盐水主要含 NaCl和少量 MgSO4。根据下图判断,下列说法正确的是( )
A、天然气是可再生能源 B、天然气难溶于盐水 C、从m端进气可采集盐水 D、从n端进水可排天然气(2)、采集的盐水主要含 NaCl和少量 MgSO4。根据下图判断,下列说法正确的是( )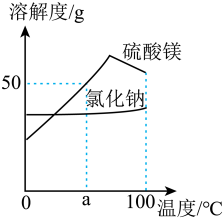 A、溶解度:MgSO4> NaCl B、MgSO4的溶解度随温度升高而增大 C、a℃时,MgSO4溶液的溶质质量分数为50% D、将盐水蒸发结晶,可得到较纯的 NaCl
A、溶解度:MgSO4> NaCl B、MgSO4的溶解度随温度升高而增大 C、a℃时,MgSO4溶液的溶质质量分数为50% D、将盐水蒸发结晶,可得到较纯的 NaCl三、填空题
-
13. 我国是茶文化的发源地。唐代陆羽《茶经》中记载:“风炉以铜铁铸之……底一窗以为通飚漏烬之所……风能兴火,火能熟水。”“漉水囊……其格以生铜铸之。”
 (1)、“铜铁”属于(填“金属”或“合成”)材料。(2)、“飚”(即风)提供燃烧所需的 。“烬”中含钾盐。农业上可用作。(3)、“火能熟水”说明燃烧 (填“吸收”或“放出”)热量。(4)、“漉水囊”可将茶叶与茶水分离,类似于基本实验操作中的 。(5)、茶香四溢,从分子角度解释其原因是 。
(1)、“铜铁”属于(填“金属”或“合成”)材料。(2)、“飚”(即风)提供燃烧所需的 。“烬”中含钾盐。农业上可用作。(3)、“火能熟水”说明燃烧 (填“吸收”或“放出”)热量。(4)、“漉水囊”可将茶叶与茶水分离,类似于基本实验操作中的 。(5)、茶香四溢,从分子角度解释其原因是 。四、科普阅读题
-
14. 地球是一个美丽的“水球”,表面约 71%被水覆盖,淡水仅占总水量的 2.5%;其余是海水或咸水海水淡化是解决人类淡水资源短缺的有效措施。全球海水淡化水用途如图1所示。
海水淡化技术主要有热分离法和膜分离法,热分离法利用热发和冷凝分离水与非挥发性物质,能耗大,成本高;膜分离法利用薄膜的选择透过性实现海水淡化,但现有薄膜的水通量低,应用受到限制,有科学家提出,给石墨烯“打上”许多特定大小的孔,制成单层纳米孔二维薄膜。可进行海水淡化。石墨烯海水淡化膜工作原理如图2所示。

依据上文,回答下列问题。
(1)、全球海水淡化水用途排在首位的是。(2)、热分离法中,水发生了(填“物理变化”或“化学变化”)。限制热分离法大规模应用的原因是 。(3)、石墨烯海水淡化膜允许通过。(4)、石墨烯、金刚石和 C60属于碳单质,下列说法正确的是(填字母)。a.都由碳元素组成 b.都由碳原子构成 c.物理性质相似
(5)、提出爱护水资源的一条建议。五、实验题
-
15. 回答下列问题。(1)、实验室制取O2及性质检验

i.上图中仪器a的名称是。
ii.用高锰酸钾制取O2 , 应选择上图中的发生装置(填字母)。化学方程式为。
iii.收集一瓶O2并进行性质检验。
操作
现象
结论

硫燃烧时,(填字母),生成刺激性气味的气体
a.产生大量白烟
b.生成黑色固体
c.发出蓝紫色火焰
O2具有氧化性
集气瓶中NaOH 溶液的作用是
(2)、制作氧自救呼吸器
查阅资料,超氧化钾(KO2)为黄色固体,分别与CO2、 H2O反应生成O2和白色固体、产氧效率高,适合作生氧剂。
①原理分析:、 则X的化学式为。
②动手实践:设计并制作氧自救呼吸器,如图所示,使用一段时间后,观察到生氧剂由(填颜色变化 ),则基本失效。
六、科学探究题
-
16. 耕地盐碱化影响粮食安全,盐碱地综合治理与利用可促进农业高质量发展,兴趣小组开展了与土壤盐碱化相关的探究活动。
 (1)、成因:由农业灌溉或化肥施用引起的土壤盐碱化如图所示,当进入土壤中盐的量超出植物的吸收能力时,随水分蒸发,导致土壤盐碱化。(2)、检测:配制土壤样品浸出液、用测定、若pH>7、则浸出液显性。(3)、探究:某地土壤碱化可能由 Na2CO3、Na2SO4中的一种两种引起。教师提供模拟盐碱化壤样品浸出液。
(1)、成因:由农业灌溉或化肥施用引起的土壤盐碱化如图所示,当进入土壤中盐的量超出植物的吸收能力时,随水分蒸发,导致土壤盐碱化。(2)、检测:配制土壤样品浸出液、用测定、若pH>7、则浸出液显性。(3)、探究:某地土壤碱化可能由 Na2CO3、Na2SO4中的一种两种引起。教师提供模拟盐碱化壤样品浸出液。[查阅资料] BaCl2易溶于水; BaCO3为白色固体,难溶于水;BaSO4为白色固体,难溶于水和盐酸。
[提出问题]样品中的是什么?
[作出猜想]猜想 1:Na2CO3
猜想2:
猜想3: Na2CO3和Na2SO4
(4)、[实验探究]取少量出分别加管A、B中
实验序号
操作
现象
结论
1
向A中滴加少量BaCl2溶液
产生白色沉淀
含Na2SO4
2
向B中滴加过量稀盐酸
含Na2CO3
(5)、[分析评价]有同学认为实验1不够严谨,理由是(用化学方程式解释)
(6)、[补充实验]实验序号
操作
现象
结论
3
向实验2反应后的溶液中滴加少量BaCl2溶液
猜想3成立
(7)、交流:应对土壤盐碱化的合理措施有(多选,填字母)a.合理施肥 b.引海水灌溉 c.用熟石灰改良 d.种植耐盐碱作物
七、流程题
-
17. 电解水制氢联合碳酸钙分解制备氧化钙,能减少碳排放,助力碳中和。该新方法的示意图如图所示。
 (1)、传统方法:CaCO3在900℃以上完全分解生成 CaO 和(填化学式)。(2)、新方法:
(1)、传统方法:CaCO3在900℃以上完全分解生成 CaO 和(填化学式)。(2)、新方法:i.电解水属于反应(填基本反应类型),反应前后氢元素的化合价(填“升高”“降低”或“不变”)。
ii.反应器 1:一定的H2环境及较低温度下CaCO3可与H2反应生成CaO、CO 和H2O。CO与H2O的分子个数比为。
CaCO3还可以直接分解。反应器 1中 CO、CO2的含量随反应温度的变化如下图所示。 ℃时,抑制 CO2生成的效果最好。

iii.反应器 2:一定条件下,CO与H2发生化合反应生成甲醇(CH3OH),化学方程式为 。
(3)、与传统方法相比,新方法的优点有(写两条)。八、综合应用题
-
18. 羰基铁粉在国防军工领域有重要应用,我国是少数几个掌握其生产技术的国家之一。制备羰基铁粉的过程如图所示。
 (1)、Fe(CO)5中碳、氧元素的质量比为。(2)、反应1的化学方程式为 。用100 kg含铁96%的海绵铁,理论上可制备Fe(CO)5的质量是多少?(写出计算过程)(3)、反应2的化学方程式为 。196kgFe(CO)5分解生成基铁粉的质量随时间的变化如下图所示。在t1时,剩余 kg Fe(CO)5未分解;在时Fe(CO)5恰好完全分解。
(1)、Fe(CO)5中碳、氧元素的质量比为。(2)、反应1的化学方程式为 。用100 kg含铁96%的海绵铁,理论上可制备Fe(CO)5的质量是多少?(写出计算过程)(3)、反应2的化学方程式为 。196kgFe(CO)5分解生成基铁粉的质量随时间的变化如下图所示。在t1时,剩余 kg Fe(CO)5未分解;在时Fe(CO)5恰好完全分解。 (4)、制备羰基铁粉过程中循环利用的物质是 。
(4)、制备羰基铁粉过程中循环利用的物质是 。
-
-
-
-
-