四川省眉山市2023年中考化学真题
试卷更新日期:2023-07-13 类型:中考真卷
一、单选题
-
1. 从中草药中分离出青蒿素,应用于疟疾的治疗,从而获得了诺贝尔医学奖的科学家是( )A、侯德榜 B、屠呦呦 C、门捷列夫 D、道尔顿2. 空气中体积分数约占78%的气体是( )A、二氧化碳 B、氮气 C、氧气 D、稀有气体3. 化学与我们的生活息息相关,下列说法错误的是( )A、氮气可用于食品充氮防腐 B、活性炭可用于冰箱除味剂 C、氢氧燃料电池用作汽车的驱动电源可以减少空气污染 D、商场里标有“补钙”“补铁”的保健品,这里的“钙铁”指的是单质4. 以下化学实验操作正确的是( )A、将大理石保存在细口瓶中
 B、将水缓慢加入浓硫酸中
B、将水缓慢加入浓硫酸中 C、量取液体
C、量取液体 D、加热液体
D、加热液体 5. 下表为四种食物的近似pH,你认为胃酸过多的患者不宜多吃的食物是( )
5. 下表为四种食物的近似pH,你认为胃酸过多的患者不宜多吃的食物是( )食物
苹果汁
豆浆
玉米粥
鸡蛋清
pH
2.9-3.3
7.4-7.9
6.8-8.0
7.6-8.0
A、苹果汁 B、豆浆 C、玉米粥 D、鸡蛋清6. 中华传统文化博大精深,很多成语、诗词和谚语中蕴含着丰富的科学道理。下列说法错误的是( )A、“木已成舟”与“铁杵成针”都属于化学变化 B、“遥知不是雪,为有暗香来”体现了分子在不断的运动 C、“真金不怕火炼”说明黄金的化学性质非常稳定 D、“冰,水为之,而寒于水”体现了物质的状态不同,物理性质不同7. 科学家利用某纳米纤维催化剂将二氧化碳转化为液体燃料甲醇(CH3OH),其微观示意图如下(图中的分子恰好完全反应)。下列说法错误的是( ) A、生成物丙中碳元素的质量分数为37.5% B、该反应的化学方程式为 C、生成物丙和丁的质量比为1:1 D、该反应有助于实现“碳中和”8. 下列有关纯碱的认识错误的是( )A、组成:由碳、氧和钠三种元素组成 B、性质:能与BaCl2、NaCl等盐溶液反应 C、用途:用于玻璃、造纸、纺织等的生产 D、生产:侯氏制碱法9. X、Y、Z、W四种元素的质子数如图所示。下列说法错误的是( )
A、生成物丙中碳元素的质量分数为37.5% B、该反应的化学方程式为 C、生成物丙和丁的质量比为1:1 D、该反应有助于实现“碳中和”8. 下列有关纯碱的认识错误的是( )A、组成:由碳、氧和钠三种元素组成 B、性质:能与BaCl2、NaCl等盐溶液反应 C、用途:用于玻璃、造纸、纺织等的生产 D、生产:侯氏制碱法9. X、Y、Z、W四种元素的质子数如图所示。下列说法错误的是( ) A、X与W属于同一周期 B、Z与Y能形成两种常见的化合物 C、在化学反应中,Y原子易得到电子,W原子易失去电子 D、常温下,X、Y、W三种元素组成的化合物的水溶液pH>710. 根据如图,下列气体的实验室制法正确的是( )
A、X与W属于同一周期 B、Z与Y能形成两种常见的化合物 C、在化学反应中,Y原子易得到电子,W原子易失去电子 D、常温下,X、Y、W三种元素组成的化合物的水溶液pH>710. 根据如图,下列气体的实验室制法正确的是( )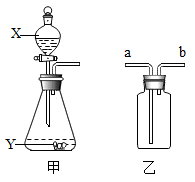 A、选择甲装置制取CO2 , X为稀硫酸 B、选择甲装置制取H2 , Y为铜粒 C、选择乙装置既可收集H2也可收集CO2 D、选择乙装置干燥O2 , 气流方向为b进a出11. 实验设计是实验探究的基本环节。下列实验设计能达到对应实验目的的是( )
A、选择甲装置制取CO2 , X为稀硫酸 B、选择甲装置制取H2 , Y为铜粒 C、选择乙装置既可收集H2也可收集CO2 D、选择乙装置干燥O2 , 气流方向为b进a出11. 实验设计是实验探究的基本环节。下列实验设计能达到对应实验目的的是( )选项
实验目的
实验设计
A
鉴别白酒和白糖水
观察颜色
B
除去KCl溶液中的少量K2SO4
加适量BaCl2溶液,过滤
C
除去氨气中的水蒸气
将气体通过浓硫酸
D
探究铜、银的金属活动性顺序
将铜丝、银丝分别浸入稀盐酸溶液中
A、A B、B C、C D、D12. 下列描述涉及反应的化学方程式正确的是( )A、服用含氢氧化铝的药物治疗胃酸过多: B、用过氧化氢溶液制氧气: C、将铁丝浸入稀盐酸中: D、用食醋清洗水壶中的水垢:13. 实验小组用传感器探究稀NaOH溶液与稀盐酸反应过程中温度和pH的变化。测定结果如图所示。下列说法错误的是( ) A、反应过程中有热量放出 B、30s时,溶液中溶质为HCl和NaCl C、60s时,加入1~2滴紫色石蕊溶液变成蓝色 D、该实验是将稀盐酸加入稀NaOH溶液14. 将一块已生锈的铁片放入质量分数为7.3%的稀盐酸中充分反应,测得生成的H2的质量与稀盐酸的质量关系如图所示(假设铁片除有外不含其他杂质)。下列说法错误的是( )
A、反应过程中有热量放出 B、30s时,溶液中溶质为HCl和NaCl C、60s时,加入1~2滴紫色石蕊溶液变成蓝色 D、该实验是将稀盐酸加入稀NaOH溶液14. 将一块已生锈的铁片放入质量分数为7.3%的稀盐酸中充分反应,测得生成的H2的质量与稀盐酸的质量关系如图所示(假设铁片除有外不含其他杂质)。下列说法错误的是( ) A、配制200g质量分数为7.3%的稀盐酸需要质量分数为36.5%的浓盐酸40g B、刚开始加稀盐酸时发生反应的化学方程式为 C、加入12g稀盐酸时,溶液中的溶质为FeCl2和FeCl3 D、m=0.2
A、配制200g质量分数为7.3%的稀盐酸需要质量分数为36.5%的浓盐酸40g B、刚开始加稀盐酸时发生反应的化学方程式为 C、加入12g稀盐酸时,溶液中的溶质为FeCl2和FeCl3 D、m=0.2二、填空题
-
15. 按要求填空:(1)、2个氢原子。(2)、画出硅原子的结构示意图。(3)、农家常用草木灰作(填“氮肥”、“磷肥”或“钾肥”)。(4)、地壳中含量最多的金属元素是。(5)、天然气的主要成分是甲烷(CH4),CH4属于(填“有机物”或“无机物”)。16. 红色经典影片《闪闪的红星》中有一段儿童团员潘冬子给红军送盐的故事。冬子开始把食盐装在竹筒中,打算扮作上山砍柴的人将食盐送给红军。途中发现敌人盘查严格,冬子急中生智跑到河边,把竹筒里的食盐全部溶成盐水,再用棉袄吸收,最终顺利地将食盐送给了红军。回答下列问题:(1)、从物质分类的角度分析,盐水属于(填“纯净物”或“混合物”);从物质变化的角度分析,食盐溶成盐水属于(填“物理变化”或“化学变化”)。(2)、从棉袄中挤出盐水,过滤,蒸发得到食盐。其中用到的玻璃仪器有烧杯、玻璃棒、酒精灯和。(3)、氯化钠的溶解度如下表。假设冬子的竹筒中有179g氯化钠,10℃时完全溶解所需水的质量至少为g。
温度/℃
0
10
20
30
40
50
60
氯化钠溶解度/g
35.7
35.8
36.0
36.3
36.6
37.0
37.8
(4)、氯化钠在生活中的用途:(任写一点即可)。17. 根据下图所示实验回答问题。 (1)、A中反应的化学方程式为 , 其基本反应类型是。(2)、B中铁丝在氧气中剧烈燃烧,火星四射,生成色固体。(3)、C中连接电源正、负两极玻璃管内产生的气体体积比约为。
(1)、A中反应的化学方程式为 , 其基本反应类型是。(2)、B中铁丝在氧气中剧烈燃烧,火星四射,生成色固体。(3)、C中连接电源正、负两极玻璃管内产生的气体体积比约为。三、流程题
-
18. 钛金属具有硬度大、密度小、熔点高、常温下耐酸碱、耐腐蚀等优良的性能,被誉为“未来金属”。我国钒钛磁铁矿床分布广泛,储量丰富,由钒钛磁铁矿提取金属钛的主要工艺过程如下。

回答下列问题:
(1)、钛铁矿需要粉碎,其目的是。(2)、钛铁矿的主要成分为钛酸亚铁(FeTiO3),其中钛元素的化合价为价。(3)、TiCl4在高温下与足量Mg反应生成金属钛,该反应的化学方程式为。(4)、金属矿物不能再生。下列能有效保护钛金属资源的措施是____。A、回收利用废旧钛金属制品 B、任意开采钛金属矿石 C、钛金属抗腐蚀性能好,可随意堆放储存 D、寻找、开发钛金属的代替品四、科学探究题
-
19. 某化学兴趣小组发现上次做实验用的澄清石灰水忘记了盖瓶盖,试剂瓶内壁附着一层白色固体、底部也有白色固体。
【提出问题】白色固体是什么?怎样产生的?
【猜想与假设】
猜想一:碳酸钙;空气中的二氧化碳与澄清石灰水反应生成碳酸钙。猜想二:氢氧化钙;水分蒸发,析出氢氧化钙固体。猜想三:氢氧化钙和碳酸钙的混合物。
【实验探究】
(1)、甲同学取少量白色固体于试管中,加入过量稀盐酸,振荡,固体全部溶解并有气泡产生。产生气泡的化学方程式为。(2)、甲同学得出结论:猜想一正确。乙同学提出质疑,认为甲同学实验结论不够严谨,其理由是(用化学方程式表示),并补充实验如下:
实验步骤
实验现象
实验结论
白色固体既含有碳酸钙又含有氢氧化钙
(3)、【实验结论】综上所述,猜想三正确。
【实验反思】
澄清石灰水必须要保存。
五、计算题
-
20. 磁铁矿石(主要成分为)是常用的炼铁原料,工业上可通过如下反应:将其中的Fe3O4转化为Fe.(1)、Fe3O4中铁、氧的微观粒子数目之比为。(2)、假设炼铁过程中铁没有损耗,用含348吨Fe3O4的磁铁矿石理论上可以炼出含铁96%的生铁的质量是多少(写出计算过程)?
-
-