吉林省长春市吉大附中力旺实验中学2021-2022九下第九次周考——化学试卷
试卷更新日期:2023-07-07 类型:月考试卷
一、选择题(共10分)
-
1. 空气成分中,体积分数最大的是()A、氧气 B、氮气 C、稀有气体 D、二氧化碳2. 中华文字博大精深,下列成语主要涉及化学变化的是( )A、滴水成冰 B、火上浇油 C、立竿见影 D、沙里淘金3. 下列物质属于氧化物的是( )A、O3 B、KClO3 C、CuSO4 D、Al2O34. 下列实验操作正确的是( )A、滴加液体
 B、量取液体
B、量取液体 C、振荡试管
C、振荡试管 D、塞紧橡胶塞
D、塞紧橡胶塞 5. 某牛仔裤标签如图所示,下列说法不正确的是( )
5. 某牛仔裤标签如图所示,下列说法不正确的是( ) A、合成纤维耐磨性较差 B、聚酯纤维是合成纤维 C、棉纤维透气性较好 D、用灼烧的方法可区分棉纤维与聚酯纤6. 食用泡腾片中含有柠檬酸(C6H8O7),下列有关柠檬酸说法不正确的是( )A、属于有机物 B、氧元素的质量分数最大 C、柠檬酸分子中含有21个原子 D、碳、氢元素的质量比为9:17. 实验室用质量分数为6%的氯化钠溶液(密度约为1.04g/cm3)配制50g质量分数为3%的氯化钠溶液。下列说法正确的是( )A、需要加水的质量是50g B、量取水时俯视会使浓度偏小 C、玻璃棒的作用是加速固体溶解 D、量取6%的氯化钠溶液时选用25mL的量筒8. 推理是化学常用的学习方法,以下推理正确的是( )A、金属能导电,所以能导电的物质一定是金属 B、溶液是均一的、稳定的,所以均一的、稳定的物质一定是溶液 C、构成过氧化氢和水的分子不同,所以化学性质一定不同 D、中和反应有盐和水生成,所以有盐和水生成的反应一定是中和反应9. 除去下列物质中混有的少量杂质(括号内为杂质)的方法错误的是( )A、铜粉(铁粉)——用磁铁吸引 B、二氧化碳(氯化氢)一一通过足量的氢氧化钠溶液 C、硫酸钠溶液(碳酸钠)——加入适量稀硫酸 D、碳酸钙(氯化钙)——加适量的水溶解、过滤、洗涤、干燥10. 甲、乙、丙、丁是初中化学常见的物质,其中甲、丁是红色固体,金属乙的年产量居第一位,丙为最轻的气体,它们间的转化关系如图所示,下列有关说法,错误的是( )
A、合成纤维耐磨性较差 B、聚酯纤维是合成纤维 C、棉纤维透气性较好 D、用灼烧的方法可区分棉纤维与聚酯纤6. 食用泡腾片中含有柠檬酸(C6H8O7),下列有关柠檬酸说法不正确的是( )A、属于有机物 B、氧元素的质量分数最大 C、柠檬酸分子中含有21个原子 D、碳、氢元素的质量比为9:17. 实验室用质量分数为6%的氯化钠溶液(密度约为1.04g/cm3)配制50g质量分数为3%的氯化钠溶液。下列说法正确的是( )A、需要加水的质量是50g B、量取水时俯视会使浓度偏小 C、玻璃棒的作用是加速固体溶解 D、量取6%的氯化钠溶液时选用25mL的量筒8. 推理是化学常用的学习方法,以下推理正确的是( )A、金属能导电,所以能导电的物质一定是金属 B、溶液是均一的、稳定的,所以均一的、稳定的物质一定是溶液 C、构成过氧化氢和水的分子不同,所以化学性质一定不同 D、中和反应有盐和水生成,所以有盐和水生成的反应一定是中和反应9. 除去下列物质中混有的少量杂质(括号内为杂质)的方法错误的是( )A、铜粉(铁粉)——用磁铁吸引 B、二氧化碳(氯化氢)一一通过足量的氢氧化钠溶液 C、硫酸钠溶液(碳酸钠)——加入适量稀硫酸 D、碳酸钙(氯化钙)——加适量的水溶解、过滤、洗涤、干燥10. 甲、乙、丙、丁是初中化学常见的物质,其中甲、丁是红色固体,金属乙的年产量居第一位,丙为最轻的气体,它们间的转化关系如图所示,下列有关说法,错误的是( )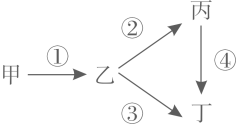 A、转化①发生反应的基本反应类型不能是置换反应 B、完成转化②,所得溶液呈浅绿色 C、由转化③可知金属活动性顺序:乙>丁 D、完成转化④,物质丙的实际用量要大于理论用量
A、转化①发生反应的基本反应类型不能是置换反应 B、完成转化②,所得溶液呈浅绿色 C、由转化③可知金属活动性顺序:乙>丁 D、完成转化④,物质丙的实际用量要大于理论用量二、非选择题(共40分)
-
11. 化学用语是学习化学的重要工具,请用适当的化学用语填空。(1)、氢原子;(2)、铵根离子;(3)、过氧化氢分子。12. 2022年2月第24届冬奥运动会中,碲化镉发电玻璃成为绿色和科技办奥创新点。(1)、①碲元素在周期表中信息为图1,其符号为;
②碲原子的相对原子质量为;
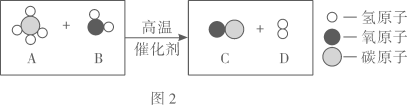
 (2)、氢燃料为本届冬奥会服务,工业上大规模生产H2的微观示意图如图2:
(2)、氢燃料为本届冬奥会服务,工业上大规模生产H2的微观示意图如图2:①该反应中涉及的化合物有种;
②反应生成C和D的质量比为。
 13. 自来水厂净化水的主要步骤如图所示,请回答相关问题。
13. 自来水厂净化水的主要步骤如图所示,请回答相关问题。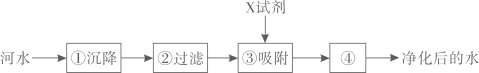 (1)、步骤①中加入明矾的作用是;(2)、步骤③加入X试剂是 , 它可以除去色素和异味;(3)、步骤①到步骤④中可除去难溶性杂质的是;(填序号)(4)、可用检验净化后的水是硬水或软水。14. 用如图实验验证可燃物燃烧的条件。
(1)、步骤①中加入明矾的作用是;(2)、步骤③加入X试剂是 , 它可以除去色素和异味;(3)、步骤①到步骤④中可除去难溶性杂质的是;(填序号)(4)、可用检验净化后的水是硬水或软水。14. 用如图实验验证可燃物燃烧的条件。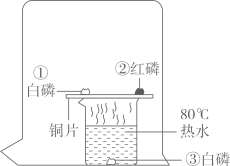 (1)、①处白磷燃烧而②处红磷不燃烧可得出的结论是;(2)、铜片上白磷能燃烧是利用铜的性;(3)、倒扣的大烧杯的作用是;(4)、要使烧杯中的白磷燃烧,可采用的操作是 。A、将水加热至90℃ B、将白磷从水中取出 C、向水中通入氧气15. 2022年4月16日,神舟十三号载人飞船成功着陆。(1)、飞船的建造使用了高强钛合金,可避免空中物体撞击,体现了钛合金有 的优点;A、硬度大 B、密度大 C、熔点低(2)、飞船与地面联系需要镍钛合金制作的自展天线,镍钛合金在低温下被折叠,进入太空后,在阳光照射下可重新展开,恢复成原状,这是利用了镍钛合金的功能;(3)、飞船使用的SiC颗粒增强铝基复合材料、超高强度钢等材料引起关注,其中超强度钢属于(填“金属”或“合成”)材料;(4)、要比较钢材料中锰(Mn)和铁的金属活动顺序,以下方法能达到目的的是 。A、查阅化学课本金属活动性顺序表 B、利用金属锰和FeSO4溶液进行实验 C、利用金属铁和MnSO4溶液进行实验 D、利用锰、铁与稀硫酸进行实验16. 根据所给氯化钠和碳酸钠溶解度曲线信息,回答下列问题。
(1)、①处白磷燃烧而②处红磷不燃烧可得出的结论是;(2)、铜片上白磷能燃烧是利用铜的性;(3)、倒扣的大烧杯的作用是;(4)、要使烧杯中的白磷燃烧,可采用的操作是 。A、将水加热至90℃ B、将白磷从水中取出 C、向水中通入氧气15. 2022年4月16日,神舟十三号载人飞船成功着陆。(1)、飞船的建造使用了高强钛合金,可避免空中物体撞击,体现了钛合金有 的优点;A、硬度大 B、密度大 C、熔点低(2)、飞船与地面联系需要镍钛合金制作的自展天线,镍钛合金在低温下被折叠,进入太空后,在阳光照射下可重新展开,恢复成原状,这是利用了镍钛合金的功能;(3)、飞船使用的SiC颗粒增强铝基复合材料、超高强度钢等材料引起关注,其中超强度钢属于(填“金属”或“合成”)材料;(4)、要比较钢材料中锰(Mn)和铁的金属活动顺序,以下方法能达到目的的是 。A、查阅化学课本金属活动性顺序表 B、利用金属锰和FeSO4溶液进行实验 C、利用金属铁和MnSO4溶液进行实验 D、利用锰、铁与稀硫酸进行实验16. 根据所给氯化钠和碳酸钠溶解度曲线信息,回答下列问题。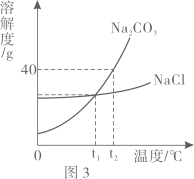 (1)、t1℃时,NaCl溶解度(填“大于”、“小于”、或“等于”) Na2CO3溶解度;(2)、t2℃时,将40g Na2CO3固体加入50g水中,所得溶液中溶质与溶剂的质量比为(最简整数比);(3)、若Na2CO3中混有少量的NaCl,提纯Na2CO3应采取的方法是;(4)、观察溶解度曲线,下列说法正确的是 。A、t1℃时,NaCl和Na2CO3两种饱和溶液中,所含溶质质量不一定相等 B、t1℃(不包含t1℃)到t2℃之间,能配制出溶质质量分数相等的NaCl和Na2CO3溶液 C、将氯化钠溶液经过某种操作后,析出晶体,过滤后所得溶液溶质质量分数与原溶液相比,不可能变大17. 实验室里现有氯酸钾、二氧化锰、稀硫酸、石灰石和稀盐酸,以及下列仪器。
(1)、t1℃时,NaCl溶解度(填“大于”、“小于”、或“等于”) Na2CO3溶解度;(2)、t2℃时,将40g Na2CO3固体加入50g水中,所得溶液中溶质与溶剂的质量比为(最简整数比);(3)、若Na2CO3中混有少量的NaCl,提纯Na2CO3应采取的方法是;(4)、观察溶解度曲线,下列说法正确的是 。A、t1℃时,NaCl和Na2CO3两种饱和溶液中,所含溶质质量不一定相等 B、t1℃(不包含t1℃)到t2℃之间,能配制出溶质质量分数相等的NaCl和Na2CO3溶液 C、将氯化钠溶液经过某种操作后,析出晶体,过滤后所得溶液溶质质量分数与原溶液相比,不可能变大17. 实验室里现有氯酸钾、二氧化锰、稀硫酸、石灰石和稀盐酸,以及下列仪器。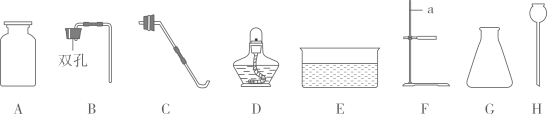 (1)、认识仪器:仪器a的名称是;(2)、制取气体:利用石灰石和稀盐酸可以制取CO2气体,选择的仪器是ABG和①(填序号);若补充上种仪器② (填名称)再利用上述仪器和药品可以制取氧气;(3)、探究性质:①实验一 (填 “能”或“不能”)得出二氧化碳密度大于空气;
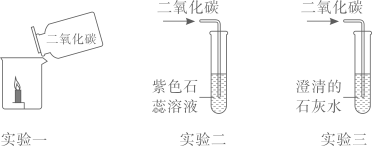
(1)、认识仪器:仪器a的名称是;(2)、制取气体:利用石灰石和稀盐酸可以制取CO2气体,选择的仪器是ABG和①(填序号);若补充上种仪器② (填名称)再利用上述仪器和药品可以制取氧气;(3)、探究性质:①实验一 (填 “能”或“不能”)得出二氧化碳密度大于空气;②实验二,溶液颜色由紫色变红色,是因为生成(填化学式);
③实验三,澄清的石灰水变浑浊,反应的化学方程式是。
 18. 取少量氢氧化钠溶液于A试管中,完成如图实验,回答下列问题。(BaCl2溶液为中性)
18. 取少量氢氧化钠溶液于A试管中,完成如图实验,回答下列问题。(BaCl2溶液为中性)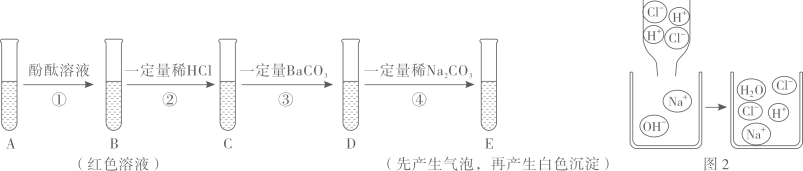 (1)、步骤②发生的反应方程式为①;图2为反应过程中的微观实质,反应中数目减少的离子是②(填符号) ;(2)、步骤③加BaCO3产生的现象有;(3)、选择下列上种试剂即可检验E中溶液除氯化钠外的溶质成分,是 。A、碳酸钠 B、稀盐酸 C、稀硫酸 D、硫酸钠19. 某同学在实验室发现上瓶标签残缺的无色溶液(如右图所示),为确认溶液中的溶质,进行如下探究活动。
(1)、步骤②发生的反应方程式为①;图2为反应过程中的微观实质,反应中数目减少的离子是②(填符号) ;(2)、步骤③加BaCO3产生的现象有;(3)、选择下列上种试剂即可检验E中溶液除氯化钠外的溶质成分,是 。A、碳酸钠 B、稀盐酸 C、稀硫酸 D、硫酸钠19. 某同学在实验室发现上瓶标签残缺的无色溶液(如右图所示),为确认溶液中的溶质,进行如下探究活动。
[提出问题]这瓶试剂可能是NaCl、NaOH、Na2CO3、NaHCO3中的一种
(1)、[查找资料]物质(20℃)
NaCl
NaOH
Na2CO3
NaHCO3
溶解度g
36
109
215
9.6
小芸根据标签和溶解度数据判断,这瓶试剂不可能是NaHCO3 , 原因是。
(2)、[实验探究]①小兵用洁净的玻璃棒蘸取试液于pH试纸上,测得pH>7,则这瓶试剂不可能是NaCl;
②小兵为了进一步检验该溶液,他取少量溶液于试管中,滴加过量的稀盐酸,观察到的现象,于是他得出结论:这瓶溶液为碳酸钠溶液。
(3)、小芸认为小兵的结论可能存在问题,她又进行如下实验:实验步骤
实验现象
结论或化学方程式
步骤1:取少量溶液于试管中,滴加过量的BaCl2溶液
产生白色沉淀
反应化学方程式①
步骤2:静置、取上层清液于另一试管,滴加CuSO4溶液
产生蓝色沉淀
原溶液中溶质成分为②
[反思交流]氢氧化钠溶液变质的原因(方程式解释)。
20. 某钢铁厂每天需消耗5000t含氧化铁76%的赤铁矿石,该厂理论上可日产含铁98%的生铁的质量是多少?(请补全下列化学方程式的计算步骤,其中找相关量及答省略)。[解] 5000t 赤铁矿石中含氧化铁的质量为: 5000t×76%==3800t
设: 3800t 氧化铁理论上可日产铁的质量是X。
Fe2O3+3CO 2Fe+3CO2
找相关量 省略
列出比例式(1)
X=2660t
折合为含铁98%的生铁的质量为: (2)(写出计算式及结果保留整数)。.