天津市和平区2023年中考二模化学试题
试卷更新日期:2023-07-03 类型:中考模拟
一、单选题
-
1. 成语是中华传统文化的瑰宝。下列成语涉及化学变化的是( )A、滴水成冰 B、钻木取火 C、绳锯木断 D、木已成舟
-
2. 下列物质中属于纯净物的是( )A、空气 B、生铁 C、赤铁矿石 D、冰水共存物
-
3. 每年的5月20日是“中国学生营养日”。处于生长发育期的青少年每天要摄入一定量的蛋类、鱼虾类、奶类等食物,这三类食物富含的基本营养素是( )A、油脂 B、糖类 C、蛋白质 D、维生素
-
4. 宏观现象的微观解释是学习化学的思维方式。下列现象的微观解释不正确的是( )A、干冰升华——分子间隔增大 B、氧气能被压入钢瓶中——分子体积变小 C、湿衣服晾干——分子不断运动 D、金刚石和石墨硬度不同——碳原子排列方式不同
-
5. 某同学用pH试纸测定了生活中一些物质的pH如下。能使酚酞溶液变红的物质是( )
物质
食醋
橘子汁
食盐水
炉具清洁剂
pH
2
4
7
12
A、食醋 B、橘子汁 C、食盐水 D、炉具清洁剂 -
6. 化学实验考查时,小芳抽到的考题是:“配制 40g 质量分数为 18%的氯化钠溶液”,她的实验操作正确的是( )A、取氯化钠固体
 B、称量 7.2g 氧化钠
B、称量 7.2g 氧化钠  C、量取 32.8mL 水
C、量取 32.8mL 水  D、玻璃棒搅拌溶解
D、玻璃棒搅拌溶解 
-
7. 下列有关实验现象的描述,正确的是( )A、硫在氧气中燃烧,产生淡蓝色火焰,生成无色无味的气体 B、镁在空气中燃烧,产生苍白色火焰,生成白色烟雾 C、红磷在空气中燃烧,发出红色的火焰,产生大量白色烟雾 D、细铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体
-
8. 我国著名科学家、中国科学院院士张青莲教授主持测定了锢、铱、锑、铕的等近十种元素的相对原子质量,为相对原子质量测定作出了卓越贡献。关于铟元素在元素周期表中的部分信息及原子结构示意图如图所示。下列说法正确的是( )
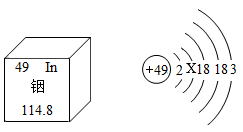 A、铟元素属于非金属元素 B、铟元素的相对原子质量是114.8g C、铟原子的质子数为49 D、铟的原子结构示意图中X=18
A、铟元素属于非金属元素 B、铟元素的相对原子质量是114.8g C、铟原子的质子数为49 D、铟的原子结构示意图中X=18 -
9. 空气是一种重要的资源。下列与空气有关的说法错误的是( )A、空气中氮气的体积分数约为78% B、稀有气体化学性质比较活泼 C、自然界中的二氧化碳处于不停循环过程中 D、工业上用分离液态空气的方法制取氧气
-
10. 在反应2A+B2=2C中,21gA和足量B2在一定条件下充分反应生成33gC,已知B的相对原子质量为16,则A的相对分子质量是( )A、26 B、28 C、30 D、32
-
11. 总结是学习化学的基本方法之一,下列总结完全正确的是( )
A.化学与健康
B.化学与安全
C.化学与生活
D.化学与环境
①六大基本营养素中只有水和无机盐不是有机物②食用腌制食品有益于健康
①可燃性气体点燃前要验纯
②精密仪器等物品失
火应使用干粉灭火器
①将煤块粉碎可增大与空气的接触面
积,反应更充分
②活性炭具有吸附
性,可作冰箱除味
剂
①大量使用化石燃料可能导致酸雨
②为减少环境污染,
禁止使用农药化肥
A、A B、B C、C D、D -
12. 下列实验方案中不能达到相应实验目的的是( )
选项
实验目的
实验方案
A
探究可燃物燃烧需要氧气
向盛有80℃热水的两只烧杯中各放入一小块白磷,然后用导管对准其中一块白磷通入氧气,观察现象
B
除去氧化钙中少量的碳酸钙
高温煅烧
C
鉴别NaCl、NaOH与NH4NO3三种固体
取等量样品,分别溶于同温等体积水中,测量溶质溶解后溶液的温度
D
检验CO2气体中是否混有HCl气体
通入紫色石蕊试液,观察溶液是否变红
A、A B、B C、C D、D
二、多选题
-
13. “价-类”二维图能反映元素的化合价与物质类别之间的关系。下图是碳元素的“价-类”二维图。下列说法不正确的是( )
 A、a=-2 B、X点对应的物质可以是金刚石或足球烯(C60) C、X、Y、M、N点对应的物质都可以通过一步反应转化为Z D、取N点对应的钠盐10.6g加入足量的稀硫酸,得到二氧化碳气体的质量一定为4.4g
A、a=-2 B、X点对应的物质可以是金刚石或足球烯(C60) C、X、Y、M、N点对应的物质都可以通过一步反应转化为Z D、取N点对应的钠盐10.6g加入足量的稀硫酸,得到二氧化碳气体的质量一定为4.4g
三、单选题
-
14. 甲、乙、丙、丁四种物质的相互反应关系如图所示(“一” 表示相连的物质间能发生反应)下列符合对应反应关系的选项是( )

选项
A
B
C
D
物质
甲
BaCl2
CO2
H2
Fe
乙
Na2CO3
NaOH
O2
HCl
丙
H2SO4
CaCl2
CuO
CuSO4
丁
Ca(OH)2
AgNO3
CO
NaOH
A、A B、B C、C D、D
四、多选题
-
15. 下列说法正确的是( )A、等质量的镁与氧化镁混合,其混合物中镁、氧两种元素的质量比为5:2 B、铁和锌的混合物6g与足量的稀盐酸反应,生成氢气的质量不可能为0.2g C、用含杂质(杂质不与酸反应,也不溶于水)的铁10g和50g稀硫酸完全反应后,滤去杂质,所得液体质量为55.4g,则含杂质的铁中铁的质量分数为56% D、现有氧化铜和氧化铁的混合物10g与100g溶质质量分数为14.7%的稀硫酸恰好完全反应,则混合物中氧元素的质量分数为24%
五、填空题
-
16. 化学就在我们身边。现有①氧气②甲烷③熟石灰④氯化钠⑤氢氧化钠⑥碳酸氢钠,选择适当的物质填空(填序号)。(1)、天然气的主要成分是;(2)、可用于炼钢、气焊的是;(3)、发酵粉的主要成分之一是;(4)、农业上可用其溶液来选种的是;(5)、建筑上常与沙子混合来砌墙的是;(6)、其固体可作为某些气体干燥剂的是。
-
17. 每年的3月22日是“世界水日”,水与人类的生产、生活密切相关。(1)、地下水是重要水源。雨水经过种植土层和砂层能得到净化,还能补给地下水。种植土层和砂层在净化水的过程中所起的作用是。(2)、目前部分农村的饮用水主要取自地下水。通常地下水的硬度较大,长期饮用会危害人体健康,生活中降低水的硬度常用的方法是。若地下水中有异味,可利用活性炭的性去除。(3)、如图是电解水实验的示意图,反应一段时间后a、b试管中产生气体的体积比约为。
 (4)、节约用水和保护水资源是每个公民应尽的责任和义务。下列说法中符合这一认识的是______(填字母序号)。A、农业生产中过度使用农药和化肥 B、淡水可以取之不尽、用之不竭 C、洗菜、淘米的水用来浇花 D、工业废水处理达标后再排放
(4)、节约用水和保护水资源是每个公民应尽的责任和义务。下列说法中符合这一认识的是______(填字母序号)。A、农业生产中过度使用农药和化肥 B、淡水可以取之不尽、用之不竭 C、洗菜、淘米的水用来浇花 D、工业废水处理达标后再排放 -
18. 在宏观、微观和符号三者之间建立联系是化学特有的思维方式。(1)、下图中,X是。
 (2)、写出一个通过化合反应生成二氧化碳的方程式。(3)、下图①②是硼和铝元素在周期表中的信息,③~⑥分别为四种粒子的结构示意图,请回答下列问题。
(2)、写出一个通过化合反应生成二氧化碳的方程式。(3)、下图①②是硼和铝元素在周期表中的信息,③~⑥分别为四种粒子的结构示意图,请回答下列问题。
a.⑥表示带一个单位负电荷的某离子结构示意图,则=。
b.③和⑤两种粒子化学性质相似的原因是。
c.④和⑥形成的化合物的化学式是。
d.观察上图,以下说法正确的是(填字母)。
A.相对原子质量铝比硼多8 B.③在化学反应中易得到电子
C.④对应的单质是由原子构成的 D.①-⑥中共有三种金属元素
e.下图是某反应的微观示意图

根据图示写出反应的化学方程式。
-
19. 完成下列反应的化学方程式(1)、硫在氧气中燃烧的反应。(2)、实验室制氢气最常用的方法。(3)、双氧水制氧气的方程式。
-
20. A、B、C三种固体物质的溶解度曲线如下图所示。请回答下列问题:
 (1)、P点的含义是。(2)、t2℃时,70gA物质的饱和溶液中溶质的质量是g。(3)、将C物质的不饱和溶液转化为饱和溶液,可采用的方法是(写出一种方法即可)。(4)、将t1℃时等质量的A、B、C三种物质的饱和溶液分别升温到t2℃(忽略水分的蒸发),所得溶液的质量大小关系是。(5)、某同学欲配制120g质量分数为10%的氯化钠溶液。请回答下列问题:
(1)、P点的含义是。(2)、t2℃时,70gA物质的饱和溶液中溶质的质量是g。(3)、将C物质的不饱和溶液转化为饱和溶液,可采用的方法是(写出一种方法即可)。(4)、将t1℃时等质量的A、B、C三种物质的饱和溶液分别升温到t2℃(忽略水分的蒸发),所得溶液的质量大小关系是。(5)、某同学欲配制120g质量分数为10%的氯化钠溶液。请回答下列问题:
a.需称取氯化钠的质量为g。
b.图示实验中,正确的操作顺序为(填序号)。
c.若量取水的体积时仰视读数,其他操作均正确,则所配制溶液的溶质质量分数(选填“偏大”、“偏小”或“无影响”)。
d.欲配制60g质量分数为5%的氯化钠溶液,需要10%的氯化钠溶液的质量为g。
六、推断题
-
21. A~K为初中化学常见的物质,它们之间有如下图所示的转化和反应关系(部分反应物、生成物及反应条件已略去),其中常温下B、C、D、H为气体,①②分别为植物的呼吸作用和光合作用,④为侯氏制碱法的一个反应,固体E在C中点燃生成黑色磁性固体,G为白色固体,F是常见的液体。

回答下列问愿:
(1)、A的化学式为。(2)、物质K是属于(填“酸”“碱”“盐”或“氧化物”)。(3)、A→G反应的化学方程式为。(4)、G与J反应的化学方程式为(任写一个)。
七、实验题
-
22. 实验中,可以根据反应物的状态和反应类型选择相同的装置制取不同气体,根据下列图示回答问题:
 (1)、图中①的名称是。(2)、实验室用过氧化氢和二氧化锰制取氧气,可以选择(用A~F填空)作为发生装置。该装置还可以用于制取二氧化碳气体,写出实验室用稀盐酸和大理石制取二氧化碳的化学方程式:。制取得到的CO2气体中往往含有HCl杂质可以选用装置F除去,除杂时气体应从(填“a”或“b)端通入。(3)、以上装置中可同时用于实验室收集O2和CO2的是(A~F填空)。
(1)、图中①的名称是。(2)、实验室用过氧化氢和二氧化锰制取氧气,可以选择(用A~F填空)作为发生装置。该装置还可以用于制取二氧化碳气体,写出实验室用稀盐酸和大理石制取二氧化碳的化学方程式:。制取得到的CO2气体中往往含有HCl杂质可以选用装置F除去,除杂时气体应从(填“a”或“b)端通入。(3)、以上装置中可同时用于实验室收集O2和CO2的是(A~F填空)。
八、填空题
-
23. 丰富多彩的中华文物铭刻着中华文化的脉络、记录着中华文明的传承。(1)、认识文物:青铜是铜与锡的合金。青铜硬度(填“大于”或“小于”)钝铜。(2)、文物锈蚀:汉代铁剪锈迹斑斑,其锈蚀是铁与空气中的发生化学反应的结果。(3)、金属冶炼:利用CO与Fe2O3反应炼铁,反应的化学方程式为。(4)、铜用作导线主要利用铜良好的延展性和性。(5)、我国是世界上最早使用湿法炼铜的国家,其主要原理是将铁放入硫酸铜溶液中把铜置换出来,该反应的化学方程式为 , 铁与硫酸铜恰好完全反应时,反应前后溶液中未发生改变的主要微粒是。(6)、现有一包由5.6g铁、7.2g镁、1.4g碳混合而成的粉末,把它加入一定量的Cu(NO3)2溶液中,实验结束后,测得剩余固体中含有三种物质。则剩余固体的质量可能是______。A、24.8g B、26.2g C、26.8g D、27g
-
24. 天然气广泛应用于生产生活,其主要成分是甲烷(CH4)。(1)、三大化石燃料包括:煤、、天然气。(2)、室温下,充分燃烧1g天然气和1g煤,产生的CO2及热量的对比如图所示。据图分析,与煤相比,用天然气作燃料的优点有。
 (3)、甲烷和二氧化碳在高温下催化重整(Ni作催化剂)可制得CO和H2 , 该反应的化学方程式为。(4)、一定质量的甲烷在不充足的氧气中燃烧,甲烷完全反应,生成物只有CO、CO2和H2O,且总质量为20.8g,其中H2O的质量为10.8g,则CO的质量为g。
(3)、甲烷和二氧化碳在高温下催化重整(Ni作催化剂)可制得CO和H2 , 该反应的化学方程式为。(4)、一定质量的甲烷在不充足的氧气中燃烧,甲烷完全反应,生成物只有CO、CO2和H2O,且总质量为20.8g,其中H2O的质量为10.8g,则CO的质量为g。
九、计算题
-
25. 中国空间站“天宫课堂”完成泡腾片趣味性实验,泡腾片放入水中产生大量的气泡,气泡不会从太空水球中冒出。泡腾片中含有柠檬酸(化学式为C6H8O7)。(1)、柠檬酸中含种元素。(2)、柠檬酸中碳元素和氢元素的质量比是(填最简整数比)。(3)、9.6g柠檬酸与g乙醇中含碳元素质量相等。
-
26. 纯碱样品中含有少量的氯化钠,某同学为测定该纯碱样品中碳酸钠的含量,他取该纯碱样品6g,全部溶解在100g水中,再加入104g溶质质量分数为10%的氯化钡溶液,恰好完全反应,过滤,所得溶液为不饱和溶液(不考虑过程中物质质量的损失)。请计算:(1)、纯碱样品中氯化钠的质量分数;(计算结果保留到0.1%)(2)、反应后所得溶液中溶质的质量分数(计算结果保留到0.1%)。
