四川省泸州市泸县2023年中考二模化学试题
试卷更新日期:2023-07-03 类型:中考模拟
一、单选题
-
1. 化学与生产生活密切相关。下列说法错误的是( )A、pH<5.6的降雨称为酸雨 B、石油属于可再生能源 C、PM2.5属于大气污染物 D、铝合金的硬度比纯铝大2. 中国文化源远流长很多成语、俗语、诗词中蕴含着丰富的科学道理。下列用化学观点解释错误的是( )A、“冰,水为之,而寒于水”——物质的状态不同,化学性质不同 B、“真金不怕火炼”——黄金高温下也不与氧气反应 C、“遥知不是雪,为有暗香来”——分子在不断运动 D、“人要实,火要虚”——增加可燃物与氧气的接触面积,可燃物燃烧得更旺3. 下列生活中的做法正确的是( )A、档案和精密仪器起火,用水来灭火 B、被蚊虫叮咬后,涂硫酸减轻痛痒 C、自行车链条喷漆防锈 D、用加入洗涤剂的水洗掉餐具上的油污4. 侯氏制碱法为NaCl+NH3+H2O+CO2=X+NH4Cl。下列说法不正确的是( )A、NaCl可由海水蒸发结晶后精制获得 B、CO2可由海边的贝壳煅烧获得 C、X为Na2CO3 , 可治疗胃酸过多 D、NH4Cl可作化肥,不能与草木灰混合施用5. 某同学绘制了含铁元素的部分物质转化关系图(图中“→”表示一种物质可以转化为另一种物质,部分反应物、生成物及反应条件已略去),下列说法不正确的是( )
 A、铁丝能在空气中剧烈燃烧实现转化① B、转化②可通过Fe3O4与CO发生反应实现 C、氧气和水同时存在是实现转化③的必备条件 D、通过Fe与CuSO4溶液反应可实现转化④6. 下列实验操作或实验方案中,不能达到实验目的是实验目的实验操作或实验方案( )
A、铁丝能在空气中剧烈燃烧实现转化① B、转化②可通过Fe3O4与CO发生反应实现 C、氧气和水同时存在是实现转化③的必备条件 D、通过Fe与CuSO4溶液反应可实现转化④6. 下列实验操作或实验方案中,不能达到实验目的是实验目的实验操作或实验方案( )实验目的
实验操作或实验方案
A
鉴别硬水和软水
分别加入肥皂水,振荡
B
除去CaCl2溶液中的HCl
加入过量碳酸钙,充分反应后过滤
C
除去粗盐水中的Mg2+、Ca2+、 , 得到精盐水
依次加入过量的BaCl2溶液、Na2CO3溶液、NaOH溶液,充分反应后过滤
D
制取玻璃
选择石灰石、石英砂和纯碱作为原料
A、A B、B C、C D、D7. 《本草纲目》记载“冬月灶中所烧薪柴之灰。令人以灰淋汁,取碱浣衣”。下列叙述不正确的是( )A、“烧”涉及氧化反应 B、“灰”指草木灰,含有碳酸钾 C、“灰淋汁”涉及溶解 D、“取碱浣(洗)衣”利用碱的腐蚀性8. 60℃时,向100g水中加入一定量KNO3形成溶液,再降温至20℃,析出固体质量的变化如图1。结合图2,下列说法正确的是( ) A、加入的KNO3质量为31.6g B、降温过程中KNO3溶液由不饱和溶液变为饱和溶液 C、蒸发溶剂可将M点的溶液转化到N点 D、20℃时,100g KNO3饱和溶液中有KNO331.6g
A、加入的KNO3质量为31.6g B、降温过程中KNO3溶液由不饱和溶液变为饱和溶液 C、蒸发溶剂可将M点的溶液转化到N点 D、20℃时,100g KNO3饱和溶液中有KNO331.6g二、填空题
-
9. 在宏观、微观和符号之间建立联系是化学学科的重要思维方式。(1)、根据图示信息判断,下列说法正确的是______(填序号)。A、硫属于金属元素 B、硫原子中的质子数为16 C、硫的相对原子质量为32.06g(2)、根据下列粒子的结构示意图,回答问题。


①图中粒子共表示种元素(填数字)。
②A为氯原子的结构示意图,与氯原子的化学性质最相似的是(填序号)。
10. 《本草纲目》记载:“杨桃具有去风热、生津止渴等功效”。下表列出的是某杨桃每100g可食用部分的主要营养成分数据。请结合所学知识完成下列问题:营养成分
水
糖类
X
脂肪
钾、钙、锌、铁
维生素
…
质量
84.8g
10.3g
0.7g
0.6g
187.4mg
62.2mg
…
(1)、表中“X”是指六大营养素中的。(2)、表中列出的属于人体中必需的微量元素的是。(3)、经测定杨桃A的pH=1.35,杨桃B的pH=1.81,其中酸性较强的杨桃是(填“A”或“B”)。(4)、杨桃中维生素有多种,人体内缺乏维生素A会引起________(填字母序号)。A、坏血病 B、氟骨病 C、甲状腺肿大 D、夜盲症(5)、为增强杨桃树的抗旱抗寒能力,可以追施(填“氮”“磷”或“钾”)肥。11. 千年泸县,宋韵龙城。泸县屈氏庄园内的白墙、青砖、黛瓦展现了传统民居文化的繁华。(1)、《天工开物》中介绍了烧制青砖的方法,其中载有“灌水其上”、“水火既济”。相关反应为水蒸气与灼热的碳生成CO和一种气体单质,气体单质的化学式为。(2)、古代建筑工匠常用糯米灰浆黏合墙砖,糯米灰浆由糯米汁、熟石灰和砂土等混合而成。糯米灰浆属于(填“复合材料”或“金属材料”),熟石灰在空气中最终转化为(填化学式)。(3)、“帘外芭蕉惹骤雨,门外惹铜绿”。铜绿[主要成分是Cu2(OH)2CO3]是铜发生一系列复杂反应的产物,空气中参与该反应过程的物质有(填化学式)和O2。12. 能源不可或缺。(1)、Ⅰ、能源的转化和储存:祝融号火星车上安装的太阳能板能将太阳能转化为能,为科学仪器供电。(2)、反应器中初始反应是甲烷和水蒸气在催化剂并加热的条件下反应生成H2和CO2 , 化学方程式是。(3)、反应器中还存在如下反应:ⅰ;ⅱ;ⅲ
已知:s表示该物质为固态;H2中混有CO不易被除去。
①上述三个反应中化合价均有变化的元素有(填元素符号)。
②通过调控反应条件,使i中生成的CO在ii中全部转化,目的是。
(4)、用CaO可以除去反应器中的CO2 , CaO消耗率随时间变化关系如图所示。从t开始,单位时间内CaO消耗率(填“升高”“降低”或“不变”)。 (5)、CO2也可用NaOH溶液吸收,但却观察不到明显现象。请设计实验证明NaOH溶液吸收了CO2 , 简述实验过程(包括操作和现象)。
(5)、CO2也可用NaOH溶液吸收,但却观察不到明显现象。请设计实验证明NaOH溶液吸收了CO2 , 简述实验过程(包括操作和现象)。三、科学探究题
-
13. 用如图装置对镁及其化合物的性质进行实验探究。

步骤一:将打磨过的镁条放入三颈烧瓶中,关闭K1、打开K2 , 加入一定量饱和NH4Cl 溶液,观察到镁条溶解,形成无色溶液,产生大量气泡。试管B中石蕊试纸变为蓝色。点燃E处气体产生淡蓝色火焰。
(1)、点燃E处气体前,必须进行的操作是。(2)、镁条与NH4Cl溶液反应的化学方程式为:Mg+2NH4Cl=+2NH3↑+H2↑。步骤二:已知:NH3+H2O=NH3·H2O。打开K1 , 通入少量NH3观察到溶液变浑浊。过滤、洗净、低温烘干得白色固体。
(3)、①某同学猜想此白色固体是Mg(OH)2 , 理由是(用化学方程式表示)。(4)、取少量白色固体,溶于适量的稀硝酸,再滴加AgNO3溶液,观察到 , 则该同学猜想不正确。资料:此白色固体为碱式氯化镁[Mgx(OH)yClz],其不溶于水,能与酸反应,加热分解生成MgO、H2O和HCl。
步骤三:
(5)、取一定量白色固体,充分加热,残留 2.40g 固体,将生成的气体用足量的AgNO3溶液吸收,生成5.74g沉淀。则白色固体中镁元素和氯元素的质量比为。四、科普阅读题
-
14. 如图是人类对氧化还原反应的认识过程中的三个阶段。
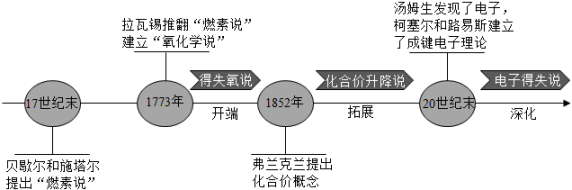
【阶段Ⅰ】得失氧说:物质跟氧发生的反应叫氧化反应,含氧化合物中的氧被夺取的反应叫还原反应。
【阶段Ⅱ】化合价升降说:凡是出现元素化合价升降的化学反应都是氧化还原反应。化合价升高的反应叫氧化反应,化合价降低的反应叫还原反应。
【阶段Ⅲ】电子转移说:化合价升降的原因是电子的转移。凡有电子转移发生的化学反应都是氧化还原反应。失电子的反应叫氧化反应,得电子的反应叫还原反应。
(1)、根据得失氧说,在H2+CuOCu+H2O化学变化中,H2发生了反应。(2)、电子转移是元素化合价改变的本质原因。失电子后,元素的化合价会(选填“升高”或“降低”)。(3)、根据化合价升降说,化学反应的四种基本类型与氧化还原反应之间的关系如图所示,其中乙是反应。 (4)、关于氧化还原反应的认识,下列理解正确的是______。A、氧化和还原是相互对立又辩证统一的关系 B、电子转移说是从微观视角来探析和建构氧化还原反应的概念 C、自然界中发生的氧化还原反应对人类的生活和生产都是有利的 D、人类对氧化还原反应的认识过程是一个逐步发展、延伸和完善的过程
(4)、关于氧化还原反应的认识,下列理解正确的是______。A、氧化和还原是相互对立又辩证统一的关系 B、电子转移说是从微观视角来探析和建构氧化还原反应的概念 C、自然界中发生的氧化还原反应对人类的生活和生产都是有利的 D、人类对氧化还原反应的认识过程是一个逐步发展、延伸和完善的过程五、流程题
-
15. 某学习小组利用锈蚀严重的废铜屑(铜锈的主要成分是碱式碳酸铜[Cu2(OH)2CO3])为原料回收铜,分别采用图1的两种方案。请回答下列问题。
资料1:
资料2:回收铜的两种实验方案。
 (1)、方案一中步骤Ⅱ生成的二氧化碳不能直接排放到空气中,需要将其回收后再与碳粉作用,又可以生成CO,写出该过程的化学反应方程式:。(2)、方案二中步骤Ⅲ、Ⅳ、V都涉及到的操作名称是 , 该操作所需的玻璃仪器有:玻璃棒、烧杯和。(3)、方案二中步骤Ⅳ加入过量铁粉的目的是 , 该反应是利用铁的金属活动性比铜的(填“强”或“弱”)。(4)、理论上等质量的废铜屑通过两种方案获得铜的质量比较:方案一方案二(选填“>、=、<”)。(5)、图2为铜元素的价类转化二维图,写出D点对应物质的化学式。步骤Ⅳ实现的是E→点(填字母)的转化。
(1)、方案一中步骤Ⅱ生成的二氧化碳不能直接排放到空气中,需要将其回收后再与碳粉作用,又可以生成CO,写出该过程的化学反应方程式:。(2)、方案二中步骤Ⅲ、Ⅳ、V都涉及到的操作名称是 , 该操作所需的玻璃仪器有:玻璃棒、烧杯和。(3)、方案二中步骤Ⅳ加入过量铁粉的目的是 , 该反应是利用铁的金属活动性比铜的(填“强”或“弱”)。(4)、理论上等质量的废铜屑通过两种方案获得铜的质量比较:方案一方案二(选填“>、=、<”)。(5)、图2为铜元素的价类转化二维图,写出D点对应物质的化学式。步骤Ⅳ实现的是E→点(填字母)的转化。 (6)、碱式碳酸铜和碳酸铜混合物11.8g,与100g9.8%的稀硫酸刚好完全反应,得到的溶液通过方案二中的步骤IV和步骤V,最终能够得到铜g(不需要写出计算过程)。
(6)、碱式碳酸铜和碳酸铜混合物11.8g,与100g9.8%的稀硫酸刚好完全反应,得到的溶液通过方案二中的步骤IV和步骤V,最终能够得到铜g(不需要写出计算过程)。
-
-