浙江省温州市2022-2023学年高一上学期1月期末考试化学试题
试卷更新日期:2023-06-21 类型:期末考试
一、单选题
-
1. 下列物质属于碱性氧化物的是A、 B、 C、 D、2. 钠在空气中燃烧的实验,下列不需要的仪器是A、
 B、
B、 C、
C、 D、
D、 3. 下列分散系能产生“丁达尔效应”的是A、稀盐酸 B、氢氧化铁胶体 C、泥浆 D、硫酸铜溶液4. 下列物质属于电解质且能导电的是A、盐酸 B、氯化钠固体 C、熔融氢氧化钠 D、铁丝5. 下列物质对应的化学式不正确的是A、纯碱: B、磁性氧化铁: C、硫黄: D、石膏:6. 反应中,氧化剂是A、 B、 C、 D、7. 下列说法不正确的是A、钾离子的结构示意图:
3. 下列分散系能产生“丁达尔效应”的是A、稀盐酸 B、氢氧化铁胶体 C、泥浆 D、硫酸铜溶液4. 下列物质属于电解质且能导电的是A、盐酸 B、氯化钠固体 C、熔融氢氧化钠 D、铁丝5. 下列物质对应的化学式不正确的是A、纯碱: B、磁性氧化铁: C、硫黄: D、石膏:6. 反应中,氧化剂是A、 B、 C、 D、7. 下列说法不正确的是A、钾离子的结构示意图: B、的分子结构模型:
B、的分子结构模型: C、甲烷的结构式:
C、甲烷的结构式: D、用电子式表示的形成过程:
D、用电子式表示的形成过程: 8. 航天器“天问一号”成功着陆火星,实现我国在深空探测领域的技术跨越。此次探测由核素提供能量,已知属于过渡元素。下列说法不正确的是A、是一种金属元素 B、、、互为同位素 C、、、的化学性质有很大不同 D、原子核内中子数与核外电子数之差为559. 下列说法不正确的是A、中存在离子键和非极性共价键 B、汽化时必须破坏分子间的氢键 C、溶于水的过程中破坏了离子键 D、中每个原子最外电子层都具有8电子稳定结构10. 常温下,在指定溶液中下列各组离子一定能大量共存的是A、强碱性溶液中:、、、 B、强酸性溶液中:、、、 C、溶液中:、、、 D、溶液中:、、、11. 下列说法不正确的是A、氢氧化铁胶体作为自来水的消毒剂 B、过氧化钠在呼吸面具或潜水艇中可作为氧气的来源 C、氯化铁溶液在工业上可作为制作印刷电路板的“腐蚀液” D、二氧化硫可作为食品加工中的抗氧化剂12. 下列相关说法正确的是A、生活中常用碳酸氢钠作膨松剂烘焙面包,因为碳酸氢钠溶液呈碱性 B、生活中常将“84消毒液”和洁厕灵(主要成分为盐酸)混合使用,为了增强去污效果 C、工业上常用铬酸氧化法对金属铝表面处理,为了增加表面厚度 D、实验里通常将转化后的难溶物或含有重金属的固体废渣,直接倒入废液缸13. 下列说法正确的是A、稀硝酸可用铝罐车运输 B、金属锂和钠保存在煤油中 C、氯水保存在棕色广口瓶中,置于阴凉干燥处 D、硫酸亚铁溶液保存时需加入少量铁粉14. 现代社会的发展与进步离不开材料。下列有关说法不正确的是( )。A、碳化硅是一种新型陶瓷材料,具有耐高温耐磨的特点 B、晶体硅是一种半导体材料,常用于制造光导纤维 C、硬铝是一种铝合金,是制造飞机和飞船的理想材料 D、石墨烯是一种新型无机非金属材料,具有高电导率的特点15. 为除去括号内少量的杂质,所用的试剂或方法正确的是A、粉:氢氧化钠溶液,过滤 B、气体:饱和亚硫酸钠溶液 C、气体:蒸馏水 D、粉末:加热16. 某实验兴趣小组配制溶液,部分操作如图所示:
8. 航天器“天问一号”成功着陆火星,实现我国在深空探测领域的技术跨越。此次探测由核素提供能量,已知属于过渡元素。下列说法不正确的是A、是一种金属元素 B、、、互为同位素 C、、、的化学性质有很大不同 D、原子核内中子数与核外电子数之差为559. 下列说法不正确的是A、中存在离子键和非极性共价键 B、汽化时必须破坏分子间的氢键 C、溶于水的过程中破坏了离子键 D、中每个原子最外电子层都具有8电子稳定结构10. 常温下,在指定溶液中下列各组离子一定能大量共存的是A、强碱性溶液中:、、、 B、强酸性溶液中:、、、 C、溶液中:、、、 D、溶液中:、、、11. 下列说法不正确的是A、氢氧化铁胶体作为自来水的消毒剂 B、过氧化钠在呼吸面具或潜水艇中可作为氧气的来源 C、氯化铁溶液在工业上可作为制作印刷电路板的“腐蚀液” D、二氧化硫可作为食品加工中的抗氧化剂12. 下列相关说法正确的是A、生活中常用碳酸氢钠作膨松剂烘焙面包,因为碳酸氢钠溶液呈碱性 B、生活中常将“84消毒液”和洁厕灵(主要成分为盐酸)混合使用,为了增强去污效果 C、工业上常用铬酸氧化法对金属铝表面处理,为了增加表面厚度 D、实验里通常将转化后的难溶物或含有重金属的固体废渣,直接倒入废液缸13. 下列说法正确的是A、稀硝酸可用铝罐车运输 B、金属锂和钠保存在煤油中 C、氯水保存在棕色广口瓶中,置于阴凉干燥处 D、硫酸亚铁溶液保存时需加入少量铁粉14. 现代社会的发展与进步离不开材料。下列有关说法不正确的是( )。A、碳化硅是一种新型陶瓷材料,具有耐高温耐磨的特点 B、晶体硅是一种半导体材料,常用于制造光导纤维 C、硬铝是一种铝合金,是制造飞机和飞船的理想材料 D、石墨烯是一种新型无机非金属材料,具有高电导率的特点15. 为除去括号内少量的杂质,所用的试剂或方法正确的是A、粉:氢氧化钠溶液,过滤 B、气体:饱和亚硫酸钠溶液 C、气体:蒸馏水 D、粉末:加热16. 某实验兴趣小组配制溶液,部分操作如图所示:
下列说法正确的是
A、称量时,将称量纸放置于电子天平并归零,然后称取固体 B、溶解后,立即将溶液转移至容量瓶 C、定容时,若俯视刻度线,则所配溶液浓度偏高 D、摇匀装瓶后,容量瓶应洗净、晾干,并直接盖上瓶塞下次备用17. 下列离子方程式正确的是A、与水反应: B、与水溶液反应: C、向稀硝酸中投入少量铁片: D、氢氧化钠溶液与过量碳酸氢钙溶液反应:18. 下列“类比”合理的是A、与反应生成和 , 则与反应生成和 B、与反应生成 , 则与反应生成 C、常温下,的溶解度比的大,则的溶解度比的大 D、与反应生成和 , 则与反应生成和19. a、b、c、d、e均为短周期主族元素,其最高正化合价或最低负化合价与原子序数的关系如图所示。下列说法正确的是 A、d的原子半径比e的小 B、常温下,c单质不与b单质反应 C、与d元素同主族的下一周期元素的单质可作为半导体材料 D、a与b元素形成的化合物仅含有极性键20. 化学与职业息息相关,下列化学职业有关说法不正确的是A、科技考古人员在研究文物和古迹时,可利用的测定分析古代人类的食物结构 B、测试工程师可运用各类高精度化学检测仪器或化学检测方法,以获得金属材料的组成及含量 C、化学科研工作者可从事特定功能新分子合成、安全高效和节能环保物质转化工艺的研发等 D、水质检测员需要在自来水出厂前,需要对其中的、放射性物质、微生物和有机物等进行检测21. 下列实验、描述与结论正确的是
A、d的原子半径比e的小 B、常温下,c单质不与b单质反应 C、与d元素同主族的下一周期元素的单质可作为半导体材料 D、a与b元素形成的化合物仅含有极性键20. 化学与职业息息相关,下列化学职业有关说法不正确的是A、科技考古人员在研究文物和古迹时,可利用的测定分析古代人类的食物结构 B、测试工程师可运用各类高精度化学检测仪器或化学检测方法,以获得金属材料的组成及含量 C、化学科研工作者可从事特定功能新分子合成、安全高效和节能环保物质转化工艺的研发等 D、水质检测员需要在自来水出厂前,需要对其中的、放射性物质、微生物和有机物等进行检测21. 下列实验、描述与结论正确的是 A、图①,在电流作用下熔融氯化钠中和发生电离和定向移动,故使灯泡发亮 B、图②,将胶头滴管中的水挤入金属钠中,红墨水右移,不能证明钠与水是放热反应 C、图③,将干燥的氯气依次通过装有干燥红纸条、湿润红纸条的广口瓶,不能证明氯气与水发生了反应 D、图④,往与浓硫酸反应后的溶液中直接加水,可观察到溶液呈蓝色22. 设为阿伏加德罗常数的值,下列说法正确的是A、固体中含离子总数为 B、标况下,与混和气体中含有中子数为 C、与足量盐酸反应生成 , 转移的电子数为 D、(分子结构:
A、图①,在电流作用下熔融氯化钠中和发生电离和定向移动,故使灯泡发亮 B、图②,将胶头滴管中的水挤入金属钠中,红墨水右移,不能证明钠与水是放热反应 C、图③,将干燥的氯气依次通过装有干燥红纸条、湿润红纸条的广口瓶,不能证明氯气与水发生了反应 D、图④,往与浓硫酸反应后的溶液中直接加水,可观察到溶液呈蓝色22. 设为阿伏加德罗常数的值,下列说法正确的是A、固体中含离子总数为 B、标况下,与混和气体中含有中子数为 C、与足量盐酸反应生成 , 转移的电子数为 D、(分子结构: )中的共价键数目为
23. 下列物质间的转化(条件已省略),不能一步实现的是A、 B、 C、 D、24. 以高硫铝土矿(主要成分为、、和少量)为原料,生产氧化铝并获得的部分工艺流程如下:
)中的共价键数目为
23. 下列物质间的转化(条件已省略),不能一步实现的是A、 B、 C、 D、24. 以高硫铝土矿(主要成分为、、和少量)为原料,生产氧化铝并获得的部分工艺流程如下:
下列有关说法不正确的是
A、步骤①,焙烧的目的是将转化为 B、步骤②,控制适当反应温度并不断搅拌,有利于提高铝、硅浸取率 C、步骤③,滤液中主要存在的阳离子有、 D、步骤④,焙烧的反应为:25. 下列实验操作、现象和结论不正确的是选项
实验操作和现象
结论
A
取洁净的铂丝蘸取某溶液,在煤气灯外焰上灼烧,火焰呈黄色
说明溶液中含 , 不确定是否含
B
用湿润的淀粉KI试纸检验某气体,试纸变蓝色
说明该气体为
C
取少量某溶液,加入盐酸酸化,无明显现象后,再滴加溶液,产生白色沉淀
说明溶液中含
D
向碳酸钠粉末中加入少量水,碳酸钠结块变成晶体,并伴有温度升高
说明该过程放热
A、A B、B C、C D、D二、填空题
-
26. 回答下列问题:(1)、写出“钡餐”的化学式。(2)、写出在水中的电离方程式。(3)、写出的电子式。(4)、已知与水反应能生成两种强酸,则与足量溶液反应的化学反应方程式。
三、实验题
-
27. 为探究固体X(仅含两种元素)的组成和性质,设计并完成如下实验:

已知溶液B仅含一种溶质,气体C的摩尔质量为。请回答:
(1)、组成固体X的两种元素为。(2)、固体X与适量稀硫酸反应的离子方程式为。(3)、白色沉淀在空气中灼烧的化学方程式为。(4)、气体C和按物质的量之比1:4通入水中恰好完全反应。请设计实验检验产物的阴离子。28. 某兴趣小组在实验室用下图装置(夹持仪器已省略)制备无水。
已知:易潮解,300℃左右时升华。请回答:
(1)、仪器Ⅰ的名称:为了更好地收集 , 装置E应采用水浴(填“热”或“冷”)。(2)、本实验合理的操作步骤:按上图连接仪器→。(按操作顺序选择序号)。①添加药品 ②检查装置气密性 ③点燃A处酒精灯 ④点燃D处酒精灯 ⑤使D中硬质玻璃管内充满黄绿色气体
(3)、将上图中装置组装完整,虚框F应选用。 (4)、为了保证仪器Ⅰ中液体顺利流下,应采用的操作是。(5)、反应结束后,在硬质玻璃管中有固体残留,同学们进行如下实验探究,你认为正确的是_______。A、取少量固体加水溶解,若不能溶解,则说明有铁残留 B、取少量固体加水溶解,若全部溶解,则说明无铁残留 C、取少量固体溶于足量的盐酸,先滴加3滴KSCN溶液,若溶液呈血红色,则说明只有氯化铁残留 D、取少量固体溶于水中,先滴加3滴KSCN溶液无明显现象,再滴加少量新制氯水溶液呈血红色,则说明铁、氯化铁都有残留
(4)、为了保证仪器Ⅰ中液体顺利流下,应采用的操作是。(5)、反应结束后,在硬质玻璃管中有固体残留,同学们进行如下实验探究,你认为正确的是_______。A、取少量固体加水溶解,若不能溶解,则说明有铁残留 B、取少量固体加水溶解,若全部溶解,则说明无铁残留 C、取少量固体溶于足量的盐酸,先滴加3滴KSCN溶液,若溶液呈血红色,则说明只有氯化铁残留 D、取少量固体溶于水中,先滴加3滴KSCN溶液无明显现象,再滴加少量新制氯水溶液呈血红色,则说明铁、氯化铁都有残留四、元素或物质推断题
-
29. 已知短周期元素W、X、Y、Z、M、Q和R在周期表中的相对位置如下所示。

请填写下列空白:
(1)、元素Q在周期表中的位置为 , 元素Y的原子结构示意图:。(2)、下列说法不正确的是_______。A、常温时,X单质能与水发生剧烈反应 B、气态氢化物的稳定性: C、最高价氧化物对应水化物的酸性: D、M、R和W元素形成的化合物一定是共价化合物(3)、X、Z、M元素的原子半径由大到小的顺序为(用元素符号表示)。(4)、已知R的单质可将碱性工业废水中的ZM-氧化生成两种无毒物质(其中一种是气体),相应的离子方程式为。五、计算题
-
30. 为确定混合均匀的和样品组成,称取4份不同质量的样品分别加入50.0mL相同浓度的溶液中,加热充分反应(溶液中的铵根离子全部转化为氨气,且加热后氨气全部逸出)。加入样品的质量和产生的气体体积( , 标准状况)的关系如下图:
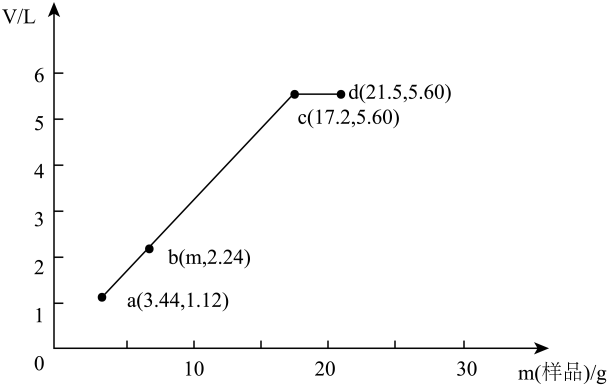
试计算:
(1)、 g。(2)、 。(3)、样品中和物质的量之比为。
-
-