四川省内江市2022-2023学年高一上学期期末考试化学试题
试卷更新日期:2023-06-21 类型:期末考试
一、单选题
-
1. 化学与生活息息相关。下列关于各“剂”在应用过程中的说法错误的是( )A、小苏打可作制糕点的“膨松剂” B、“84消毒液”可作新冠肺炎病毒的“消毒剂” C、活性铁粉在食品袋中作“抗氧剂” D、烧碱可作胃酸过多的“中和剂”2. 下列有关化学用语表述正确的是( )A、氢氧化钠的电子式:
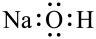 B、质子数为29,中子数为34的铜原子符号:
C、的结构式:O-C-O
D、的结构示意图:
B、质子数为29,中子数为34的铜原子符号:
C、的结构式:O-C-O
D、的结构示意图: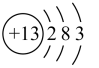 3. 分类是学习和研究化学的一种重要方法。下列物质分类合理的是( )
3. 分类是学习和研究化学的一种重要方法。下列物质分类合理的是( )选项
碱性氧化物
离子化合物
纯净物
电解质
①
稀硫酸
②
液氯
③
胶体
④
盐酸
A、① B、② C、③ D、④4. 下列说法正确的是( )A、水中含有氢分子和氧分子 B、的摩尔质量是 C、常温常压下,体积为 D、溶液中的浓度为5. 下列说法错误的是( )A、青铜属于合金材料,硬度比纯铜小,熔点比纯铜高 B、少量金属钠着火,可用干燥沙土覆盖灭火 C、在氧气中,铷的燃烧产物比钢的燃烧产物更复杂 D、用激光笔照射胶体,可观察到一条光亮的通路6. 下列叙述不正确的是( )A、Na、Mg、Al元素最高化合价依次升高 B、Li、Na、K元素的金属性依次增强 C、P、S、Cl元素最高价氧化物对应的水化物酸性依次增强 D、N、O、F原子的半径依次增大7. 常温下,下列各组离子能在指定溶液中大量共存的是( )A、透明溶液:、、、 B、强酸性溶液:、、、 C、小苏打溶液:、、、 D、强碱性溶液:、、、。8. 同温同压下,等质量的和相比较,下列结论正确的是( )A、它们的体积比为 B、共价键数之比为 C、它们的质子数之比为 D、密度之比为9. 设表示阿伏加德罗常数的值。下列叙述正确的是( )A、标准状况下,含有的电子数为 B、溶液中所含的物质的量为 C、中含有的阴、阳离子总数为 D、与一定量反应,生成和的混合物,钠失去的电子数为10. 下列离子方程式书写错误的是( )A、三氯化铁溶液与铁粉反应: B、溶于水: C、向烧碱溶液中加入一小段铝片: D、将稀盐酸滴在石灰石上:11. 下列有关物质的除杂方法错误的是( )选项
目标物质
杂质
除杂方法
①
加热至恒重
②
加入过量溶液,过滤
③
通过饱和食盐水,洗气
④
加入过量铜粉,过虑
A、① B、② C、③ D、④12. 已知短周期元素的四种离子aA2+、bB+、cC3-、dD-具有相同的电子层结构,则下列叙述中正确的是( )A、原子半径:B>A>C>D B、原子序数:D>C>B>A C、离子半径:C3->D->A2+>B+ D、氧化性:A2+>B+ , 还原性:C3-<D-13. 下列实验装置及操作能达到实验目的的是( )A
B
C
D




实验室制备少量Fe(OH)2
证明干燥的氯气无漂白作用
钾元素的焰色试验
除去水中的泥沙
A、A B、B C、C D、D14. 已知反应 , 下列说法正确的是( )A、氧化产物是 B、反应中氧化剂与还原剂的物质的量之比为 C、当有反应时,反应中转移电子 D、该反应属于置换反应15. 化合价和物质类别是整理元素的单质及化合物知识的两个要素,可表示为“价-类”二维图。已知铁元素的“价-类”二维图如图所示。下列说法正确的是( )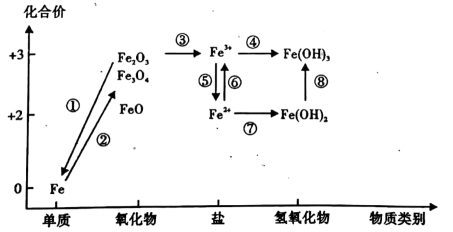 A、利用上述转化④,向溶液中滴加饱和溶液,可制取胶体 B、是一种黑色粉末,不稳定,在空气中受热,迅速被氧化成 C、露置于空气中,可实现上述转化⑧,该反应既属于化合反应,又属于氧化还原反应 D、实验室中检验 , 先加入氯水可实现上述转化⑥,再加入KSCN溶液,溶液变红,证明溶液中含
A、利用上述转化④,向溶液中滴加饱和溶液,可制取胶体 B、是一种黑色粉末,不稳定,在空气中受热,迅速被氧化成 C、露置于空气中,可实现上述转化⑧,该反应既属于化合反应,又属于氧化还原反应 D、实验室中检验 , 先加入氯水可实现上述转化⑥,再加入KSCN溶液,溶液变红,证明溶液中含二、填空题
-
16. 对于数以千万计的物质和为数众多的化学反应,分类法的作用几乎是无可代替的。
现有以下物质:①②酒精③④⑤溶液
(1)、以上物质中属于酸性氧化物的是(填序号)。(2)、请写出①的电子式。(3)、写出⑤中溶质的电离方程式。(4)、 ③在标准状况下的体积是 , 其中含氧原子的物质的量是mol。(5)、 (其中元素为价)是一种新型绿色消毒剂,主要用于饮用水处理。湿法制备高铁酸钠反应为:该反应中,被氧化的元素是(填元素符号),氧化剂是(填化学式),生成时,转移电子的物质的量为 , 消耗g。三、元素或物质推断题
-
17. 下表列出了七种短周期元素在周期表中的位置:
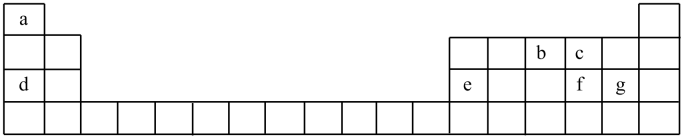 (1)、 单质的结构式为。(2)、 化合物的电子式为 , 该化合物与水反应的化学方程式为。(3)、元素c在周期表中的位置是 , c的两种同素异形体的化学式为。(4)、元素d、e、f、g形成的简单离子中,离子半径最小的是(填离子符号)。(5)、 单质通入d元素最高价氧化物的水化物中可制备“84消毒液”,该反应的离子方程式为。(6)、下列事实不能说明g的非金属性比f的非金属性强的是_______。A、将g的单质通入f的气态氢化物形成的溶液中,有淡黄色沉淀产生 B、气态氢化物稳定性: C、f单质与化合时产物中为价,g单质与化合时产物中为价 D、氧化物对应水化物的酸性:18. 元素的“价-类”二维图是同学们认识物质性质及其转化关系的重要思维工具,从物质类别、化合价角度认识含氯元素的物质的性质及其转化关系,图中甲~辛均为含氯元素的物质。回答下列问题:
(1)、 单质的结构式为。(2)、 化合物的电子式为 , 该化合物与水反应的化学方程式为。(3)、元素c在周期表中的位置是 , c的两种同素异形体的化学式为。(4)、元素d、e、f、g形成的简单离子中,离子半径最小的是(填离子符号)。(5)、 单质通入d元素最高价氧化物的水化物中可制备“84消毒液”,该反应的离子方程式为。(6)、下列事实不能说明g的非金属性比f的非金属性强的是_______。A、将g的单质通入f的气态氢化物形成的溶液中,有淡黄色沉淀产生 B、气态氢化物稳定性: C、f单质与化合时产物中为价,g单质与化合时产物中为价 D、氧化物对应水化物的酸性:18. 元素的“价-类”二维图是同学们认识物质性质及其转化关系的重要思维工具,从物质类别、化合价角度认识含氯元素的物质的性质及其转化关系,图中甲~辛均为含氯元素的物质。回答下列问题: (1)、己的化学式为。(2)、甲、乙、丙中,属于非电解质的是(填化学式)。(3)、检验溶液丁中含的方法:向少量丁溶液中滴加溶液,然后再加入适量酸 , 酸为(填名称),加入酸Y的目的是。(4)、庚为漂白粉的有效成分,写出由乙制备漂白粉的化学方程式。(5)、庚是“84消毒液”的有效成分,能有效灭菌。某化学社团模拟生产厂家配制了“84消毒液”,并在瓶体贴上标签,如图所示。回答下列问题:
(1)、己的化学式为。(2)、甲、乙、丙中,属于非电解质的是(填化学式)。(3)、检验溶液丁中含的方法:向少量丁溶液中滴加溶液,然后再加入适量酸 , 酸为(填名称),加入酸Y的目的是。(4)、庚为漂白粉的有效成分,写出由乙制备漂白粉的化学方程式。(5)、庚是“84消毒液”的有效成分,能有效灭菌。某化学社团模拟生产厂家配制了“84消毒液”,并在瓶体贴上标签,如图所示。回答下列问题:84消毒液
(有效成分)NaClO (规格)500mL
(质量分数)14.9% (密度)1.1g·cm-3
①该“84消毒液”有效成分的物质的量浓度为。
②“84消毒液”与稀硫酸混合使用可增强消毒能力,请用化学方程式解释其原因。某消毒小组人员用的浓硫酸配制的稀硫酸用于增强“84消毒液”的消毒能力,配制该稀硫酸的过程中,除用到量筒、烧杯、玻璃棒及胶体滴管外,还需要的玻璃仪器有。若所配制的稀硫酸浓度偏高,则可能的原因是(填字母)。
A.配制前,容量瓶中有少量蒸馏水 B.量取浓硫酸时,仰视液体的凹液面
C.未冷却,立即转移至容量瓶定容 D.未洗涤烧杯和玻璃棒
四、实验题
-
19. 某小组设计如下实验探究铁与水蒸气反应。
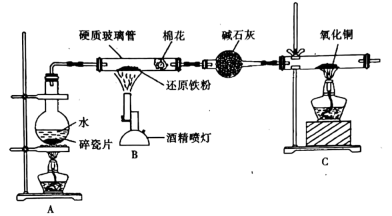
回答下列问题:
(1)、写出铁和水蒸气反应的化学方程式,并用双线桥表示电子转移的方向和数目。(2)、A、B、C三个装置中应先点燃处的酒精(喷)灯,点燃C处酒精灯之前应进行的操作是。(3)、检验固体中是否存在和:取少量固体,先用足量稀硫酸溶解,将所得溶液分成两份,一份加入试剂 (填字母,下同)可检验 , 另一份加入试剂可检验。可选择试剂:A.溶液 B.新制氯水 C.溶液 D.酸性溶液(4)、工业上用废磁铁(主要成分为 , 含少量的与)制取绿矾的流程图如下。
①与分别为(填化学式)。
②加入过量溶液发生反应的离子方程式为。
③写出流程图中溶解的离子方程式。
-