江苏省南京市联合体2023年中考一模化学试题
试卷更新日期:2023-06-20 类型:中考模拟
一、单选题
-
1. 下列变化属于化学变化的是( )A、干冰升华 B、石蜡熔化 C、酒精挥发 D、水的电解2. 下列物质在氧气中燃烧,火星四射,有黑色固体生成的是( )A、铁丝 B、木炭 C、红磷 D、硫粉3. 下列物质中,属于合成材料的是( )A、生铁 B、羊毛 C、塑料 D、棉花4. 制作景泰蓝的轴料中常含钴元素。钴元素在元素周期表中的信息如图,下列有关钴元素的说法不正确的是( )
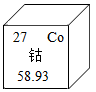 A、中子数是27 B、元素符号是Co C、属于金属元素 D、相对原子质量是58.935. 稀释浓硫酸并进行硫酸性质实验的下列操作,正确的是( )A、
A、中子数是27 B、元素符号是Co C、属于金属元素 D、相对原子质量是58.935. 稀释浓硫酸并进行硫酸性质实验的下列操作,正确的是( )A、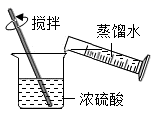 稀释浓硫酸
B、
稀释浓硫酸
B、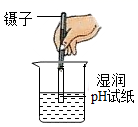 测稀硫酸的pH
C、
测稀硫酸的pH
C、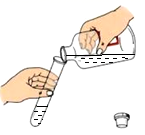 倾倒稀硫酸
D、
倾倒稀硫酸
D、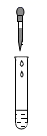 滴加稀硫酸
6. 将下列气体通入酚酞溶液中,酚酞溶液会变红的是( )A、NH3 B、O2 C、NO2 D、SO27. 下列有关化学用语的叙述,正确的是( )A、Ne——表示氖气 B、C60——表示60个碳原子 C、Fe3+——表示亚铁离子 D、2N——表示2个氮分子8. 下列有关燃烧和灭火的说法,正确的是( )A、用嘴吹灭蜡烛——降低石蜡的着火点 B、森林着火开辟隔离带——清除可燃物 C、木柴架空——增大空气中氧气浓度 D、煤炉火越扇越旺——增大与氧气的接触面积9. 下列叙述正确的是( )A、用活性炭可将硬水软化 B、用甲醛水溶液做食品保鲜剂 C、用食盐水除去热水壶内壁的水垢 D、用汽油可除去衣服上的油污10. 下表中对宏观事实的微观解释,不合理的是( )
滴加稀硫酸
6. 将下列气体通入酚酞溶液中,酚酞溶液会变红的是( )A、NH3 B、O2 C、NO2 D、SO27. 下列有关化学用语的叙述,正确的是( )A、Ne——表示氖气 B、C60——表示60个碳原子 C、Fe3+——表示亚铁离子 D、2N——表示2个氮分子8. 下列有关燃烧和灭火的说法,正确的是( )A、用嘴吹灭蜡烛——降低石蜡的着火点 B、森林着火开辟隔离带——清除可燃物 C、木柴架空——增大空气中氧气浓度 D、煤炉火越扇越旺——增大与氧气的接触面积9. 下列叙述正确的是( )A、用活性炭可将硬水软化 B、用甲醛水溶液做食品保鲜剂 C、用食盐水除去热水壶内壁的水垢 D、用汽油可除去衣服上的油污10. 下表中对宏观事实的微观解释,不合理的是( )选项
事实
解释
A
水银温度计放入热水中,水银柱升高
受热后原子之间的间隔变大
B
一氧化碳和二氧化碳化学性质不同
分子的构成不同
C
酸具有相似的化学性质
酸溶液中都含有酸根离子
D
铵态氮肥和碱性物质不能混用
铵根离子和氢氧根离子会发生反应
A、A B、B C、C D、D11. 除去下列物质中混有的少量杂质(括号内为杂质),拟定的实验方案可行的是( )A、CO2气体(HCl气体)——通过足量NaOH溶液,干燥 B、CuO固体(Cu)——加入足量的稀盐酸,过滤,洗涤,干燥 C、FeCl2溶液(CuCl2)——加入过量的铁粉,过滤 D、NaCl溶液(Na2SO4)——加入适量的Ba(NO3)2溶液,过滤12. 某冶炼厂处理尾气时有下列转化,下列说法不正确的是( ) A、转化①是氧化反应 B、甲、乙、丁属于氧化物 C、乙中氮元素的化合价为+4价 D、转化②中,参加反应的乙与生成丙的分子个数之比为2:113. 下列实验设计不能达到实验目的的是( )
A、转化①是氧化反应 B、甲、乙、丁属于氧化物 C、乙中氮元素的化合价为+4价 D、转化②中,参加反应的乙与生成丙的分子个数之比为2:113. 下列实验设计不能达到实验目的的是( )选项
A
B
C
D
实验设计




实验目的
探究铁生锈条件
探究燃烧条件
验证质量守恒定律
探究硝酸铵溶解吸热
A、A B、B C、C D、D14. 某兴趣小组同学将pH传感器分别插入三只盛有相同体积蒸馏水的烧杯中,打开磁力搅拌器,同时采集数据,再向三只烧杯中同时分别加入适量的柠檬酸、氯化钠、氢氧化钠三种固体。实验数据如图所示,下列说法不正确的是( ) A、①表示氢氧化钠溶于水,说明OH-浓度越大pH越大 B、②表示氯化钠溶于水,pH=7说明溶液中无自由移动离子 C、③表示柠檬酸溶于水,说明H+浓度越大pH越小 D、柠檬酸溶液和氢氧化钠能发生中和反应15. 某气体中可能含有CO2、O2、N2中的一种或几种,将该气体依次通过:①足量炽热的焦炭;②足量灼热的氧化铜;③足量的碱石灰(氢氧化钠和氧化钙的混合物)。每一步均充分反应,最终得到的气体为纯净物,气体的分子数目与反应步骤的关系如图所示,下列说法不正确的是( )
A、①表示氢氧化钠溶于水,说明OH-浓度越大pH越大 B、②表示氯化钠溶于水,pH=7说明溶液中无自由移动离子 C、③表示柠檬酸溶于水,说明H+浓度越大pH越小 D、柠檬酸溶液和氢氧化钠能发生中和反应15. 某气体中可能含有CO2、O2、N2中的一种或几种,将该气体依次通过:①足量炽热的焦炭;②足量灼热的氧化铜;③足量的碱石灰(氢氧化钠和氧化钙的混合物)。每一步均充分反应,最终得到的气体为纯净物,气体的分子数目与反应步骤的关系如图所示,下列说法不正确的是( ) A、a点气体中一定含N2 , 还含有CO2和O2中一种或两种 B、b点气体由两种分子构成 C、c点气体中CO2和N2的分子数目比为2:1 D、该过程中发生了化合反应、置换反应和复分解反应
A、a点气体中一定含N2 , 还含有CO2和O2中一种或两种 B、b点气体由两种分子构成 C、c点气体中CO2和N2的分子数目比为2:1 D、该过程中发生了化合反应、置换反应和复分解反应二、实验题
-
16. 下图所示的仪器常用于实验室制取气体,回答下列问题。
 (1)、用稀盐酸和大理石制取二氧化碳的化学方程式为 , 发生装置和收集装置的仪器组合是(填字母)。
(1)、用稀盐酸和大理石制取二氧化碳的化学方程式为 , 发生装置和收集装置的仪器组合是(填字母)。A.①②⑦⑧ B.①③④⑥⑨ C.①②⑥⑧⑨ D.①③⑤⑥⑧⑨
(2)、用高锰酸钾制取氧气的化学方程式为。(3)、请设计实验鉴别氧气和二氧化碳两瓶气体,并完成实验报告。实验步骤
实验现象
实验结论
17. 在丰富多彩的物质世界里,碳及其化合物占有重要地位。(1)、金刚石和石墨的化学性质相似,但物理性质却存在很大差异,原因是。(2)、我国科学家将立方金刚石中的每个碳原子,用一个由四个碳原子组成的正四面体结构单元取代,形成了用途更为广泛的“T—碳”(如图),下列关于“T—碳”的说法不正确的是____(填字母)。 A、其中的碳原子静止不动 B、它与金刚石是同一种物质 C、它是一种新型的含碳化合物 D、它在氧气中完全燃烧的产物是CO2(3)、我国力争在2060年前实现“碳中和”。实现“碳中和”通常可采取如下措施:
A、其中的碳原子静止不动 B、它与金刚石是同一种物质 C、它是一种新型的含碳化合物 D、它在氧气中完全燃烧的产物是CO2(3)、我国力争在2060年前实现“碳中和”。实现“碳中和”通常可采取如下措施:①碳减排:使用氢能源汽车可以有效减少二氧化碳的排放。单质硼(B)可与物质X反应制取氢气,化学方程式为 , 则X的化学式为。
②海洋吸收:用海水吸收二氧化碳,该反应的化学方程式是。
③碳转化:将二氧化碳和氨气在一定条件下反应生成尿素【CO(NH2)2】和水,写出该反应的化学方程式。
(4)、工业上用氢氧化钙实现“碳捕捉”,某石灰水中含有氢氧化钙3.7g,要使该石灰水中氢氧化钙全部转化为沉淀,能够吸收二氧化碳的质量是多少?(写出计算过程)三、综合题
-
18. 某实验室排放的废液中含有CuSO4、FeSO4和ZnSO4三种溶质,为减少水污染并节约成本,回收硫酸锌、金属铁和铜,某兴趣小组同学设计流程如下图所示。
 (1)、步骤1—4的操作中均用到的玻璃仪器是。(2)、固体a的成分是。(3)、Y是(写名称)。(4)、步骤1和步骤3发生的相同反应的化学方程式为。19. 溶液在生产生活中有重要的用途,(1)、生理盐水的溶剂是。(2)、下列关于溶液的说法,正确的是____(填字母)。A、溶液一定是无色的 B、溶液一定是均一、稳定的混合物 C、溶液中的溶质可以有多种 D、长期放置后不会分层的液体一定是溶液(3)、甲、乙两种不含结晶水的固体物质的溶解度曲线如图1所示。
(1)、步骤1—4的操作中均用到的玻璃仪器是。(2)、固体a的成分是。(3)、Y是(写名称)。(4)、步骤1和步骤3发生的相同反应的化学方程式为。19. 溶液在生产生活中有重要的用途,(1)、生理盐水的溶剂是。(2)、下列关于溶液的说法,正确的是____(填字母)。A、溶液一定是无色的 B、溶液一定是均一、稳定的混合物 C、溶液中的溶质可以有多种 D、长期放置后不会分层的液体一定是溶液(3)、甲、乙两种不含结晶水的固体物质的溶解度曲线如图1所示。

①t1℃时,将等质量的甲、乙两种物质分别加入盛有100g水的A、B两只烧杯中,充分搅拌后现象如图2所示,烧杯A中溶解的溶质是(填“甲”或“乙”),烧杯B中的上层清液属于溶液(填“饱和”或“不饱和”)。
②将t3℃时甲的饱和溶液150g稀释成质量分数为10%的甲溶液,需加水mL(水的密度为1g/cm3)。完成稀释的主要操作步骤是:计算、、混匀。
③现有t2℃时的甲的饱和溶液和乙的饱和溶液。下列说法正确的是(填字母)。
A.两溶液中溶质的质量均为30g
B.分别升温至t3℃,所得溶液中溶质的质量分数一定相等
C.分别降温到t1℃,析出甲的质量一定大于析出乙的质量
D.保持温度不变,分别加入等质量的水,混匀后所得溶液中溶质的质量分数一定相等
20. 图中A~I是初中化学常见的物质,其中A、D为单质,B、C为氧化物,组成D的元素在地壳中的含量位居第四;F可用来改良酸性土壤;H可用作干燥剂,图中“一”表示两端的物质问能发生化学反应;“→”表示物质间存在转化关系:部分反应物、生成物或反应条件已略去。 (1)、写出化学式:D。(2)、写出B→C反应的化学方程式。(3)、写出F与I反应的化学方程式。(4)、写出G与H反应的化学方程式。21. 硫酸铜及硫酸锅晶体(CuSO4·5H2O俗称胆矾,相对分子质量为250)广泛应用于生产生活及实验中。(1)、Ⅰ、结构与类别
(1)、写出化学式:D。(2)、写出B→C反应的化学方程式。(3)、写出F与I反应的化学方程式。(4)、写出G与H反应的化学方程式。21. 硫酸铜及硫酸锅晶体(CuSO4·5H2O俗称胆矾,相对分子质量为250)广泛应用于生产生活及实验中。(1)、Ⅰ、结构与类别构成硫酸铜的微观粒子是(填符号)。
(2)、硫酸铜属于____(填字母)。A、化合物 B、氧化物 C、酸 D、碱 E、盐(3)、Ⅱ、性质农药波尔多液由硫酸铜和石灰乳等配制而成,其中两种主要成分(填“能”或“不能”)发生复分解反应,判断依据是。
(4)、CuSO4溶液对过氧化氢的分解具有催化作用,写出该反应的化学方程式。(5)、将25.0g胆矾加热,固体质量与成分简温度变化的曲线如图。
①根据胆矾分解的化学方程式 , 计算出图中X的值是。
②650℃时,CuSO4开始发生分解反应,生成CuO和另一种氧化物,则该反应的化学方程式为。
③剩余7.2g固体中铜元素和氧元素的质量比为(填最简整数比)。
(6)、检验该气体中是否含水蒸气的装置是(填字母)。(7)、若反应过程中产生的气体全部被D、E吸收,装置D、E分别增重4.5g、4.4g,则该气体中一定含有的成分是。