广东省广州市番禺区2023年中考一模化学试题
试卷更新日期:2023-06-08 类型:中考模拟
一、选择题
-
1. 下列事实中,利用物质化学性质的是( )A、干冰用于人工降雨 B、汽油作燃料 C、铜作导线 D、石墨用于制铅笔2. 金刚石和石墨是常见的碳单质,其结构如图所示。下列说法正确的是( )
 A、构成金刚石和石墨的原子大小不同 B、金刚石和石墨中原子排列方式相同 C、1g金刚石和1g石墨所含原子数相同 D、金刚石和石墨在氧气中都不能燃烧3. 铷(Rb)原子钟被称作北斗卫星的“心脏”、下图为铷原子的结构示意图,下列说法不正确的是( )
A、构成金刚石和石墨的原子大小不同 B、金刚石和石墨中原子排列方式相同 C、1g金刚石和1g石墨所含原子数相同 D、金刚石和石墨在氧气中都不能燃烧3. 铷(Rb)原子钟被称作北斗卫星的“心脏”、下图为铷原子的结构示意图,下列说法不正确的是( ) A、铷原子核内的质子数为37 B、铷原子在化学变化中容易失去1个电子 C、铷原子的核外电子分5层排布 D、氯化铷的化学式为RbCl24. 将足量NH3和CO2依次通入饱和食盐水,发生反应:① ;② 。下列说法正确的是( )A、总的化学方程式为 B、上述反应过程中观察不到明显现象 C、反应②是有沉淀生成的复分解反应 D、上述反应中有元素化合价发生变化5. 某种火箭在发射时,其燃料发生反应的微粒种类变化示意图如下。下列说法正确的是( )
A、铷原子核内的质子数为37 B、铷原子在化学变化中容易失去1个电子 C、铷原子的核外电子分5层排布 D、氯化铷的化学式为RbCl24. 将足量NH3和CO2依次通入饱和食盐水,发生反应:① ;② 。下列说法正确的是( )A、总的化学方程式为 B、上述反应过程中观察不到明显现象 C、反应②是有沉淀生成的复分解反应 D、上述反应中有元素化合价发生变化5. 某种火箭在发射时,其燃料发生反应的微粒种类变化示意图如下。下列说法正确的是( )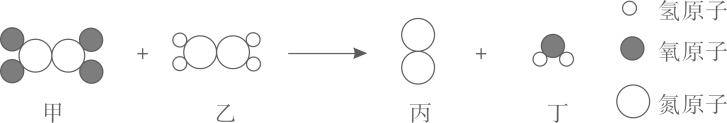 A、该反应为置换反应 B、反应前后都存在N2分子 C、每个甲分子中含有6个原子 D、反应生成丙和丁的质量比为28:186. 下列关于氯化钠的认识,正确的是( )A、组成:含有钠和氯两种单质 B、性质:与盐酸类似,能与碳酸盐反应 C、用途:可用于生产金属钠 D、生产:常用钠与氯气通过化合反应获得7. 25℃时,探究某固体物质的溶解性,实验记录如下表。下列实验结论正确的是( )
A、该反应为置换反应 B、反应前后都存在N2分子 C、每个甲分子中含有6个原子 D、反应生成丙和丁的质量比为28:186. 下列关于氯化钠的认识,正确的是( )A、组成:含有钠和氯两种单质 B、性质:与盐酸类似,能与碳酸盐反应 C、用途:可用于生产金属钠 D、生产:常用钠与氯气通过化合反应获得7. 25℃时,探究某固体物质的溶解性,实验记录如下表。下列实验结论正确的是( )编号
①
②
③
④
水的质量/g
50
50
50
50
加入固体质量/g
5
10
15
20
现象
固体完全溶解
固体完全溶解
剰余少量固体
剩余较多固体
A、实验①所得溶液溶质的质量分数为10% B、实验②说明25℃时该物质的溶解度是20g C、实验③④所得溶液溶质的质量分数相同 D、实验④所得溶液中含溶质的质量为20g8. 用如图所示实验探究燃烧的条件,下列说法正确的是( )①
②
③
④




白磷不燃烧
白磷不燃烧
白磷不燃烧
白磷燃烧
A、对比①③说明燃烧的条件之一是可燃物接触氧气 B、对比①④说明燃烧的条件之一是需要有可燃物 C、对比③④说明燃烧的条件之一是达到可燃物的着火点 D、本实验用盘成螺旋状的细铁丝替代白磷,能得到相同的实验结论9. “劳动创造幸福,实干成就伟业。”下列劳动所涉及的化学知识正确的是( )选项
劳动项目
化学知识
A
用明矾处理较浑浊的天然水
明矾主要起杀菌消毒作用
B
煮水时,若水的硬度大,易结垢
硬水中含有较多可溶性钙、镁化合物
C
在盐田中晾晒海水,得到粗盐
盐除去泥沙即可得到纯净的氯化钠
D
用含小苏打的发酵粉焙制糕点
小苏打(NaHCO3)的化学名称是碳酸钠
A、A B、B C、C D、D10. 有X,Y,Z三种金属片,分别放入稀硫酸中,X,Z表面有气泡产生,Y没有明显现象X放入ZCln溶液,没有明显现象。判断这三种金属的活动性由强到弱的顺序是( )
A、X>Y>Z B、Z>X>Y C、X>Z>Y D、Y>X>Z11. 下列关于化肥的说法不正确的( )A、化肥对提高农作物的产量具有重要作用 B、化肥的过度使用会造成土壤酸化,可用熟石灰改良 C、铵态氮肥与熟石灰混合研磨后能嗅到刺激性气味 D、氯化钾(KCl)和磷酸氢二铵 都属于复合肥料12. 下列说法不正确的是( )A、多吃果蔬可以补充维生素 B、炒菜用加碘盐可补充碘元素 C、葡萄糖、淀粉、蛋白质都是有机高分子化合物 D、CO与血红蛋白的结合能力强于O213. 下列关于物质的性质和用途的表述没有直接联系的是( )选项
性质
用途
A
常温下碳的化学性质不活泼
用墨绘制字画
B
醋酸显酸性
用醋酸除去热水瓶中的水垢
C
NaOH能与油脂反应
用NaOH除去油污
D
CH4常温下是气体
用CH4作燃料
A、A B、B C、C D、D14. 下列实验方案中,能达到目的的是( )选项
实验目的
实验方案
A
除去盐酸中的少量硫酸
加入过量Ba(NO3)2溶液后过滤
B
除去MgCl2溶液中的少量盐酸
加入过量MgO后过滤
C
鉴别NH4Cl和K2CO3固体
取样,加入CaCl2粉末,研磨、闻气味
D
鉴别NaCl和Na2SO4溶液
取样,滴加Mg(NO3)2溶液,观察现象
A、A B、B C、C D、D二、非选择题
-
15. 制笔行业中经常用到铂、钌(Ru)等贵金属。现有5种含钌元素的物质:Ru、RuO2、Ru2O3、RuCl3、K2RuO4。回答下列问题:(1)、RuO2读作。(2)、上述5种物质中钌元素的化合价一共有种。(3)、从物质分类的角度看,K2RuO4属于____。(填选项)A、化合物 B、氧化物 C、碱 D、盐(4)、H2与Ru2O3在加热条件下反应可得到Ru。写出反应的化学方程式。(5)、人类一直将金属单质及其合金应用于生产生活中,青铜器在我国夏商时期已经开始使用,铁制农具在我国春秋时期已经开始使用,而一直到1807年,科学家汉弗里·戴维通过电解熔融氢氧化钾首次制取得到金属单质钾。请写出人类发现和利用金属单质及其合金的时间早晚与金属活动性的关系为。你认为其原因是。16. 某固体混合物可能含有Na2CO3、Na2SO4、CuSO4、CaCl2、NaCl中的一种或几种,为了确定该混合物的成分,进行如下实验:
步骤I:将固体混合物溶于水,搅拌后得无色透明溶液
步骤II:往此溶液中滴加足量硝酸钡溶液,有白色沉淀生成
步骤III:过滤,将沉淀物置于稀硝酸中,发现沉淀全部溶解,并放出气体。试判断:
(1)、固体混合物中肯定有 , 肯定没有 , 可能有(2)、对可能有的物质,可采用向步骤III中的滤液滴加溶液来检验。(3)、写出步骤III中发生的化学方程式17. 碳捕集和碳的资源化利用是碳中和领域研究热点。(1)、I、碳捕集:捕捉烟气中的CO2 , 将其再释出可实现资源化利用,相关物质转化如下:
已知:
“颗粒反应室”中发生的反应为复分解反应,其化学方程式为。
(2)、上述流程中可循环使用的物质有2种,分别是、(填化学式)。(3)、Ⅱ、碳的资源化利用:中国科学家已实现由CO2到淀粉的全人工合成,主要过程如下:
绿色植物通过作用实现将CO2转化为葡萄糖。
(4)、阶段I反应的微观过程如图1所示。写出甲醇的化学式。 (5)、阶段II的物质转化如图2所示。反应a中四种物质的化学计量数均为1。
(5)、阶段II的物质转化如图2所示。反应a中四种物质的化学计量数均为1。①推测分子中氢原子数目:甲醇甲醛(填“>”、“<”或“=”)。
②为使甲醇持续转化为甲醛,反应b需补充H2O2 , 理论上需补充的H2O2与反应a中生成的H2O2的分子个数比:。
18. 实验室常用溶质质量分数为6%的H2O2溶液(MnO2作催化剂)制取氧气。(1)、配制质量分数为6%的H2O2溶液。①计算:配制150g质量分数为6%的H2O2溶液,需要质量分数为30%(密度为1.1g/cm3)的H2O2溶液体积为mL(计算结果保留一位小数),水为g。
②量取:用量筒量取所需H2O2溶液和水,倒入烧杯中。用量筒量取液体时,视线应与。
③混匀:…。
(2)、制取氧气(可能用到的部分装置如图)。
①实验室用氯酸钾(MnO2作催化剂)制取干燥的氧气,选择的发生装置和收集装置为(填字母),反应的化学方程式为。
②实验室用发生装置B制取氧气的化学方程式为。
(3)、实验反思。①若其他操作正确,量取水时俯视读数,则配制的H2O2溶液溶质质量分数6%(填“>”、“<”或“=”)。
②若用E装置收集一瓶(容积为200mL)体积分数为80%的氧气,预先应用量筒量取mL的水加入该集气瓶中(不考虑水蒸气的影响)。
19. 氢氧化钠变质的实验探究:(1)、I:向钠离子质量分数均为2%的氯化钠溶液、氢氧化钠溶液、碳酸钠溶液中滴加酚酞,氯化钠溶液不变红,氢氧化钠溶液、碳酸钠溶液变红。Ⅱ:一位实验员在实验室刚配制一定质量分数的氢氧化钠溶液后,突然接到紧急任务离开,几天后回到实验室才发现没有盖上瓶塞。
你认为能使酚酞变红的微粒为____。
A、Na+ B、OH- C、或由引发生成的OH-。(2)、氢氧化钠变质为碳酸钠,反应的化学方程式为。溶液中的离子数量如何变化?。(填:不变、减少、增大)(3)、欲证明有氢氧化钠变质为碳酸钠,同学甲认为可选择试剂a:稀盐酸,同学乙认为可选择试剂b;氯化钡溶液,你的观点是____。(单项选择题)A、过量稀盐酸 B、过量氯化钡溶液 C、过量稀盐酸和氯化钡溶液均可以 D、过量稀盐酸和氯化钡溶液均不可以(4)、同学丙认为氢氧化钠只有一部分变质为碳酸钠,溶液中仍然含有氢氧化钠,他通过设计以下实验证明其结论是正确的。第一步:取少量待测液,向其中加入过量的溶液,过滤;
第二步:向以上滤液中加入 , 出现的现象,则丙同学观点正确。
(5)、100g质量分数为A%的氢氧化钠溶液有部分变质后,同学丁认为仍然可以通过设计实验方案计算出A的数值,其具体的实验方案如下:向变质后的溶液中加入过量的稀盐酸,蒸发结晶,洗涤,干燥,得到5.85g固体,从而可以计算出A的数值。你认为是否可以?(填“可以”或“不可以”)。若不可以,请简述理由,若可以,则写出A的数值。20. 草酸镍晶体(NiC2O4·2H2O)难溶于水,可用于制镍催化剂。(1)、【探究一】某小组用废镍催化剂(主要成分含有Ni,还含有少量的Al2O3、Fe)制备草酸镍晶体的部分实验流程如图1:

“粉碎”的目的是。
(2)、“酸浸”的目的是为了得到NiSO4 , 但同时会生成新的杂质,写出生成杂质的化学反应方程式、。(3)、“一系列操作”主要是为了除去溶液中铁元素对应的离子和(填写离子符号)等。(4)、保持其他条件相同,在不同温度下对废镍催化剂进行“酸浸”,镍浸出率(硫酸镍的产率)随时间变化如图2。从工业生产和能源利用率的角度分析,“酸浸”的最适宜温度与时间分别为____(单项选择)。 A、30℃、30min B、90℃、150min C、70℃、120min D、90℃、120min(5)、发生“沉镍”反应后生成草酸镍晶体,其化学方程式为 , “沉镍”后的滤液在农业中可用作。(6)、【探究二】对草酸镍晶体(NiC2O4·2H2O)进行热重分析,温度与TG%的关系如图3所示
A、30℃、30min B、90℃、150min C、70℃、120min D、90℃、120min(5)、发生“沉镍”反应后生成草酸镍晶体,其化学方程式为 , “沉镍”后的滤液在农业中可用作。(6)、【探究二】对草酸镍晶体(NiC2O4·2H2O)进行热重分析,温度与TG%的关系如图3所示【查阅资料】①NiC2O4·2H2O加热至200℃左右完全失去结晶水,生成NiC2O4;继续加热,则剩余固体会受热分解生成镍的氧化物、CO2和CO。
②
A点(TG=90.16)物质的化学式。
(7)、C点(TG=45.36)物质的化学式。