北京市燕山地区2023年中考一模化学试题
试卷更新日期:2023-06-08 类型:中考模拟
一、单选题
-
1. 下列人体所必需的元素中,缺乏会引起骨质疏松的是()A、铁 B、钙 C、碘 D、锌2. 化肥对提高农作物的产量具有重要作用。下列物质能用作磷肥的是( )A、K2SO4 B、CO(NH2)2 C、NH4Cl D、Ca(H2PO4)23. 废弃的易拉罐和塑料瓶属于( )A、厨余垃圾 B、其他垃圾 C、可回收物 D、有害垃圾4. 下列物质中,含有氧分子的是( )A、O2 B、MnO2 C、CO2 D、H2O25. 下列标志中,应贴在浓硫酸运输车上的是( )A、
 B、
B、 C、
C、 D、
D、 6. 下列物质在空气中暴露一段时间后,质量会减少的是( )A、浓硫酸 B、浓盐酸 C、大理石 D、食盐7. 下列实验操作正确的是( )A、
6. 下列物质在空气中暴露一段时间后,质量会减少的是( )A、浓硫酸 B、浓盐酸 C、大理石 D、食盐7. 下列实验操作正确的是( )A、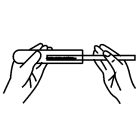 取固体粉末
B、
取固体粉末
B、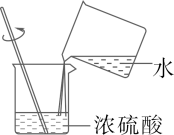 稀释浓硫酸
C、
稀释浓硫酸
C、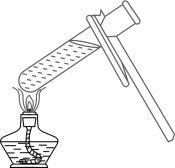 加热液体
D、
加热液体
D、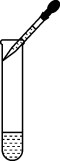 滴加液体
8. 下列符号中,能表示 2 个氢原子的是( )A、2H B、2H+ C、H2O D、2H29. 某同学制作的试剂标签如下,其中化学式书写不正确的是( )A、
滴加液体
8. 下列符号中,能表示 2 个氢原子的是( )A、2H B、2H+ C、H2O D、2H29. 某同学制作的试剂标签如下,其中化学式书写不正确的是( )A、 B、
B、 C、
C、 D、
D、 10. 下列关于电解水实验的说法中,正确的是( )
10. 下列关于电解水实验的说法中,正确的是( ) A、管a中的气体为H2 B、与管a相连的是电源的正极 C、管a与管b中气体质量比为2:1 D、该实验可说明水由H2和O2组成11. 下列对于灭火原理的分析中,正确的是( )A、砍掉大火蔓延路线前的树木 —— 隔离可燃物 B、用水扑灭燃着的木材 —— 降低木材的着火点 C、用锅盖盖灭油锅内的火 —— 降低油温 D、用扇子扇灭烛火 —— 隔绝空气12. 下列物质的用途中,利用其化学性质的是( )A、干冰做制冷剂 B、金属铜用于制导线 C、熟石灰改良酸性土壤 D、金刚石用于裁玻璃13. 氧气能压缩在钢瓶中保存,主要体现了( )A、分子的质量很小 B、分子间有间隔 C、分子在不断运动 D、分子由原子构成14. 碳元素与氧元素的本质区别是( )A、质子数不同 B、电子数不同 C、中子数不同 D、最外层电子数不同15. 下列方法不能区分O2和CO2两瓶气体的是( )A、观察颜色 B、伸入带火星木条 C、伸入燃着的木条 D、倒入澄清石灰水16. 从化学式“CO”中不能获取的信息是( )A、表示一氧化碳这种物质 B、一氧化碳有毒 C、碳元素与氧元素质量比为12:16 D、表示一个一氧化碳分子17. 下列化学方程式书写正确的是( )A、 B、 C、 D、18. 下列有关金元素的说法不正确的是( )
A、管a中的气体为H2 B、与管a相连的是电源的正极 C、管a与管b中气体质量比为2:1 D、该实验可说明水由H2和O2组成11. 下列对于灭火原理的分析中,正确的是( )A、砍掉大火蔓延路线前的树木 —— 隔离可燃物 B、用水扑灭燃着的木材 —— 降低木材的着火点 C、用锅盖盖灭油锅内的火 —— 降低油温 D、用扇子扇灭烛火 —— 隔绝空气12. 下列物质的用途中,利用其化学性质的是( )A、干冰做制冷剂 B、金属铜用于制导线 C、熟石灰改良酸性土壤 D、金刚石用于裁玻璃13. 氧气能压缩在钢瓶中保存,主要体现了( )A、分子的质量很小 B、分子间有间隔 C、分子在不断运动 D、分子由原子构成14. 碳元素与氧元素的本质区别是( )A、质子数不同 B、电子数不同 C、中子数不同 D、最外层电子数不同15. 下列方法不能区分O2和CO2两瓶气体的是( )A、观察颜色 B、伸入带火星木条 C、伸入燃着的木条 D、倒入澄清石灰水16. 从化学式“CO”中不能获取的信息是( )A、表示一氧化碳这种物质 B、一氧化碳有毒 C、碳元素与氧元素质量比为12:16 D、表示一个一氧化碳分子17. 下列化学方程式书写正确的是( )A、 B、 C、 D、18. 下列有关金元素的说法不正确的是( ) A、原子序数是79 B、属于非金属元素 C、元素符号是Au D、相对原子质量为197.019. 依据如图实验,不能得到的二氧化碳的性质是
A、原子序数是79 B、属于非金属元素 C、元素符号是Au D、相对原子质量为197.019. 依据如图实验,不能得到的二氧化碳的性质是 A、不可燃 B、不支持燃烧 C、能溶于水 D、密度大于空气20. 某食品包装信息如下图所示。完成下面小题。
A、不可燃 B、不支持燃烧 C、能溶于水 D、密度大于空气20. 某食品包装信息如下图所示。完成下面小题。
 (1)、饼干中含有的“钠”是指( )A、分子 B、原子 C、单质 D、元素(2)、梳打饼干中含量最高的营养素是( )A、糖类 B、蛋白质 C、油脂 D、无机盐(3)、下列物质中,溶于水能形成溶液的是( )A、小麦粉 B、食盐 C、棕榈油 D、蔬菜碎21. 如下图所示,60℃时,向100g水中加入65.8gKNO3 , 得①中溶液,降温至30℃,得②中溶液。不同温度下KNO3的溶解度如下表。
(1)、饼干中含有的“钠”是指( )A、分子 B、原子 C、单质 D、元素(2)、梳打饼干中含量最高的营养素是( )A、糖类 B、蛋白质 C、油脂 D、无机盐(3)、下列物质中,溶于水能形成溶液的是( )A、小麦粉 B、食盐 C、棕榈油 D、蔬菜碎21. 如下图所示,60℃时,向100g水中加入65.8gKNO3 , 得①中溶液,降温至30℃,得②中溶液。不同温度下KNO3的溶解度如下表。
温度/℃
20
30
40
50
60
溶解度/g
31.6
45.8
63.9
85.5
110
下列说法正确的是( )
A、①中溶液是KNO3饱和溶液 B、开始析出固体时的温度为30℃ C、②比①溶液质量少 D、②中溶液的溶质质量分数为45.8%22. 下列实验设计能达到实验目的的是( )选项
A
B
C
D
实验设计




实验目的
证明甲烷中含有碳、氢元素
验证二氧化碳与水反应
验证分子运动速率与温度有关
净化河水得到纯水
A、A B、B C、C D、D23. 甲酸(HCOOH)具有清洁制氢的巨大潜力,其分解制氢的微观示意图如下
下列说法正确的是( )
A、甲酸中有5个原子 B、乙中碳元素和氧元素的质量分数相等 C、反应前后分子种类发生改变 D、该反应中生成的甲和乙的质量比为1:1二、生活现象解释
-
24. 从A或B两题中任选一个作答,若两题均作答,按A计分。
A.Na2CO3的俗称是。
B.NaOH的俗称是。
25. 能源与环境。(1)、现阶段的能源结构仍以化石燃料为主,化石燃料包括煤、和天然气。(2)、氢气是一种清洁能源。氢气燃烧实现“零排放”的原因是(用化学方程式表示)。(3)、下列燃料在O2中充分燃烧时,不会产生CO2的是____(填序号)。A、天然气 B、酒精(C2H5OH) C、肼(N2H4)26. 铁是生活中使用最多的金属。(1)、铁丝在氧气中燃烧,观察到的现象是。(2)、工业用一氧化碳和赤铁矿炼铁原理的化学方程式为。(3)、出土的铁质编磬锈蚀严重,金饼却依然金光灿灿,从物质性质的角度解释其原因。三、科普阅读理解
-
27. 阅读下面科普短文。
中国是世界上最早发现和利用茶树的国家。
茶树适宜生长在pH为4.5~6.5的土壤中。茶叶有效成分主要含有的三类物质分别为茶多酚、氨基酸、咖啡碱。咖啡碱(化学式为C8H10N4O2)能使人体中枢神经产生兴奋,喝茶能提神解乏。茶多酚是茶叶所含多酚类物质的总称,是形成茶叶色香味的主要成分,也是茶叶中有保健功能的主要成分。

泡茶前一般要洗茶,可以唤醒茶叶的活性,冲泡时香气可以得到最大程度的散发,口感更加醇厚,另外茶叶在加工、储存过程中会有浮尘附着,洗茶,喝着更放心。
泡茶时水的温度不同,影响着茶水中茶多酚的浓度。温度过高,茶所具有的有益物质遭受破坏,温度过低,不能使茶叶中的有效成分充分浸出,其滋味淡薄。而且,不同种类的茶需要不同温度的水冲泡,才能达到茶的最佳保健效果。
以龙井茶(绿茶)为例进行研究,如图2为水温及浸泡时间对茶多酚溶解率的影响。

除了控制水温和浸泡时间外,多次浸泡也可提高茶多酚的溶解率。
(1)、茶树适宜生长在(填“酸性”“碱性”或“中性”)土壤。(2)、结合题中图1,把茶叶和茶水分离的操作是。(3)、咖啡碱中含有种元素。(4)、下列说法正确的是____(填序号)。A、结合图2为减少茶多酚流失,洗龙井茶时水的温度适宜在50℃左右 B、冲泡龙井茶时,水温、浸泡时间影响茶多酚的溶解率大小 C、生活中,各种茶都要用100℃的水冲泡(5)、保存茶叶时需要注意防潮,茶叶包装中常放入一小袋干燥剂,其成分为生石灰,写出生石灰与水反应的化学方程式。四、生产实际分析
-
28. 采用水解法生产高纯Al2O3的主要工艺流程如下:

已知:Al(OH)3难溶于水。
(1)、整个工艺流程中,属于氧化物的有(填化学式)。(2)、Al(OH)3中铝元素的化合价是。(3)、高温煅烧窑中主要发生分解反应,其化学方程式为。29. 我国的煤炭资源丰富,但液体燃料短缺。通过“煤液化”技术,用煤炭和水制取甲醇(CH3OH)对我国具有重要意义。主要流程如下: (1)、冷却器里发生的是(填“物理”或“化学”)变化。(2)、合成塔中发生的化学反应的微观示意图如下,请在方框内补全相应微粒的图示。
(1)、冷却器里发生的是(填“物理”或“化学”)变化。(2)、合成塔中发生的化学反应的微观示意图如下,请在方框内补全相应微粒的图示。 (3)、下列说法中,合理的是____(填序号)。A、甲醇属于有机化合物 B、煤炭与水在常温下即可生成CO和H2 C、甲醇的合成会受到CO和H2比例的影响
(3)、下列说法中,合理的是____(填序号)。A、甲醇属于有机化合物 B、煤炭与水在常温下即可生成CO和H2 C、甲醇的合成会受到CO和H2比例的影响五、基本实验及其原理分析
-
30. 根据下图回答问题。
 (1)、①实验室用KMnO4制取O2 , 选用的发生装置是(填序号,下同)。
(1)、①实验室用KMnO4制取O2 , 选用的发生装置是(填序号,下同)。②用双氧水(二氧化锰做催化剂)制取氧气的化学方程式为。
(2)、①实验室制取CO2 , 反应的化学方程式为。②检验某气体是二氧化碳,选用的装置是。发生化学反应的方程式为。
31. 从下图选择仪器进行实验,除去粗盐中难溶性杂质。 (1)、除去粗盐中难溶性杂质的基本实验步骤为:溶解、过滤、。(2)、溶解过程中玻璃棒的作用是。(3)、过滤时除铁架台(带铁圈)、滤纸外,还需要的仪器有(填序号)。32. 实验探究铁锈蚀影响因素,记录如下(炭不与盐酸反应)。
(1)、除去粗盐中难溶性杂质的基本实验步骤为:溶解、过滤、。(2)、溶解过程中玻璃棒的作用是。(3)、过滤时除铁架台(带铁圈)、滤纸外,还需要的仪器有(填序号)。32. 实验探究铁锈蚀影响因素,记录如下(炭不与盐酸反应)。实验装置
序号
其它试剂
200s时O2的含量

①
干燥剂
x%
②
10滴水
15%
③
10滴水和1.0g食盐
8%
(1)、①证明在干燥的空气中铁不锈蚀,则x是%。(2)、下列说法正确的是____(填序号)。A、②③中O2含量减少表明铁已锈蚀 B、①②证明水对锈蚀有影响 C、②③证明食盐能加快铁锈蚀 D、①②③证明炭粉对铁锈蚀有影响(3)、取出少量实验②后集气瓶中的固体于试管中,加入足量稀盐酸,看到有气泡产生,该现象证明取出的固体中一定含有。33. 下图所示的一组实验可用于验证可燃物燃烧的条件。 (1)、磷燃烧反应的化学方程式为。(2)、设计铜片上的白磷与红磷作对比,其目的是。(3)、得到“可燃物燃烧需要与氧气接触”的结论,依据的现象是。34. 用如图装置进行实验。实验时,先将浓NaOH溶液挤入盛有CO2的试管中,振荡,将止水夹K打开。
(1)、磷燃烧反应的化学方程式为。(2)、设计铜片上的白磷与红磷作对比,其目的是。(3)、得到“可燃物燃烧需要与氧气接触”的结论,依据的现象是。34. 用如图装置进行实验。实验时,先将浓NaOH溶液挤入盛有CO2的试管中,振荡,将止水夹K打开。 (1)、A中发生反应的化学方程式为。(2)、打开止水夹K后,观察到B中稀盐酸被倒吸入A中,产生此现象的原因是 , 又观察到A中的现象是 , 发生此反应的化学方程式为。
(1)、A中发生反应的化学方程式为。(2)、打开止水夹K后,观察到B中稀盐酸被倒吸入A中,产生此现象的原因是 , 又观察到A中的现象是 , 发生此反应的化学方程式为。六、科学探究题
-
35. 84消毒液是次氯酸钠和表面活性剂的混配消毒剂。有效成分为次氯酸钠(NaClO),广泛用于医院、宾馆、旅游、家庭等的卫生消毒,84消毒液不稳定,光照能加速分解。其杀菌作用主要依靠有效氯,有效氯越高杀菌效果越好,杀菌就是使病毒蛋白质变性,蛋白质发生变性反应后会变形、变硬。84消毒液还具备漂白能力。某化学兴趣小组对该消毒液进行了如下系列探究。(1)、【实验1】84消毒液中有效氯的稳定性。
测定0.5%的84消毒液在不同温度、不同存放时间下的有效氯存留率:
存放时间(小时)
不同温度下,有效氯存留率
60℃
70℃
80℃
90℃
0(对照)
100%
100%
100%
100%
3.0
94.66%
88.05%
6.0
96.66%
89.67%
74.69%
12.0
93.32%
82.62%
20.0
94.75%
30.0
92.99%
【解释与结论】
84消毒液是(填“纯净物”或“混合物”)。
(2)、综合分析实验1中数据,0.5%的84消毒液有效氯存留率受温度和时间的影响,其影响的变化趋势是。(3)、保存84消毒液应注意的问题是。(4)、【实验2】不同浓度84消毒液的有效氯含量稀释体积比例(原液:水)
有效氯含量(mg/L)
使用范围
1
1:4
10000-20000
A
2
1:9
5000-10000
公共场所
3
1:100
250-400
餐饮器具
4
1:200
100-250
B
【解释与结论】
“医院血液污物”应在使用范围(填“A”或“B”)。
(5)、洁厕灵主要成分是盐酸,与84消毒液混合会产生有毒气体Cl2 , 完成反应的化学方程式: , 两者不能混合使用。(6)、桑蚕丝(主要成分是蛋白质)衣物不能使用84消毒液漂白,原因是。七、实际应用定量计算
-
36. 工业上,煅烧石灰石可制得生石灰和二氧化碳,。如果要制取2.8t氧化钙,需要碳酸钙的质量是多少?(写出计算过程及结果)
-
-