重庆市渝北区六校2022-2023学年九年级下学期第一学月大练兵化学试题
试卷更新日期:2023-06-01 类型:月考试卷
一、单选题
-
1. 下列不属于化学变化的是( )A、粮食酿酒 B、红磷燃烧 C、苹果腐烂 D、浓盐酸挥发2. 下列不能形成溶液的是( )A、碘和汽油 B、面粉和水 C、蔗糖和水 D、氯化钠和水3. “酸”对于我们来说一定不陌生。下列说法不正确的是( )A、浓硫酸具有腐蚀性 B、汽水中含有H2CO3 C、食醋使无色酚酞变红 D、稀盐酸能使紫色石蕊变红4. 正确的实验操作是科学探究成功的基础.下列操作中正确的是( )A、
 取用少量液体
B、
取用少量液体
B、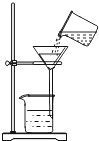 过滤
C、
过滤
C、 闻气味
D、
闻气味
D、 稀释浓硫酸
5. 下列物质属于碱的是( )A、HCl B、Al(OH)3 C、NaNO3 D、C2H5OH6. 下列物质溶于水时,溶液温度明显降低的是( )A、氯化钠 B、硝酸铵 C、浓硫酸 D、氢氧化钠7. 已知生活中一些常见食物的pH,其中酸性最强的是( )A、柠檬pH=2.3 B、菠萝pH=4.1 C、牛奶pH=6.5 D、鸡蛋清pH=7.68. 要使不饱和溶液变成饱和溶液,下面一定可行的是( )A、加溶剂 B、加溶质 C、升高温度 D、降低温度9. 下列关于溶液的叙述中,正确的是( )A、溶质一定为固体 B、饱和溶液不能再溶解任何物质 C、一定温度时,某物质的浓溶液一定是饱和溶液 D、乙醇不导电,是因为溶液中没有自由移动的离子10. 下列有关实验现象的描述中,正确的是( )A、打开盛有浓盐酸的试剂瓶,在瓶口观察到白烟 B、细铁丝在空气中燃烧,火星四射,生成黑色固体 C、氧化铜与稀硫酸反应时,黑色粉末溶解,形成蓝色溶液 D、硫在空气中燃烧,产生蓝紫色火焰,生成有刺激性气味的气体11. 某溶液的溶质质量分数为20%,则下列质量比不正确的是( )A、m(溶质):m(溶剂)=1:4 B、m(溶质):m(溶液)=1:5 C、m(溶剂):m(溶液)=4:5 D、m(溶质):m(溶剂)=1:512. 下列溶液长期露置在空气中,质量会增加且有新物质生成的是( )A、浓硫酸 B、双氧水 C、浓盐酸 D、氢氧化钠溶液13. 下列各项括号里的物质或操作是除去杂质所用的药品或方法,其中错误的是( )A、CaO中混有CaCO3(高温煅烧) B、Ca(OH)2中混有CaCO3(稀盐酸) C、Ag中混有Zn(稀盐酸) D、CO中混有CO2(氢氧化钠溶液)14. 逻辑推理是一种重要的化学思维方法,以下推理正确的是( )A、pH<7的雨水呈酸性,所以酸雨是指pH<7的雨水 B、碱的溶液中一定呈碱性,则呈碱性的溶液中一定有碱 C、中和反应生成盐和水,但生成盐和水的反应不一定是中和反应 D、铝比铁更易与氧气发生化学反应,所以在空气中铝制品比铁制品更易被腐蚀15. 验证Fe、Cu、Ag三种金属的活动性顺序,下列选项正确的是( )A、Fe、Cu、Ag、稀盐酸 B、Fe、Cu、AgNO3溶液 C、Cu、Ag、Fe(NO3)2溶液 D、Fe、Ag、Cu(NO3)2溶液16. 下列四个图象,能正确反映其对应实验操作的是( )A、
稀释浓硫酸
5. 下列物质属于碱的是( )A、HCl B、Al(OH)3 C、NaNO3 D、C2H5OH6. 下列物质溶于水时,溶液温度明显降低的是( )A、氯化钠 B、硝酸铵 C、浓硫酸 D、氢氧化钠7. 已知生活中一些常见食物的pH,其中酸性最强的是( )A、柠檬pH=2.3 B、菠萝pH=4.1 C、牛奶pH=6.5 D、鸡蛋清pH=7.68. 要使不饱和溶液变成饱和溶液,下面一定可行的是( )A、加溶剂 B、加溶质 C、升高温度 D、降低温度9. 下列关于溶液的叙述中,正确的是( )A、溶质一定为固体 B、饱和溶液不能再溶解任何物质 C、一定温度时,某物质的浓溶液一定是饱和溶液 D、乙醇不导电,是因为溶液中没有自由移动的离子10. 下列有关实验现象的描述中,正确的是( )A、打开盛有浓盐酸的试剂瓶,在瓶口观察到白烟 B、细铁丝在空气中燃烧,火星四射,生成黑色固体 C、氧化铜与稀硫酸反应时,黑色粉末溶解,形成蓝色溶液 D、硫在空气中燃烧,产生蓝紫色火焰,生成有刺激性气味的气体11. 某溶液的溶质质量分数为20%,则下列质量比不正确的是( )A、m(溶质):m(溶剂)=1:4 B、m(溶质):m(溶液)=1:5 C、m(溶剂):m(溶液)=4:5 D、m(溶质):m(溶剂)=1:512. 下列溶液长期露置在空气中,质量会增加且有新物质生成的是( )A、浓硫酸 B、双氧水 C、浓盐酸 D、氢氧化钠溶液13. 下列各项括号里的物质或操作是除去杂质所用的药品或方法,其中错误的是( )A、CaO中混有CaCO3(高温煅烧) B、Ca(OH)2中混有CaCO3(稀盐酸) C、Ag中混有Zn(稀盐酸) D、CO中混有CO2(氢氧化钠溶液)14. 逻辑推理是一种重要的化学思维方法,以下推理正确的是( )A、pH<7的雨水呈酸性,所以酸雨是指pH<7的雨水 B、碱的溶液中一定呈碱性,则呈碱性的溶液中一定有碱 C、中和反应生成盐和水,但生成盐和水的反应不一定是中和反应 D、铝比铁更易与氧气发生化学反应,所以在空气中铝制品比铁制品更易被腐蚀15. 验证Fe、Cu、Ag三种金属的活动性顺序,下列选项正确的是( )A、Fe、Cu、Ag、稀盐酸 B、Fe、Cu、AgNO3溶液 C、Cu、Ag、Fe(NO3)2溶液 D、Fe、Ag、Cu(NO3)2溶液16. 下列四个图象,能正确反映其对应实验操作的是( )A、 高温煅烧石灰石
B、
高温煅烧石灰石
B、 用等质量、等质量分数的过氧化氢溶液制取氧气
C、
用等质量、等质量分数的过氧化氢溶液制取氧气
C、 向一定体积的稀盐酸中逐滴加入氢氧化钠溶液
D、
向一定体积的稀盐酸中逐滴加入氢氧化钠溶液
D、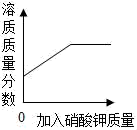 某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体
某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体
二、填空题
-
17. 日常生活与化学密切相关,请从下列四种物质中选出合适的答案,用化学式填空(1)、胃酸中含有的酸是。(2)、可改良酸性土壤的物质是。(3)、汽车用铅蓄电池中含有的物质是。(4)、炉具清洁剂中含有的、可用来除油污的物质是。18. 按要求写出下列反应的化学方程式(1)、用生石灰制取熟石灰:。(2)、实验室制取二氧化碳:。(3)、用澄清石灰水检验二氧化碳:。(4)、用氢氧化铝治疗胃酸过多症:。19. 根据你所学到的知识,按要求填空(1)、以下物质可以用作食品干燥剂的有____。A、铁粉 B、浓硫酸 C、生石灰 D、固体氢氧化钠(2)、生活中常用洗涤剂除油污是利用洗涤剂的作用。(3)、铁钉长期暴露在空气中能与空气中的反应生成铁锈;生锈的铁钉浸泡在稀硫酸中除锈的时间不宜过长,请用化学方程式说明原因。20. 如图是a、b、c三种物质的溶解度曲线,看图回答以下问题
 (1)、P点的含义是。(2)、t2℃时,三种物质溶解度由大到小依次为。(3)、t2℃时,40g的a物质加入到50g的水中充分搅拌,形成的溶液的质量为g;(4)、若a物质中混有少量b物质,提纯a物质的方法是。(填“降温结晶”或“蒸发结晶”)
(1)、P点的含义是。(2)、t2℃时,三种物质溶解度由大到小依次为。(3)、t2℃时,40g的a物质加入到50g的水中充分搅拌,形成的溶液的质量为g;(4)、若a物质中混有少量b物质,提纯a物质的方法是。(填“降温结晶”或“蒸发结晶”)三、综合题
-
21. 硫铁矿是一种宝贵资源,主要成分为二硫化亚铁(FeS2),假设其他成分不含铁和硫元素,化工生产中常用其制备氯化铁和硫酸钠,工艺流程如图。
 (1)、二硫化亚铁(FeS2)中硫元素的化合价为价。(2)、步骤Ⅱ中反应的化学方程式 , 现象固体逐渐消失,溶液逐渐变为色。(3)、A物质的俗名 , 步骤Ⅲ中反应的化学方程式。22. 如图是配制100g溶质质量分数为20%的NaCl溶液的实验操作示意图。
(1)、二硫化亚铁(FeS2)中硫元素的化合价为价。(2)、步骤Ⅱ中反应的化学方程式 , 现象固体逐渐消失,溶液逐渐变为色。(3)、A物质的俗名 , 步骤Ⅲ中反应的化学方程式。22. 如图是配制100g溶质质量分数为20%的NaCl溶液的实验操作示意图。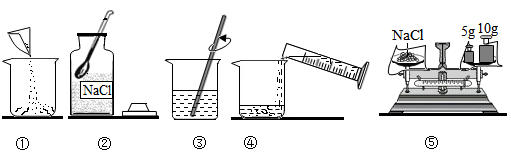 (1)、②中盛放NaCl的玻璃仪器的名称;③中玻璃棒的作用是。(2)、根据计算,应选取(填“10”“50”或“100”)mL的量筒量取所需的水。(3)、若要把配制的100g溶质质量分数为20%的NaCl溶液,稀释为10%,需要加水g。(4)、下列有关配制一定溶质质量分数的溶液的叙述中正确的是____。A、量取水时俯视读数,溶液的浓度会偏大 B、该实验的步骤依次为:计算-称量-量取-溶解-装瓶贴标签 C、若要配制一定浓度的NaOH溶液,将NaOH固体放在小纸片上称量 D、将配置好的溶液转移到试剂瓶时有少量液体溅出,会导致溶质的质量分数偏小23. 某兴趣小组同学在实验室将一定量的稀盐酸加入到盛有氢氧化钠溶液的烧杯中,未看到明显现象;此时他们对烧杯内溶液中溶质成分进行探究。(1)、写出该中和反应的化学反应方程式。(2)、该兴趣小组的同学对溶液中溶质的成分进行了如下猜想:
(1)、②中盛放NaCl的玻璃仪器的名称;③中玻璃棒的作用是。(2)、根据计算,应选取(填“10”“50”或“100”)mL的量筒量取所需的水。(3)、若要把配制的100g溶质质量分数为20%的NaCl溶液,稀释为10%,需要加水g。(4)、下列有关配制一定溶质质量分数的溶液的叙述中正确的是____。A、量取水时俯视读数,溶液的浓度会偏大 B、该实验的步骤依次为:计算-称量-量取-溶解-装瓶贴标签 C、若要配制一定浓度的NaOH溶液,将NaOH固体放在小纸片上称量 D、将配置好的溶液转移到试剂瓶时有少量液体溅出,会导致溶质的质量分数偏小23. 某兴趣小组同学在实验室将一定量的稀盐酸加入到盛有氢氧化钠溶液的烧杯中,未看到明显现象;此时他们对烧杯内溶液中溶质成分进行探究。(1)、写出该中和反应的化学反应方程式。(2)、该兴趣小组的同学对溶液中溶质的成分进行了如下猜想:猜想一:NaCl和NaOH 猜想二:NaCl
猜想三:。 猜想四:NaCl、NaOH和HCl
这时马上就有同学提出“猜想四”不合理,原因是。
(3)、实验:实验步骤
步骤Ⅰ
步骤Ⅱ
实验操作
取少量烧杯内的溶液与试管中,滴入几滴酚酞溶液,振荡
取少量烧杯中的溶液于另一只试管中,滴加碳酸钠
实验现象
①。
②。
实验结果
猜想一不成立
猜想三成立
(4)、反思:兴趣小组的同学一起回顾了酸的化学性质,提出步骤Ⅱ中可以采用其他方案证明猜想三成立,请你写出一种可行的方案。四、计算题
-
24. 波尔多液是一种运用广泛的农药,由石灰乳和硫酸铜配制而成,工厂用以下反应:来生产硫酸铜,若要制得80kg硫酸铜。试计算:(1)、硫酸铜中(填名称)元素的质量分数最小。(2)、求参加反应的氧气的质量。(3)、若恰好消耗稀硫酸的质量为600kg,求所得硫酸铜溶液中溶质的质量分数。