四川省德阳市中江县2022-2023学年九年级下学期课改教学质量监控化学练习四
试卷更新日期:2023-06-01 类型:月考试卷
一、单选题
-
1. 下列能量转化过程中,属于化学变化的是( )A、水力发电 B、利用生活垃圾发电 C、太阳能热水器供热水 D、寒冷的冬季用电热毯取暖2. “21金维他”中蕴含有铁、钾、钙等多种成分,这里的铁、钾、钙是指( )A、单质 B、元素 C、分子 D、原子3. 下列各组物质的溶液,不能发生复分解反应的是( )A、HCl与NaHCO3 B、Na2CO3与CaCl2 C、KNO3与NaCl D、KOH与CuSO44. 大雪纷飞,腊梅飘香,在腊梅花附近就能闻到花香,说明( )A、分子可以再分 B、分子间有一定的间隔 C、分子在不停地运动 D、分子的体积和质量都很小5. 在神舟十三号的太空舱里,为了保持其舱内的O2含量相对稳定,常用NiFe2O4作催化剂,将航天员呼出的CO2转化为O2 , NiFe2O4中铁为+3价,则Ni的化合价为( )A、+2 B、+1 C、+3 D、+46. 下列实验装置或操作错误的是( )A、
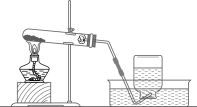 高锰酸钾制氧气
B、
高锰酸钾制氧气
B、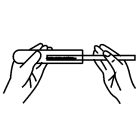 取用粉末状药品
C、
取用粉末状药品
C、 收集二氧化碳
D、
收集二氧化碳
D、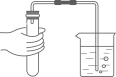 检查装置气密性
7. 下列物质溶于水后,其水溶液分别能与铁、氯化钡溶液、烧碱溶液反应的是( )A、浓盐酸 B、三氧化硫 C、氧化钙 D、硫酸钠8. 烯烃具有可燃性,某烃燃烧的化学方程式如下:2x+9O26CO2+6H2O,则x的化学式是( )A、CH4 B、C3H6 C、C4H8 D、C2H49. 已知同温同压下,相同体积的任何气体含有相同数目的分子,二氧化氮气体能与水反应,生成硝酸和不溶于水的一氧化氮气体。现将一支充满二氧化氮的试管倒扣在盛有足量水的烧杯中,最终观察到的现象是( )A、水占试管容积的 B、水占试管容积的 C、水占试管容积的 D、水充满整个试管10. 某同学在做蜡烛燃烧的探究实验时,用火柴点去蜡烛刚熄灭时的白烟,他惊奇地发现蜡烛又能重新燃烧起来。由此他大胆地推测,此白烟是( )A、氧气 B、二氧化碳 C、水 D、石蜡固体小颗粒11. 现有四种未知溶液分别是①MgCl2②CuSO4③NaOH④KNO3 , 不使用其他试剂,未知溶液被鉴别出来先后顺序是( )A、①②③④ B、④③②① C、②④①③ D、②③①④12. 将一定量的铝粉和氧化铜混合加热反应的化学方程式为:3CuO+2Al3Cu+Al2O3反应结束后,为了检验氧化铜是否完全反应,取少量反应后的固体,加入足量稀硫酸,充分反应后,将铁片插入溶液中。下列现象能说明氧化铜是否完全反应的是( )
检查装置气密性
7. 下列物质溶于水后,其水溶液分别能与铁、氯化钡溶液、烧碱溶液反应的是( )A、浓盐酸 B、三氧化硫 C、氧化钙 D、硫酸钠8. 烯烃具有可燃性,某烃燃烧的化学方程式如下:2x+9O26CO2+6H2O,则x的化学式是( )A、CH4 B、C3H6 C、C4H8 D、C2H49. 已知同温同压下,相同体积的任何气体含有相同数目的分子,二氧化氮气体能与水反应,生成硝酸和不溶于水的一氧化氮气体。现将一支充满二氧化氮的试管倒扣在盛有足量水的烧杯中,最终观察到的现象是( )A、水占试管容积的 B、水占试管容积的 C、水占试管容积的 D、水充满整个试管10. 某同学在做蜡烛燃烧的探究实验时,用火柴点去蜡烛刚熄灭时的白烟,他惊奇地发现蜡烛又能重新燃烧起来。由此他大胆地推测,此白烟是( )A、氧气 B、二氧化碳 C、水 D、石蜡固体小颗粒11. 现有四种未知溶液分别是①MgCl2②CuSO4③NaOH④KNO3 , 不使用其他试剂,未知溶液被鉴别出来先后顺序是( )A、①②③④ B、④③②① C、②④①③ D、②③①④12. 将一定量的铝粉和氧化铜混合加热反应的化学方程式为:3CuO+2Al3Cu+Al2O3反应结束后,为了检验氧化铜是否完全反应,取少量反应后的固体,加入足量稀硫酸,充分反应后,将铁片插入溶液中。下列现象能说明氧化铜是否完全反应的是( )①加入稀硫酸后,有气泡产生 ②加入稀硫酸后没有气泡产生 ③加入稀硫酸后,溶液中有红色不溶物质 ④插入溶液中的铁片表面有红色物质生成
A、①④ B、②③ C、③④ D、①③④13. 去年春季,在张献忠沉银考古现场,整齐堆放着金册、银册、金币、银币、铜币和银锭,还有铁刀、铁矛等兵器。下列说法中错误的是( )A、“真金不怕火炼”说明了黄金的化学性质稳定 B、上述钱币用金、银、铜而不用铁,从化学角度看主要原因是铁的冶炼困难 C、自然界有天然的银、金却没有天然的金属铁 D、常温下验证铁、铜、银三种金属的活动性顺序时,至少需一种金属单质14. 向一定质量FeCl2和CuCl2的混和溶液中逐渐加入足量的锌粒,下列图象不能正确反映对应关系的是( )A、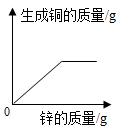
B、
B、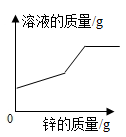
C、
C、
D、
D、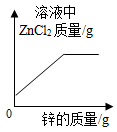
15. 有质量分数为5%的NaOH溶液100g,要将其质量分数提高到20%,则不可取的措施是( )A、加入NaOH固体18.75g B、加入质量分数为25%的NaOH溶液300g C、把溶液质量减少50g D、把溶剂蒸发掉75g16. 下列各组物质中,能共同存在于水溶液中的是( )A、BaCl2、Na2SO4、Ca(OH) 2 B、MgCl2、CuSO4、NaNO3 C、AgNO3、BaCl2、K2SO4 D、CaCl2、K2CO3、NaNO317. 下列措施不能使不饱和溶液转变为饱和溶液的是( )A、蒸发溶剂 B、增加溶质 C、改变温度 D、加速搅拌18. 下列说法正确的是( )A、某种溶液可以是稀溶液,但同时不可能是饱和溶液 B、不改变溶液的量,饱和溶液不可能变成不饱和溶液 C、浓溶液中溶解的溶质多,这时的溶液肯定是饱和溶液 D、室温下固体溶质共存的溶液是该物质的饱和溶液19. 下列物质中能与盐酸反应,生成物之一又能与石灰石反应的是( )A、Na2CO3 B、AgNO3 C、KOH D、CaO20. 下列实验所得的结论中,可靠的是( )A、加入AgNO3溶液有白色沉淀生成,则原溶液中肯定有Cl- B、加入BaCl2溶液有白色沉淀生成,继续加稀HNO3沉淀不消失,原溶液不一定含有 C、加入盐酸有能使澄清石灰水变浑浊的气体放出,原溶液中肯定没有 D、在某无色溶液中滴加酚酞试液显红色,原溶液一定是碱类物质
15. 有质量分数为5%的NaOH溶液100g,要将其质量分数提高到20%,则不可取的措施是( )A、加入NaOH固体18.75g B、加入质量分数为25%的NaOH溶液300g C、把溶液质量减少50g D、把溶剂蒸发掉75g16. 下列各组物质中,能共同存在于水溶液中的是( )A、BaCl2、Na2SO4、Ca(OH) 2 B、MgCl2、CuSO4、NaNO3 C、AgNO3、BaCl2、K2SO4 D、CaCl2、K2CO3、NaNO317. 下列措施不能使不饱和溶液转变为饱和溶液的是( )A、蒸发溶剂 B、增加溶质 C、改变温度 D、加速搅拌18. 下列说法正确的是( )A、某种溶液可以是稀溶液,但同时不可能是饱和溶液 B、不改变溶液的量,饱和溶液不可能变成不饱和溶液 C、浓溶液中溶解的溶质多,这时的溶液肯定是饱和溶液 D、室温下固体溶质共存的溶液是该物质的饱和溶液19. 下列物质中能与盐酸反应,生成物之一又能与石灰石反应的是( )A、Na2CO3 B、AgNO3 C、KOH D、CaO20. 下列实验所得的结论中,可靠的是( )A、加入AgNO3溶液有白色沉淀生成,则原溶液中肯定有Cl- B、加入BaCl2溶液有白色沉淀生成,继续加稀HNO3沉淀不消失,原溶液不一定含有 C、加入盐酸有能使澄清石灰水变浑浊的气体放出,原溶液中肯定没有 D、在某无色溶液中滴加酚酞试液显红色,原溶液一定是碱类物质二、填空题
-
21. 将一根锃亮的铁丝放入蓝色的硫酸铜溶液中,过一会儿,发现铁丝表面出现了红色物质。(1)、写出发生反应的化学方程式:。(2)、由此判断,金属的活动性:FeCu(用“>”、“=”、“<”填空)。(3)、在化学反应中,元素化合价升高的反应物是还原剂,元素化合价降低的反应物是氧化剂。试判断上述反应中,氧化剂是。22. 指出下列能量转化关系:(1)、水果电池 。(2)、钻木取火。(3)、植物光合作用。23. 近年来,我国开展垃圾分类回收。如图所示是我们鸡西市的街道垃圾桶,请回答下列问题:
 (1)、铁制外筒、塑料顶盖、铝合金内筒,图中标识的物质,属于金属材料的是 。(2)、使用铝合金做的优点是 (写出一点即可)。(3)、某品牌饮料的空易拉罐应收入 (填“可回收”或“不可回收”)筒中。(4)、铁制品锈蚀的过程,实际上是铁跟空气中的发生化学反应的过程;用稀盐酸除锈的化学方程式。24. 某同学在课外书上得知:2KClO32KCl+3O2↑,他在研究硫酸亚铁受热分解时,作了两种假设;(1)、假设它按KClO3受热分解的方式来分解,反应的方程式为:。(2)、假设它按CaCO3受热分解的方式来分解,反应的方程式为:。(3)、事实上FeSO4分解生成氧化铁、二氧化硫、三氧化硫(在500℃)反应的化学方程式为:。
(1)、铁制外筒、塑料顶盖、铝合金内筒,图中标识的物质,属于金属材料的是 。(2)、使用铝合金做的优点是 (写出一点即可)。(3)、某品牌饮料的空易拉罐应收入 (填“可回收”或“不可回收”)筒中。(4)、铁制品锈蚀的过程,实际上是铁跟空气中的发生化学反应的过程;用稀盐酸除锈的化学方程式。24. 某同学在课外书上得知:2KClO32KCl+3O2↑,他在研究硫酸亚铁受热分解时,作了两种假设;(1)、假设它按KClO3受热分解的方式来分解,反应的方程式为:。(2)、假设它按CaCO3受热分解的方式来分解,反应的方程式为:。(3)、事实上FeSO4分解生成氧化铁、二氧化硫、三氧化硫(在500℃)反应的化学方程式为:。三、综合题
-
25. A﹣G是初中化学中常见的物质,其相互反应及转化关系如图所示,部分反应条件省略。已知A是易与人体血红蛋白结合的有毒气体,B是赤铁矿的主要成分,C是相对分子质量最小的氧化物,F是最轻的气体。
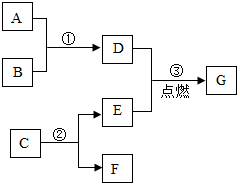 (1)、G的化学式为;(2)、反应③的实验现象是;(3)、写出相应反应的化学方程式:
(1)、G的化学式为;(2)、反应③的实验现象是;(3)、写出相应反应的化学方程式:①;
②。
26. 某硝酸钠固体中混有少量的硫酸铵和碳酸氢钠杂质。设计一种实验方案,既除去杂质,又配成硝酸钠溶液。供选用的试剂:①稀HCl ②稀HNO3 ③稀H2SO4 ④NaOH溶液 ⑤Na2CO3溶液 ⑥BaCl2溶液 ⑦Ba(OH)2溶液 ⑧Ba(NO3)2溶液
供选用的实验操作:A、加热 B、过滤 C、蒸发 D、结晶 E、蒸馏
实验方案:先将固体溶于蒸馏水配成溶液,然后填表完成各步实验(填序号,要求试剂不超过3种)
选择试剂和实验操作
27. 下图是某同学探究氢氧化钠、氢氧化铜性质的操作过程示意图,请回答: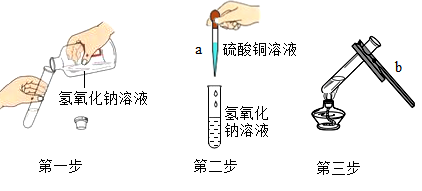 (1)、编号仪器的名称:a是;b是 。(2)、操作中没有错误的步骤是 , 其化学反应方程式是 。(3)、当第三步操作正确时,则试管内会发生分解反应,且产物是氧化铜和水,则第三步操作中观察到的现象是。28. 冶炼金属的方法有很多,多数金属的冶炼过程属于热还原法。常用的还原剂有焦炭、一氧化碳、氢气及活泼金属等。浓硫酸与乙二酸在加热条件下发生如下的反应:H2C2O4CO2↑+CO↑+H2O↑,有人利用此反应产生的CO还原氧化铁,并设计了下图所示的装置。其中A和F各盛有浓硫酸,烧瓶B中盛有乙二酸,D中盛有NaOH浓溶液,E和I中各盛有澄清的石灰水,H中装有氧化铁的粉末。
(1)、编号仪器的名称:a是;b是 。(2)、操作中没有错误的步骤是 , 其化学反应方程式是 。(3)、当第三步操作正确时,则试管内会发生分解反应,且产物是氧化铜和水,则第三步操作中观察到的现象是。28. 冶炼金属的方法有很多,多数金属的冶炼过程属于热还原法。常用的还原剂有焦炭、一氧化碳、氢气及活泼金属等。浓硫酸与乙二酸在加热条件下发生如下的反应:H2C2O4CO2↑+CO↑+H2O↑,有人利用此反应产生的CO还原氧化铁,并设计了下图所示的装置。其中A和F各盛有浓硫酸,烧瓶B中盛有乙二酸,D中盛有NaOH浓溶液,E和I中各盛有澄清的石灰水,H中装有氧化铁的粉末。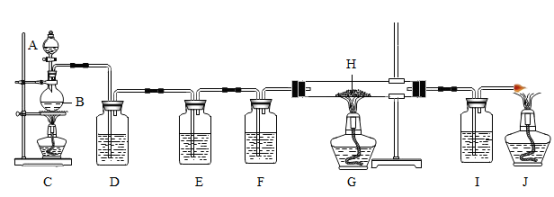 (1)、D装置的作用是;E装置的作用是。(2)、I装置的作用是;J装置的作用是。(3)、为了节能降耗,提出一条改进本实验装备的建议。(4)、冶炼金属一般有下列三种方法:①热分解法、②热还原法、③电解法。有下面三种金属制备方法:Ⅰ用焦炭与氧化铜共热炼铜、Ⅱ湿法炼铜、Ⅲ铝热法炼铬。下列对三种金属制备方法分类不正确的是____。A、Ⅰ③ B、Ⅱ③ C、Ⅲ②
(1)、D装置的作用是;E装置的作用是。(2)、I装置的作用是;J装置的作用是。(3)、为了节能降耗,提出一条改进本实验装备的建议。(4)、冶炼金属一般有下列三种方法:①热分解法、②热还原法、③电解法。有下面三种金属制备方法:Ⅰ用焦炭与氧化铜共热炼铜、Ⅱ湿法炼铜、Ⅲ铝热法炼铬。下列对三种金属制备方法分类不正确的是____。A、Ⅰ③ B、Ⅱ③ C、Ⅲ②四、计算题
-
29. 某石化厂有一种石油产品含有溶质质量分数为4.9%的残余硫酸,过去他们都是用NaOH溶液来清洗这些硫酸。计算:(1)、如果清洗100kg这种石油产品,要多少千克的NaOH?(2)、该石化厂的工人经过技术改造,采用Ca(OH)2来中和这些残余硫酸。如处理100kg这种石油产品,可以节约多少经费?
温馨提示:和市场价格如下表:
名称
NaOH
Ca(OH)2
价格(元/kg)
24.00
6.00