江苏省南京市金中集团联考2022-2023学年九年级下学期学情调研(第一次月考)化学试题
试卷更新日期:2023-06-01 类型:月考试卷
一、单选题
-
1. 人体中含量最高的金属元素是( )A、O B、Fe C、Ca D、Na2. 下列常见材料中,属于合成材料的是( )A、不锈钢 B、焊锡 C、钢筋混凝士 D、塑料3. 下列化肥属于复合肥料的是( )A、KCl B、Ca2(PO4)3 C、KNO3 D、CO(NH2)24. 下列物质由分子构成的是( )A、锌 B、硫酸铜 C、水 D、氯化钠5. 下列粒子结构示意图中表示阴离子的是( )A、
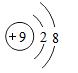 B、
B、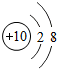 C、
C、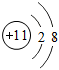 D、
D、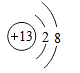 6. 目前,金属材料顶级期刊《Acta材料》刊登我国科学家成功研制用于外太空核反应堆的高强韧钼合金。相元素在元素周期表中的信息如图所示,下列说法正确的是( )
6. 目前,金属材料顶级期刊《Acta材料》刊登我国科学家成功研制用于外太空核反应堆的高强韧钼合金。相元素在元素周期表中的信息如图所示,下列说法正确的是( )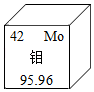 A、钼原子的最外层电子数为42 B、钼的元素符号为Mo C、钼的相对原子质量为95.96g D、钼属于非金属元素7. 下列有关加热高锰酸钾制取氧气的实验操作正确的是( )A、组装仪器
A、钼原子的最外层电子数为42 B、钼的元素符号为Mo C、钼的相对原子质量为95.96g D、钼属于非金属元素7. 下列有关加热高锰酸钾制取氧气的实验操作正确的是( )A、组装仪器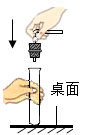 B、检查气密性
B、检查气密性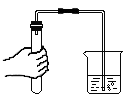 C、加热固体
C、加热固体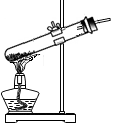 D、氧气验满
D、氧气验满 8. 下列物质的名称、俗称、用途有错误的是( )A、氧化钙—生石灰—作干燥剂 B、氢氧化钠—火碱—制肥皂 C、碳酸钠—烧碱—制玻璃 D、碳酸氢钠—小苏打—烘焙糕点9. 下列各组离子在溶液中能大量共存的是( )A、、、、Cl- B、H+、Ba2+、OH-、 C、Cu2+、Na+、、OH- D、Ca2+、Cl-、、K+10. 丙氨酸(C3H7O2N)是一种常见的氨基酸。下列叙述正确的是( )A、每个丙氨酸分子中含有1个氧分子 B、丙氨酸中碳、氮元素的质量比为3:1 C、丙氨酸属于有机小分子化合物 D、丙氨酸是由3个碳原子,7个氢原子,2个氧原子,1个氮原子构成11. 下列关于燃烧和灭火的说法中,不正确的是( )A、点燃前氢气要验纯,以防爆炸 B、二氧化碳灭火器可以用来扑灭图书的失火 C、一阵风吹熄蜡烛,其主要的灭火原理是隔绝氧气 D、灭火的原理是破坏燃烧的三个条件之一即可12. 生产VR(虚拟现实)设备的材料之一是硅(Si),工业制取高纯硅的微观示意图如图。下列有关说法不正确的是( )
8. 下列物质的名称、俗称、用途有错误的是( )A、氧化钙—生石灰—作干燥剂 B、氢氧化钠—火碱—制肥皂 C、碳酸钠—烧碱—制玻璃 D、碳酸氢钠—小苏打—烘焙糕点9. 下列各组离子在溶液中能大量共存的是( )A、、、、Cl- B、H+、Ba2+、OH-、 C、Cu2+、Na+、、OH- D、Ca2+、Cl-、、K+10. 丙氨酸(C3H7O2N)是一种常见的氨基酸。下列叙述正确的是( )A、每个丙氨酸分子中含有1个氧分子 B、丙氨酸中碳、氮元素的质量比为3:1 C、丙氨酸属于有机小分子化合物 D、丙氨酸是由3个碳原子,7个氢原子,2个氧原子,1个氮原子构成11. 下列关于燃烧和灭火的说法中,不正确的是( )A、点燃前氢气要验纯,以防爆炸 B、二氧化碳灭火器可以用来扑灭图书的失火 C、一阵风吹熄蜡烛,其主要的灭火原理是隔绝氧气 D、灭火的原理是破坏燃烧的三个条件之一即可12. 生产VR(虚拟现实)设备的材料之一是硅(Si),工业制取高纯硅的微观示意图如图。下列有关说法不正确的是( )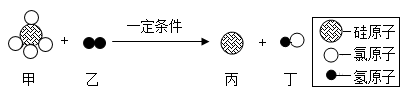 A、甲属于化合物 B、反应中乙和丁的分子个数比为1:2 C、反应前后氢、氯原子个数不发生改变 D、参加反应的甲和乙的质量比为85:113. 下列除杂试剂和方法正确的是( )
A、甲属于化合物 B、反应中乙和丁的分子个数比为1:2 C、反应前后氢、氯原子个数不发生改变 D、参加反应的甲和乙的质量比为85:113. 下列除杂试剂和方法正确的是( )选项
物质(括号内为杂质)
加入的除杂试剂及方法
A
CO2(CO)
O2、点燃
B
CaO(CuO)
加水溶解、过滤
C
FeCl2溶液(CuCl2)
加过量铁粉、过滤
D
稀硫酸(盐酸)
加适量AgNO3溶液、过滤
A、A B、B C、C D、D14. 甲、乙、丙、丁是初中化学常见物质,其反应可表示为甲+乙→丙+丁、下列推测正确的是( )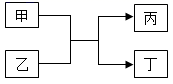 A、若甲、乙是化合物,则丙、丁也一定是化合物 B、若甲为单质,则此反应一定是置换反应 C、若乙为稀硫酸,则丙、丁中一定有盐 D、若丙为氯化钠,则甲、乙中一定有碱15. 以FeSO4为原料制备铁黑颜料Fe3O4(其中Fe既有+2价,也有+3价)的过程如下:
A、若甲、乙是化合物,则丙、丁也一定是化合物 B、若甲为单质,则此反应一定是置换反应 C、若乙为稀硫酸,则丙、丁中一定有盐 D、若丙为氯化钠,则甲、乙中一定有碱15. 以FeSO4为原料制备铁黑颜料Fe3O4(其中Fe既有+2价,也有+3价)的过程如下: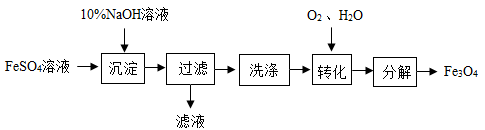
“转化”过程的反应为: ;若原料中含FeSO4质量为9.12t,下列说法错误的是( )
A、理论上“转化”过程参与反应的O2的质量为320kg B、理论上与FeSO4反应的NaOH溶液的质量为4.8t C、该方法理论上最终可以获得Fe3O4的质量为4.64t D、若“转化”过程参与反应的O2过量,则最终所得固体的质量偏大二、填空题
-
16. 化学就在我们身边,人类的生活离不开化学。(1)、新鲜的蔬菜、水果中富含的营养素主要是水和。(2)、目前人们使用的燃料大多来自化石燃料,如:、石油和天然气。(3)、冬奥会上提供经过二氧化氯消毒处理的直饮水,请写出二氧化氯的化学式,并标出氯元素的化合价:。(4)、儿童缺少元素,会引起食欲不振,生长迟缓,发育不良。(5)、铁在空气中锈蚀生成铁锈,铁锈的主要成分是(填化学式)。(6)、若要鉴别氯化铵和氯化钾两种固体,通常可采用的方法是。
三、综合题
-
17. 下图是实验室制取气体常用的装置,结合图示回答下列问题。
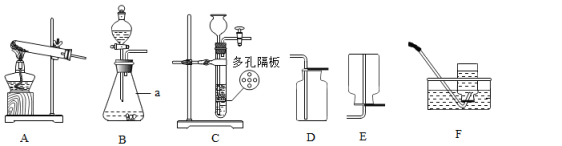 (1)、写出装置图中标号仪器的名称:a。(2)、实验室可以用装置A制取氧气,该反应的化学方程式为 , 可以用装置F收集氧气,原因是。(3)、实验室可以用装置C制取二氧化碳,多孔隔板上放置的药品是 , 打开活塞,从长颈漏斗加入的药品是。该反应的化学方程式为 , 一段时间后,关闭活塞,可以观察到的现象是。18. 溶液与人类生产、生活密切相关。(1)、把少量下列物质分别放入水中,充分搅拌,能得到溶液的是____(填序号)。A、硝酸钾 B、植物油 C、面粉 D、蔗糖(2)、按图中所示装置,将x加入装有y的试管中,会导致U形管中右端液面升高,则可能的组合是____(填字母)
(1)、写出装置图中标号仪器的名称:a。(2)、实验室可以用装置A制取氧气,该反应的化学方程式为 , 可以用装置F收集氧气,原因是。(3)、实验室可以用装置C制取二氧化碳,多孔隔板上放置的药品是 , 打开活塞,从长颈漏斗加入的药品是。该反应的化学方程式为 , 一段时间后,关闭活塞,可以观察到的现象是。18. 溶液与人类生产、生活密切相关。(1)、把少量下列物质分别放入水中,充分搅拌,能得到溶液的是____(填序号)。A、硝酸钾 B、植物油 C、面粉 D、蔗糖(2)、按图中所示装置,将x加入装有y的试管中,会导致U形管中右端液面升高,则可能的组合是____(填字母)选项
X
y
A
稀盐酸
镁
B
浓硫酸
水
C
水
硝酸铵
D
水
氧化钙
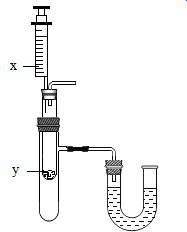 A、A B、B C、C D、D(3)、如图为a、b、c三种固体物质的溶解度曲线。
A、A B、B C、C D、D(3)、如图为a、b、c三种固体物质的溶解度曲线。
①P点的含义是。
②t2℃时,一定质量a物质的饱和溶液,从t2℃降温至t1℃,析出15g物质a,则该溶液中溶剂水的质量为。
③将c的饱和溶液转化为c的不饱和溶液的操作是。
④下列说法正确的是。
A.t1℃时,三种物质的溶解度:b>a-=c
B.t1℃时,将30g物质a放入50g水中,充分搅拌,所得溶液的质量是80g
C.分别将t2℃时三种物质的饱和溶液降温到t1℃,a溶液中析出的晶体质量最大
D.分别将t2℃时三种物质的饱和溶液降温到t1℃,溶液中溶质的质量分数:b>a>c
(4)、将5.4g铝粉平均分成两份,进行如下实验。①一份在足量氧气中加热至完全反应,理论上生成氧化铝固体的质量是。
②另一份与溶质质量分数为9.8%的稀硫酸溶液反应,生成硫酸铝和氢气。若铝粉完全反应,理论上需要9.8%的稀硫酸的质量至少为多少?(在答题卡上写出计算过程)
19. 中国航天工业飞速发展,金属钛常被用于航空航天工业,下图是以钛铁矿为主要原料冶炼金属钛的生产工艺流程:已知:①钛铁矿主要成分为钛酸亚铁(FeTiO3);②钛酸(H2TiO3)是一种难溶于水的白色固体。请回答下列问题: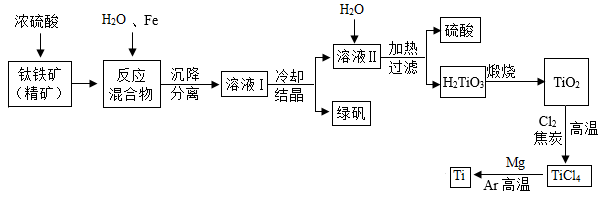 (1)、FeTiO3中钛元素的化合价为 , 钛铁矿溶浸在浓硫酸中发生反应, 反应前需将钛铁矿粉碎的目的是。(2)、溶液Ⅱ的主要溶质为TiOSO4 , 加热时和水发生反应生成钛酸,操作I的名称是。(3)、TiO2、Cl2和焦炭发生反应, , X的化学式为。(4)、流程中,在氩气的保护和高温条件下,四氯化钛(TiCl4)与镁反应制得钛(Ti)的化学方程式为。20. 小明在学完初中化学知识后,把常见八种化合物(酸、碱、盐、氧化物)的相互关系连接成如图所示。图中A~H是初中常见物质,且分别是由H、C、O、N、Na、Ca、S、Cl中的一种或几种元素组成。已知F、G、H三种物质的类别相同,只有A、C是由两种元素组成。A是最常见的一种溶剂、也是人体中含量最多的物质;F广泛应用于玻璃、造纸、纺织和洗涤剂生产。图中“一”表示两端的物质间能发生化学反应,“→”表示物质间存在转化关系:部分反应物、生成物或反应条件已略去。
(1)、FeTiO3中钛元素的化合价为 , 钛铁矿溶浸在浓硫酸中发生反应, 反应前需将钛铁矿粉碎的目的是。(2)、溶液Ⅱ的主要溶质为TiOSO4 , 加热时和水发生反应生成钛酸,操作I的名称是。(3)、TiO2、Cl2和焦炭发生反应, , X的化学式为。(4)、流程中,在氩气的保护和高温条件下,四氯化钛(TiCl4)与镁反应制得钛(Ti)的化学方程式为。20. 小明在学完初中化学知识后,把常见八种化合物(酸、碱、盐、氧化物)的相互关系连接成如图所示。图中A~H是初中常见物质,且分别是由H、C、O、N、Na、Ca、S、Cl中的一种或几种元素组成。已知F、G、H三种物质的类别相同,只有A、C是由两种元素组成。A是最常见的一种溶剂、也是人体中含量最多的物质;F广泛应用于玻璃、造纸、纺织和洗涤剂生产。图中“一”表示两端的物质间能发生化学反应,“→”表示物质间存在转化关系:部分反应物、生成物或反应条件已略去。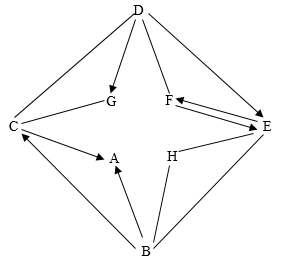 (1)、写出A的化学式 , D的俗名。(2)、写出B→C的化学方程式。(3)、写出D→E反应的化学方程式。(4)、G一C的基本反应类型是。21. 某化学兴趣小组用图1所示的装置,对氢氧化钙溶液进行探究
(1)、写出A的化学式 , D的俗名。(2)、写出B→C的化学方程式。(3)、写出D→E反应的化学方程式。(4)、G一C的基本反应类型是。21. 某化学兴趣小组用图1所示的装置,对氢氧化钙溶液进行探究【查阅资料】溶液的导电能力越强,溶液的电导率越大。单位体积溶液中某离子的个数越多,则该离子的浓度越大,溶液的导电能力越强。
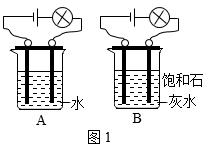 (1)、在图1的A、B两个相同装置中,分别放入等体积的水和饱和石灰水,通电,发现B装置灯泡更亮,原因是。(2)、接通直流电,同时利用温度传感器测量溶液的温度。观察到B装置中插入溶液的两个碳棒(石墨)电极附近有气泡产生,一段时间后发现烧杯中的溶液的温度由24℃变为28℃,同时出现白色浑浊,这可能是因为析出了氢氧化钙固体,析出氢氧化钙固体的原因可能是 , 还可能是。(3)、仔细观察,发现B装置中,白色浑浊出现在正极附近。联想电解水时,与电源正极相连的电极附近产生的(请用化学式表示,下同),它可能与石墨电极中的碳反应生成二氧化碳而使石灰水变浑浊,如果假设成立,则最后一步反应的化学方程式为。为了验证白色浑浊液体的成分,取上述实验得到的浑浊液体少量,滴加酚酞变红色,说明浑浊液体中还存在。(4)、将B装置中剩余浑浊液搅拌均匀后分成等体积的两份,第一组同学取一份加入一定量的稀盐酸,没有发现气泡产生。第二组同学取另一份倒入密封的三颈烧瓶中进行数字化实验。连接好传感器等装置,先开启测量二氧化碳含量的数据传感器,然后用注射器注入足量的稀盐酸数字化实验装置及所测量到的二氧化碳体积分数变化情况如图2。
(1)、在图1的A、B两个相同装置中,分别放入等体积的水和饱和石灰水,通电,发现B装置灯泡更亮,原因是。(2)、接通直流电,同时利用温度传感器测量溶液的温度。观察到B装置中插入溶液的两个碳棒(石墨)电极附近有气泡产生,一段时间后发现烧杯中的溶液的温度由24℃变为28℃,同时出现白色浑浊,这可能是因为析出了氢氧化钙固体,析出氢氧化钙固体的原因可能是 , 还可能是。(3)、仔细观察,发现B装置中,白色浑浊出现在正极附近。联想电解水时,与电源正极相连的电极附近产生的(请用化学式表示,下同),它可能与石墨电极中的碳反应生成二氧化碳而使石灰水变浑浊,如果假设成立,则最后一步反应的化学方程式为。为了验证白色浑浊液体的成分,取上述实验得到的浑浊液体少量,滴加酚酞变红色,说明浑浊液体中还存在。(4)、将B装置中剩余浑浊液搅拌均匀后分成等体积的两份,第一组同学取一份加入一定量的稀盐酸,没有发现气泡产生。第二组同学取另一份倒入密封的三颈烧瓶中进行数字化实验。连接好传感器等装置,先开启测量二氧化碳含量的数据传感器,然后用注射器注入足量的稀盐酸数字化实验装置及所测量到的二氧化碳体积分数变化情况如图2。
实验结论:第二组同学通过图像分析说明白色浑浊溶液中存在(除水外)
实验反思:
①第一组同学的实验中,没有发现产生气泡,原因可能是。
②第二组同学在数字化实验中,发现曲线图开始时段的CO2百分比下降,可能的原因是。
-