湖北省荆门市沙洋县国道片区2022-2023学年九年级下学期3月月考化学试题
试卷更新日期:2023-06-01 类型:月考试卷
一、单选题
-
1. 下列物质的用途利用了物质的化学性质的是( )A、活性炭除去房间中的异味 B、用煤、石油、天然气作燃料 C、干冰用于冷藏食品 D、用铜或铝制作导线2. 下列实验操作正确的是( )A、过滤
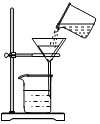 B、倾倒液体
B、倾倒液体 C、测量液体pH
C、测量液体pH D、稀释浓硫酸
D、稀释浓硫酸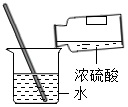 3. 2019年4月25日是第12个世界疟疾日,中国中医科学院青蒿素研究中心和中药研究所的科学家们在国际权威期刊《新英格兰医学杂志》上提出了“青蒿素抗药性”的合理应对方案。青蒿素的分子式为 ,关于青蒿素的说法错误的是( )A、青蒿素由三种元素组成 B、每个青蒿素分子由42个原子构成 C、青蒿素中碳元素和氧元素的质量比为3:1 D、青蒿素的相对分子质量为2824. 下列有关燃烧与灭火的说法正确的是( )A、通过降低可燃物的着火点可以灭火 B、吹灭燃着蜡烛的灭火原理是隔绝氧气 C、室内起火应迅速开所有门窗通风 D、面粉厂、加油站等场所应严禁烟火5. 硒元素是动物体必需营养元素和植物有益的营养元素。硒在元素周期表中的信息及原子结构示意图如图所示。下列关于硒元素的说法错误的是( )
3. 2019年4月25日是第12个世界疟疾日,中国中医科学院青蒿素研究中心和中药研究所的科学家们在国际权威期刊《新英格兰医学杂志》上提出了“青蒿素抗药性”的合理应对方案。青蒿素的分子式为 ,关于青蒿素的说法错误的是( )A、青蒿素由三种元素组成 B、每个青蒿素分子由42个原子构成 C、青蒿素中碳元素和氧元素的质量比为3:1 D、青蒿素的相对分子质量为2824. 下列有关燃烧与灭火的说法正确的是( )A、通过降低可燃物的着火点可以灭火 B、吹灭燃着蜡烛的灭火原理是隔绝氧气 C、室内起火应迅速开所有门窗通风 D、面粉厂、加油站等场所应严禁烟火5. 硒元素是动物体必需营养元素和植物有益的营养元素。硒在元素周期表中的信息及原子结构示意图如图所示。下列关于硒元素的说法错误的是( )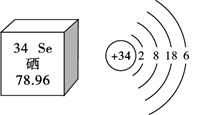 A、硒的原子序数为34 B、硒的相对原子质量是78.96 C、硒在化学反应中容易失去电子 D、硒化氢的化学式是H2Se6. 如图是某反应的微观示意图。下列说法不正确的是( )
A、硒的原子序数为34 B、硒的相对原子质量是78.96 C、硒在化学反应中容易失去电子 D、硒化氢的化学式是H2Se6. 如图是某反应的微观示意图。下列说法不正确的是( )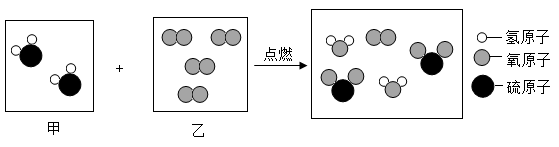 A、反应后硫元素化合价升高 B、生成物均为氧化物 C、反应后分子总数减少 D、参加反应的甲、乙分子个数比为1:27. 某同学在探究X、Y、Z三种金属的活动性顺序时,做了如下实验,①把X和Y分别放入稀硫酸中。X表面产生大量气泡,Y表面无明显现象:②将Y放入Z的硝酸盐溶液中,Y表面有Z析出。下列金属活动性由强到弱的顺序正确的是( )A、Z>Y>X B、X>Z>Y C、X>Y>Z D、Y>Z>X8. 下列各组离子在溶液中能大量共存的是( )A、Ag+、OH﹣、Cl﹣ B、K+、、 C、Cu2+、Na+、OH﹣ D、Ca2+、K+、9. 以下推理合理的是( )A、中和反应生成盐和水,所以凡是生成盐和水的反应都是中和反应 B、碱溶液一定显碱性,所以显碱性的溶液一定是碱溶液 C、阳离子是带正电荷的粒子,所以带正电荷的粒子一定是阳离子 D、由不同种元素组成的纯净物是化合物,所以化合物一定含有不同种元素10. 下列实验方案合理可行的是( )
A、反应后硫元素化合价升高 B、生成物均为氧化物 C、反应后分子总数减少 D、参加反应的甲、乙分子个数比为1:27. 某同学在探究X、Y、Z三种金属的活动性顺序时,做了如下实验,①把X和Y分别放入稀硫酸中。X表面产生大量气泡,Y表面无明显现象:②将Y放入Z的硝酸盐溶液中,Y表面有Z析出。下列金属活动性由强到弱的顺序正确的是( )A、Z>Y>X B、X>Z>Y C、X>Y>Z D、Y>Z>X8. 下列各组离子在溶液中能大量共存的是( )A、Ag+、OH﹣、Cl﹣ B、K+、、 C、Cu2+、Na+、OH﹣ D、Ca2+、K+、9. 以下推理合理的是( )A、中和反应生成盐和水,所以凡是生成盐和水的反应都是中和反应 B、碱溶液一定显碱性,所以显碱性的溶液一定是碱溶液 C、阳离子是带正电荷的粒子,所以带正电荷的粒子一定是阳离子 D、由不同种元素组成的纯净物是化合物,所以化合物一定含有不同种元素10. 下列实验方案合理可行的是( )选项
实验目的
所用试剂或操作方法
A
鉴别稀盐酸、NaOH溶液和蒸馏水
分别滴加无色酚酞溶液,观察颜色
B
除去硝酸钠溶液中的硫酸钠
加入适量氯化钡溶液,过滤
C
验证Zn、Cu、Ag的金属活动性
将铜片分别放入到Zn(NO3)2溶液,AgNO3溶液中,观察现象
D
除去CO2中混有少量的HCl气体
将气体通入足量的NaOH溶液
A、A B、B C、C D、D二、填空题
-
11. 化学就在我们身边,人类的衣、食、住、行都离不开化学。(1)、杂交水稻之父袁隆平说“人就像一粒种子,要做一粒好的种子”、水稻种子的主要成分为淀粉,淀粉属于____营养物质。A、蛋白质 B、糖类 C、油脂 D、维生素(2)、碱性甲烷燃料电池具有低污染、高效率等特点,是一种很有前途的能源利用方式。
①电池总反应方程式为CH4+2O2+2KOH═K2CO3+3X,则X的化学式为。
②草木灰的成分中含有K2CO3 , 可以作钾肥,其中K2CO3属于(填物质类别),其中碳元素化合价为。
(3)、4500L氧气可加压装入容积为30L钢瓶中,其原因是(从微观角度解)。(4)、区分自来水是硬水还是软水,最简单的方法是用试剂来检验。12. 如图是a、b、c三种物质(均不含结晶水)的溶解度曲线,根据如图回答下列问题。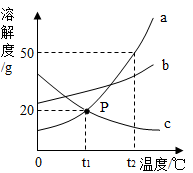 (1)、P点的含义是。(2)、在不改变溶液质量的情况下,将接近饱和的a溶液变成饱和溶液可采用的方法是。(3)、t2℃时,将50g a物质加入到50g水中,充分搅拌溶解后恢复到原温度,所得溶液质量是。(4)、t2℃时,将a、b、c三种物质的等质量的饱和溶液降温至t1℃,下列说法正确的是____。A、此时的溶液都是饱和溶液 B、溶质质量分数大小关系是:b>a>c C、析出晶体质量最多的是a13. 根据下列装置图,结合所学知识,请回答下列问题:
(1)、P点的含义是。(2)、在不改变溶液质量的情况下,将接近饱和的a溶液变成饱和溶液可采用的方法是。(3)、t2℃时,将50g a物质加入到50g水中,充分搅拌溶解后恢复到原温度,所得溶液质量是。(4)、t2℃时,将a、b、c三种物质的等质量的饱和溶液降温至t1℃,下列说法正确的是____。A、此时的溶液都是饱和溶液 B、溶质质量分数大小关系是:b>a>c C、析出晶体质量最多的是a13. 根据下列装置图,结合所学知识,请回答下列问题: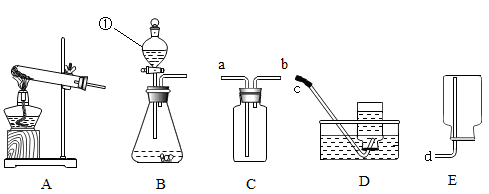 (1)、仪器①的名称为(2)、实验室选A装置用高锰酸钾制取O2时,相应反应的化学方程式为A装置存在的不足之处是(3)、实验室制取CO2气体的发生装置通常选用的是(用字母A~E填空);选择恰当的CO2气体收集装置,CO2气体应该从(用字母ab填空)导入。14. 初中化学常见物质的转化关系如图,部分反应物、生成物和反应条件未标出。其中D与E的组成元素相同,B、D、E在通常状况下是气体,F可用来改良酸性土壤,G是石灰石的主要成分,M是一种黑色固体粉末。
(1)、仪器①的名称为(2)、实验室选A装置用高锰酸钾制取O2时,相应反应的化学方程式为A装置存在的不足之处是(3)、实验室制取CO2气体的发生装置通常选用的是(用字母A~E填空);选择恰当的CO2气体收集装置,CO2气体应该从(用字母ab填空)导入。14. 初中化学常见物质的转化关系如图,部分反应物、生成物和反应条件未标出。其中D与E的组成元素相同,B、D、E在通常状况下是气体,F可用来改良酸性土壤,G是石灰石的主要成分,M是一种黑色固体粉末。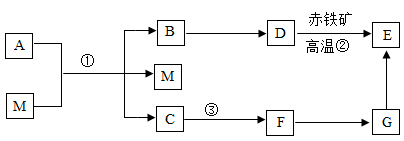
请完成下列问题:
(1)、写出物质的化学式G。(2)、物质M在反应①中所起的作用是。(3)、写出下列反应的化学方程式:②。
③。
15. 在学习了常见的酸和碱后,某化学兴趣小组的同学围绕“酸碱中和反应”,在老师引导下开展实验探究活动,请你参与下列活动。(1)、【实验探究】将稀硫酸与氢氧化钾溶液混合,观察不到明显现象,为证明稀硫酸与氢氧化钾溶液发生了反应,某兴趣小组同学进行了以下实验。测定溶液pH变化的方法
甲同学在实验过程中测得pH变化如图1所示,则该同学是将(填字母序号)。

a.稀硫酸滴入氢氧化钾溶液中 b.氢氧化钾溶液滴入稀硫酸中
(2)、借助于酸碱指示剂
乙同学通过图所示实验,他观察到溶液由红色变成无色,也证明氢氧化钾溶液与稀硫酸发生了化学反应,反应的化学方程式为。
(3)、【提出问题】针对图反应后无色溶液中溶质的成分,丙同学提出了猜想。【猜想与假设】
猜想一:;猜想二:有K2SO4和H2SO4
【进行实验】为了验证猜想,学习小组选用适当药品,进行如下探究:
实验方案
实验操作
实验现象
实验结论
方案1
取少量反应后的溶液于试管中,加入
有气泡冒出
溶液中有H2SO4 , 猜想二正确
方案2
取少量反应后的溶液于试管中,滴加BaCl2溶液
溶液中有H2SO4 , 猜想二正确
【实验结论】通过探究,同学们一致确定猜想二是正确的。
(4)、【评价与反思】丁同学针对上述方案提出疑问,认为(选填“方案1”或“方案2”)是不合理的,理由是。
三、计算题
-
16. 将含有少量Na2SO4的NaCl样品10 g溶于80 g水,再向其中滴加70 g BaCl2溶液,恰好完全反应,过滤后称得滤液的质量为157.67 g,计算:(1)、样品中Na2SO4的质量(2)、滤液中溶质的质量