福建省厦门市海沧区2022-2023学年九年级下学期3月月考化学试题
试卷更新日期:2023-06-01 类型:月考试卷
一、单选题
-
1. 科学防控疫情,健康与我同行。疫情防护期间,下列日常活动中涉及化学变化的是( )A、用体温计测量体温 B、用医用酒精对手消毒 C、出示动态行程卡 D、佩戴防护口罩2. 用纳米材料制成的用品具有很多奇特的性质。例如,纳米铜在室温下可拉长50多倍而不出现裂纹,这利用了它的( )A、导电性 B、导热性 C、延展性 D、硬度大3. 烧杯是化学实验中常用的实验仪器,下列有关烧杯的实验操作中正确的是( )A、稀释浓硫酸
 B、加热液体
B、加热液体 C、称量氢氧化钠固体
C、称量氢氧化钠固体 D、过滤浑浊的天然水
D、过滤浑浊的天然水 4. 建构模型是学习化学的重要方法。下列模型与说法匹配的是( )A、
4. 建构模型是学习化学的重要方法。下列模型与说法匹配的是( )A、 四个氧原子模型
B、
四个氧原子模型
B、 地壳中元素含量模型
C、
地壳中元素含量模型
C、 物质分类模型
D、
物质分类模型
D、 空气成分模型
5. 纳米技术是研究结构尺寸在0.1-100nm范围内材料的性质和应用。下图为某纳米小人(C39H42O2)的结构简式。下列说法正确的是( )
空气成分模型
5. 纳米技术是研究结构尺寸在0.1-100nm范围内材料的性质和应用。下图为某纳米小人(C39H42O2)的结构简式。下列说法正确的是( ) A、C39H42O2中碳、氢元素的质量比为78:7 B、一个该分子中含有84个原子 C、研究纳米技术可实现对整个微观世界的有效控制 D、该分子由碳、氢、氧三种元素组成6. 化学学习者常用化学学科观念去认识和理解世界,下列说法错误的是( )A、变化与守恒:某物质在氧气中充分燃烧后生成CO2和H2O,可推知该物质中含有碳、氢、氧元素 B、模型与推理:碱溶液能使酚酞溶液变红,NaOH是碱,可知NaOH溶液能使酚酞溶液变红 C、宏观与微观:H2O和H2O2化学性质不同,是因为它们的分子构成不同 D、探究与创新:将燃着的镁条伸入充满CO2的集气瓶中,镁条继续燃烧,瓶壁出现黑色物质,可推知CO2在一定条件下可以支持燃烧7. 某口罩中使用了MOF催化过滤材料,在潮湿空气中臭氧去除率可达100%,反应的微观过程如图所示。下列说法中正确的是( )
A、C39H42O2中碳、氢元素的质量比为78:7 B、一个该分子中含有84个原子 C、研究纳米技术可实现对整个微观世界的有效控制 D、该分子由碳、氢、氧三种元素组成6. 化学学习者常用化学学科观念去认识和理解世界,下列说法错误的是( )A、变化与守恒:某物质在氧气中充分燃烧后生成CO2和H2O,可推知该物质中含有碳、氢、氧元素 B、模型与推理:碱溶液能使酚酞溶液变红,NaOH是碱,可知NaOH溶液能使酚酞溶液变红 C、宏观与微观:H2O和H2O2化学性质不同,是因为它们的分子构成不同 D、探究与创新:将燃着的镁条伸入充满CO2的集气瓶中,镁条继续燃烧,瓶壁出现黑色物质,可推知CO2在一定条件下可以支持燃烧7. 某口罩中使用了MOF催化过滤材料,在潮湿空气中臭氧去除率可达100%,反应的微观过程如图所示。下列说法中正确的是( )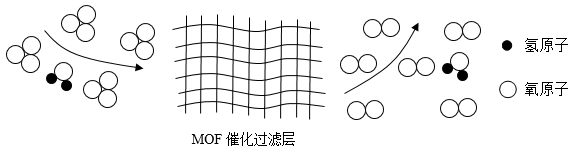 A、该反应属于化合反应 B、臭氧全部转化生成了氧气 C、氧元素化合价发生改变 D、经上述过滤后的气体属于纯净物8. 20℃时,向盛有100g水的烧杯中加入60 g ZnSO4进行实验(忽略水的蒸发)。依据下图所示的实验和ZnSO4溶解度曲线,下列说法正确的是( )
A、该反应属于化合反应 B、臭氧全部转化生成了氧气 C、氧元素化合价发生改变 D、经上述过滤后的气体属于纯净物8. 20℃时,向盛有100g水的烧杯中加入60 g ZnSO4进行实验(忽略水的蒸发)。依据下图所示的实验和ZnSO4溶解度曲线,下列说法正确的是( )
 A、20℃时,充分搅拌后烧杯中溶液的质量为160g B、升温到40℃时,烧杯中的溶液为饱和溶液 C、从60℃升温到80℃时,烧杯内溶液中溶质的质量分数减小 D、100℃时,烧杯内溶液中溶质的质量分数为37.5%9. 下列依据实验目的设计的实验方案正确的是( )
A、20℃时,充分搅拌后烧杯中溶液的质量为160g B、升温到40℃时,烧杯中的溶液为饱和溶液 C、从60℃升温到80℃时,烧杯内溶液中溶质的质量分数减小 D、100℃时,烧杯内溶液中溶质的质量分数为37.5%9. 下列依据实验目的设计的实验方案正确的是( )选项
实验目的
实验方案
A
鉴别水和过氧化氢溶液
取两种液体于试管中,分别加入少量二氧化锰
B
证明某气体是否为氢气
用试管收集该气体做爆鸣实验
C
比较吸入空气和呼出气体的二氧化碳含量
将带火星的木条分别伸入等体积的空气和呼出气体中
D
实验室制取二氧化碳气体
用块状大理石和稀硫酸反应
A、A B、B C、C D、D10. 利用数字化实验可以形象地比较不同形状的碳酸钙与稀盐酸反应的速率。倾斜锥形瓶使试管内的稀盐酸流入瓶中与固体发生反应,瓶内气压的变化如曲线所示。
有关说法正确的是( )
A、曲线①表示块状碳酸钙与稀盐酸反应 B、b点表示碳酸钙与盐酸反应已停止 C、等质量碳酸钙粉末产生的CO2的质量最多 D、对比分析点c、d可知,相同的气压时,粉状碳酸钙与稀盐酸反应速率更快二、填空题
-
11. 根据下列信息回答问题。
 (1)、如图为铝原子结构示意图及铝在元素周期表中的部分信息,其中,X=;铝的相对原子质量为。(2)、在空气中铝制品更耐腐蚀,用化学方程式表示其原因是;(3)、人类冶炼和使用金属铝的时间较晚是因为(填字母)。
(1)、如图为铝原子结构示意图及铝在元素周期表中的部分信息,其中,X=;铝的相对原子质量为。(2)、在空气中铝制品更耐腐蚀,用化学方程式表示其原因是;(3)、人类冶炼和使用金属铝的时间较晚是因为(填字母)。a、地壳中铝元素含量少 b、冶炼铝的技术要求高
(4)、已知一氧化碳具有还原性,可用于冶炼金属,请你写出一氧化碳和氧化铁在高温下的化学方程式(5)、炼钢中充氧的目的是降低生铁中的 , 获得性能更好的钢。12. “碳中和”要求二氧化碳的排放与吸收动态平衡。实现“碳中和”通常可采取如下措施:(1)、(一)碳循环CO2和H2在甲烷化装置中,用高功率的紫外LED灯照射(光催化)时,在室温下几乎能完全反应生成甲烷和水,具体应用如图1所示。

写出甲烷化装置中发生反应的化学方程式:。
(2)、写出在此过程中可以循环利用的物质的化学式(写一种)。(3)、(二)碳转化科学家研究发现,一定条件下,可将二氧化碳在催化剂表面转化成某种有机清洁燃料,其反应原理如图2所示。

反应涉及的物质中属于氧化物的有种。
(4)、参加反应的二氧化碳和氢气的分子个数比为。(5)、(三)碳封存重庆合川实验基地从大气中分离出二氧化碳,将其压缩液化泵入地下从而实现对二氧化碳的封存。
从微观角度分析,二氧化碳气体被压缩为液体时,发生变化。
13. “化”说中国古代炼“金”术。(1)、《吕氏春秋》:金(即铜)柔锡柔,合两柔则为刚。“合两柔则为刚”体现了合金的特性。(2)、古人按“一两黄金+七两X”的比例混合成金泥,涂抹在器物表面,之后上火烘烤,金属X遇热蒸发,金就成功附着。试推断出常温下呈液态的金属X为。(3)、北魏《黄白第十六》记载:“曾青涂铁,铁赤如铜”。曾青即硫酸铜溶液,“涂铁”后的反应原理为(用化学方程式表示)(4)、"沉睡三千年,一醒惊天下" 三星堆出土大量有研究价值的文物,其中出土的黄金面具有很强的抗腐性的原因是14. 水是人类宝贵的自然资源。(1)、1745 年左右纳瓦雷特的《中国帝国游记》记录黄河沿岸百姓掌握用明矾使黄河水变澄清的技术。其中明矾的作用是(2)、在水电解器中加入稀 Na2SO4溶液,至充满管A和管B(Na2SO4不参与反应,只起增强导电作用)。通直流电一段时间后现象如图1所示。
①电极N与电源(选填“正极”或“负极”)相连
②电解水的实验说明水是由组成的
③自来水厂用二氧化氯(ClO2)消毒杀苗,二氧化氯中氯元素显价
④长期饮用硬水对健康不利,生活中常通过方法降低水的硬度。
⑤因为了防止水的污染,下面可以采用的方法(填字母)
a.抑制水中所有动、植物的生长 b.不任意排放工业废水;
c.禁止使用农药和化肥 d.生活污水经过净化处理后再排放
(3)、海水晒盐后得到的晶体是粗盐,剩余的液体称为苦卤,苦卤中除氯化钠外还含有 MgCl2、KCl和MgSO4等物质,图2是三种物质的溶解度曲线。①80℃时,把 40gKCl放入50g水中,所得溶液的质量为。
②保持温度80℃,将溶质质量分数为10%的MgSO4溶液变成饱和溶液,可采取的方法是
三、科普阅读题
-
15. 阅读下面短文,回答问题
“冰丝带”是全球首个采用二氧化碳跨临界直冷制冰的冬奥速滑场馆。该技术碳排放趋近于零,且对大气臭氧层没有影响,是目前世界上最环保、最高效的制冰技术之一,研究发现,制冰机的二氧化碳蒸发湿度和转桶材料对制冰量都有影响。图!是当其他条件相同时,制冰量随二氧化碳蒸发温度和转桶材料的变化情况。
冰面下是混凝土冰板层,其主要材料是水泥。水泥是以石灰石、黏土(主要成分为 SiO2)等为原料,在一定条件下反应制得硅酸盐(如硅酸钙 CaSiO3)。科学家通过调整混凝土的材料配方增强其抗冻性。图2是掺有陶粒的混凝土和普通混凝土的抗冻性对比实验结果(强度损失率越高,抗冻性越差)。

 (1)、运动员在经过剧烈运动,并且大量出汗之后,通常会饮用一些含“钾”、“钠”等成分的淡盐水,这里的“钾”、“钠”指的是(选“分子”、“原子”或“元素”)。(2)、采用二氧化碳跨临界直冷制冰技术的优点有(写出一条即可)。(3)、由图1知,相同条件下,转桶材料为(选填“不锈钢”或“铝”)"时制冰量较大。(4)、由图2可推断“陶粒混凝土的抗冻性优于普通混凝土”依据是(5)、已知:2NaOH+SiO2X+H2O,则X的化学式是(6)、为减少CO2的排放,可将CO2进行转化,图4中反应的化学方程式为。
(1)、运动员在经过剧烈运动,并且大量出汗之后,通常会饮用一些含“钾”、“钠”等成分的淡盐水,这里的“钾”、“钠”指的是(选“分子”、“原子”或“元素”)。(2)、采用二氧化碳跨临界直冷制冰技术的优点有(写出一条即可)。(3)、由图1知,相同条件下,转桶材料为(选填“不锈钢”或“铝”)"时制冰量较大。(4)、由图2可推断“陶粒混凝土的抗冻性优于普通混凝土”依据是(5)、已知:2NaOH+SiO2X+H2O,则X的化学式是(6)、为减少CO2的排放,可将CO2进行转化,图4中反应的化学方程式为。
四、综合题
-
16. 实验室制取气体的部分装置如图所示,请结合图示回答问题。
 (1)、用10%的稀盐酸制取二氧化碳
(1)、用10%的稀盐酸制取二氧化碳【溶液配制】
①用30%的盐酸50g可配得10%的稀盐酸g。
【气体制备】
②实验室用装置A作为制取二氧化碳的发生装置,大理石应装在内,该装置的优点是。
(2)、加热高锰酸钾制取氧气【气体制备】
①为防止试管内的粉末堵塞导管,装置B的试管口应。②用装置E收集氧气,当观察到时,开始收集气体。
③用装置F装满水可收集氧气(保持瓶口朝上),将氧气从导管(填“a”或“b”)端通入,待瓶中的水排尽即可。
【分离生成物】
④若要分离完全反应后的固体产物,回收二氧化锰(难溶于水),需进行的实验操作是:溶解、、洗涤、干燥。
17. 某学习小组对铁锈蚀进行探究。【提出问题】铁锈蚀与哪些因素有关?
【查阅资料】①氯化钙固体可作干燥剂。
②一定条件下,碳可加快铁的锈蚀,但碳本身不参加反应。
【设计与实验】
(1)、实验一:定性探究铁锈蚀的因素取四枚相同的洁净无锈铁钉分别放入试管,进行图 1 实验,现象如表 1。

表 1
试管
一周后现象
A
铁钉表面有一层铁锈
B
铁钉表面无明显变化
C
铁钉表面无明显变化
D
铁钉表面有较厚铁锈
对比 A,B,C 试管中实验现象,说明铁锈蚀主要是与空气中的发生反应;
(2)、对比 A,D 试管中实验现象,说明铁锈蚀还与有关;(3)、铁锈的主要成分是(填化学式),铁锈蚀后应及时除锈的原因是。(4)、实验二:定量探究铁锈蚀的因素小组设计了图 2 装置,检查气密性,将 5g 铁粉和 2g 碳粉加入三颈烧瓶,t1时刻加入2mL 饱和 NaCl 溶液后,再将一只装有 5mL 稀盐酸的注射器插到烧瓶上,采集数据。

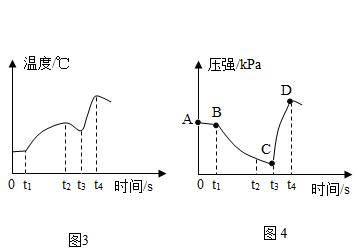
据图 3,铁锈蚀的过程中(填“吸热”或“放热”);
(5)、据图 4,对比 AB 段和 BC 段说明 , 分析 t3时刻后压强突然变大的原因是。(6)、【反思与评价】与实验一对比,实验二铁锈蚀明显更快的原因是。
五、计算题
-
18. 海鲜速运包装箱里常用过氧化钙(化学式为CaO2)与水反应提供氧气。其化学反应方程式为2CaO2+2H2O=2Ca(OH)2+O2 , 已知氧气的密度为1.4g/L,求用72克过氧化钙和足量的水反应可以制取到氧气的体积是多少(计算结果精确到0.1%)
-