河北省唐山市2023届高三二模考试化学试题
试卷更新日期:2023-05-25 类型:高考模拟
一、单选题
-
1. 化学与人类健康生活及环境保护息息相关。下列叙述正确的是( )A、食品加工时不可添加任何防腐剂 B、温室气体是形成酸雨的主要物质 C、大量使用含磷洗涤剂会造成水体污染 D、小苏打常用作烘焙面包,它的主要成分是2. 高分子化合物在人类生产生活中有着重要用途。下列有关说法正确的是 ( )A、酚醛树脂的单体为苯酚和甲醛,通过缩聚反应合成 B、淀粉和纤维素均表示为 , 二者互为同分异构体 C、塑料、橡胶、合成纤维均为合成高分子材料 D、聚乙烯为可降解材料,而聚氯乙烯为不可降解材料3. 下列实验操作不能达到实验目的的是 ( )
A
B
C
D
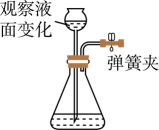
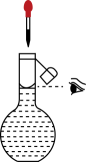

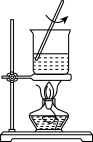
装置气密性检查
配制一定物质的量浓度的溶液
萃取时振荡混合液
溶液蒸干制备无水固体
A、A B、B C、C D、D4. 是阿伏加德罗常数的值。下列说法错误的是 ( )A、标准状况下,22.4 L氧气所含的质子数为 B、1 mol 晶体中含有的共价键数目为 C、向100 mL 溶液中加入足量Cu粉充分反应,转移电子数目为 D、1 L 溴化铵溶液中与离子数之和大于5. 化学工业是国民产业的基础。下列说法错误的是 ( )A、工业合成氨的反应原理为 B、工业制盐酸的反应原理为 C、侯氏制碱法中向饱和食盐水依次通入、 , 可得 D、高炉炼铁中用CO做还原剂6. 甲、乙、丙、丁为中学化学常见物质,其相互转化关系如图所示,下列组合不符合题意的是 ( )
甲
乙
丙
A
B
C
S
D
Fe
A、A B、B C、C D、D7. 短周期主族元素W、X、Y、Z的原子序数依次增大,W的核外电子数与X、Z的最外层电子数之和相等,Y元素的族序数与Z的最外层电子数之和等于X的原子序数,由X、W、Y三种元素形成的化合物M的结构如图所示。下列叙述正确的是 ( )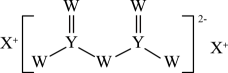 A、元素非金属性强弱的顺序为W>Y>Z B、W与X形成的二元化合物中阴阳离子数目之比为1:2 C、Y与W形成的二元化合物可用作半导体材料 D、电解饱和XZ水溶液可以制得X单质和Z单质8. 利用电化学原理消除污染,还可获得电能,下面是一种处理垃圾渗透液的装置工作原理图。下列说法错误的是 ( )
A、元素非金属性强弱的顺序为W>Y>Z B、W与X形成的二元化合物中阴阳离子数目之比为1:2 C、Y与W形成的二元化合物可用作半导体材料 D、电解饱和XZ水溶液可以制得X单质和Z单质8. 利用电化学原理消除污染,还可获得电能,下面是一种处理垃圾渗透液的装置工作原理图。下列说法错误的是 ( )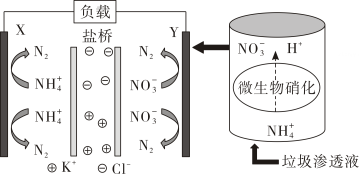 A、X极的电极反应式为 B、Y是正极,发生还原反应 C、当电路中通过5 mol电子,正极区有14 g气体放出 D、盐桥内移向X电极9. 下列实验能达到目的的是 ( )
A、X极的电极反应式为 B、Y是正极,发生还原反应 C、当电路中通过5 mol电子,正极区有14 g气体放出 D、盐桥内移向X电极9. 下列实验能达到目的的是 ( )选项
实验目的
实验方法或操作
A
制备NO气体
将铜丝插入浓硝酸中
B
探究浓度对化学反应速率的影响
取等体积不同浓度的NaClO溶液,分别加入等体积等浓度的溶液,对比现象
C
检验某盐溶液中是否含有
向溶液中加入NaOH溶液并加热,观察产生的气体能否使湿润的红色石蕊试纸变蓝
D
检验淀粉是否发生水解
向淀粉水解液中加入碘水
A、A B、B C、C D、D10. 化合物M(3,4-二咖啡酰奎宁酸)是中药材金银花中的一种化学物质,具有清热解毒的功效。下列说法错误的是 ( ) A、化合物M的分子式是 B、化合物M分子中手性碳原子数为4 C、1 mol M与足量NaOH溶液反应,最多消耗7 mol NaOH D、化合物M能发生加成反应、取代反应、水解反应、氧化反应11. 连二亚硫酸钠()俗称保险粉,是一种强还原剂,广泛用于纺织工业。某种的生产工艺流程如图所示,若在实验室模拟该工艺流程,下列说法正确的是 ( )
A、化合物M的分子式是 B、化合物M分子中手性碳原子数为4 C、1 mol M与足量NaOH溶液反应,最多消耗7 mol NaOH D、化合物M能发生加成反应、取代反应、水解反应、氧化反应11. 连二亚硫酸钠()俗称保险粉,是一种强还原剂,广泛用于纺织工业。某种的生产工艺流程如图所示,若在实验室模拟该工艺流程,下列说法正确的是 ( )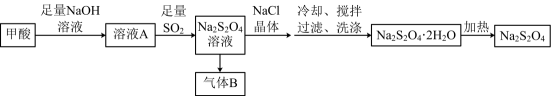 A、可用银氨溶液鉴别甲酸中是否含有甲醛 B、NaCl溶解度大于的溶解度 C、过滤操作中需要用的玻璃仪器只有漏斗、烧杯 D、由溶液A制备溶液过程中,氧化剂与还原剂物质的量之比为1:212. 是离子晶体,具有反萤石结构,晶胞如图所示,其晶格能可通过图中的循环计算得到。
A、可用银氨溶液鉴别甲酸中是否含有甲醛 B、NaCl溶解度大于的溶解度 C、过滤操作中需要用的玻璃仪器只有漏斗、烧杯 D、由溶液A制备溶液过程中,氧化剂与还原剂物质的量之比为1:212. 是离子晶体,具有反萤石结构,晶胞如图所示,其晶格能可通过图中的循环计算得到。

下列说法错误的是 ( )
A、Li的第一电离能为 B、Li的配位数为8 C、晶格能为 D、晶胞参数为a nm,则的密度为13. 一定条件下,在容积为2 L的恒容密闭容器中通入2 mol 发生反应 , 一定温度下,测得的转化率随时间的变化曲线如图所示,在60 min时反应达到平衡状态。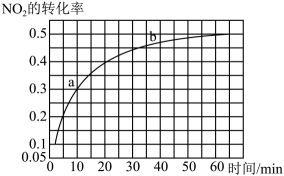
下列说法错误的是 ( )
A、a点处的逆反应速率小于b点处的正反应速率 B、0~10 min内,的平均反应速率 C、其他条件不变,若在恒压条件下发生反应,平衡时的转化率大于50% D、60 min后,保持温度不变,向该容器中再通入0.5 mol 和1 mol , 则反应逆向进行14. 已知HA、HB均为一元弱酸,且 , 向20 mL 的NaB溶液中逐滴滴加等浓度的HA溶液,溶液中与的变化关系如图所示: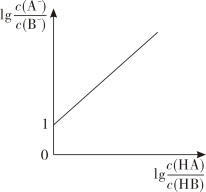
下列说法错误的是 ( )
A、 B、pH=7时, C、滴入HA溶液10 mL时, D、滴入HA溶液20 mL时,二、非选择题
-
15. 阿司匹林是人类历史上第一种重要的人工合成药物,它与青霉素、安定并称为“医药史上三大经典药物”。其合成原理如下:
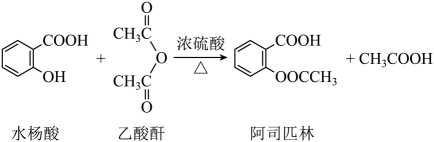
已知:
①副反应:

②水杨酸聚合物难溶于水,不溶于溶液。
③主要试剂和产品的物理常数如下:
名称
相对分子质量
密度/()
水溶性
水杨酸
138
1.44
微溶
醋酸酐
102
1.10
反应生成醋酸
乙酰水杨酸
180
1.35
微溶
实验室中合成少量阿司匹林的操作步骤如下:
①物质制备:向a中依次加入6.9 g水杨酸、10 mL乙酸酐、0.5 mL浓硫酸,在85℃~90℃条件下,加热5~10 min。
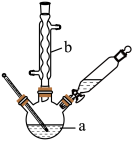
②产品结晶:冷却,加入一定量的冰水,抽滤,并用冰水洗涤沉淀2~3次,低温干燥,得阿司匹林粗产品。
③产品提纯:向阿司匹林粗品中缓慢加入饱和碳酸氢钠溶液,不断搅拌至无气泡产生。抽滤,洗涤沉淀,将洗涤液与滤液合并。合并液用浓盐酸酸化后冷却、可析出晶体,抽滤,冰水洗涤,低温干燥。得乙酰水杨酸晶体7.2 g。
(1)、水杨酸分子中最多有个原子共面,1 mol水杨酸分子中含有σ键NA。(2)、装置中仪器b的名称是 , 制备过程的加热方式是。(3)、步骤②和③中“抽滤”操作相对于普通过滤的优点是。(4)、步骤③中饱和碳酸氢钠溶液的作用是 , 抽滤之后将洗涤液与滤液合并的目的是。(5)、合并液与浓盐酸反应的化学方程式为。(6)、阿司匹林的产率是。16. 海水中提取镁的工艺流程: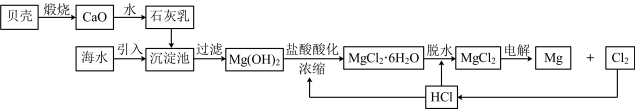 (1)、该工艺流程中属于分解反应的有个,请写出其中属于氧化还原反应的化学方程式。(2)、脱水得到的过程中,通入HCl的作用是。(3)、25℃时,在沉镁的过程中,将溶液滴加到悬浊液中,当混合溶液中pH=12时,同时存在、两种沉淀,则此时溶液中。判断此时(填“是”或“否”)完全沉淀。( , , 当某离子浓度降到以下时,认为该离子已经完全沉淀。)(4)、新工艺向含氧化镁熔浆中添加三氯化铈()和氯气反应,生成和无水氯化镁。请写出该反应的化学方程式。(5)、某实验小组对进行热重曲线分析:
(1)、该工艺流程中属于分解反应的有个,请写出其中属于氧化还原反应的化学方程式。(2)、脱水得到的过程中,通入HCl的作用是。(3)、25℃时,在沉镁的过程中,将溶液滴加到悬浊液中,当混合溶液中pH=12时,同时存在、两种沉淀,则此时溶液中。判断此时(填“是”或“否”)完全沉淀。( , , 当某离子浓度降到以下时,认为该离子已经完全沉淀。)(4)、新工艺向含氧化镁熔浆中添加三氯化铈()和氯气反应,生成和无水氯化镁。请写出该反应的化学方程式。(5)、某实验小组对进行热重曲线分析:
①分析181℃时固体产物的化学式为。
②写出在300℃时生成固体产物(一种含镁的碱式盐)的化学方程式。
17. 将和两种气体转化为合成气(和CO),可以实现能量综合利用,对环境保护具有十分重要的意义。甲烷及二氧化碳重整涉及以下反应:I. 平衡常数
Ⅱ. 平衡常数
Ⅲ. 平衡常数
(1)、为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1 mol该物质的焓变。对于稳定相态单质,其为零。根据下表数据,计算反应Ⅱ的反应热 , 该反应正反应活化能逆反应活化能(填“大于”、“小于”或“等于”)。物质
CO
()
(2)、平衡常数(用、表示)。(3)、一定温度下,维持压强 , 向一密闭容器中通入等物质的量的和发生反应。已知反应Ⅱ的速率方程可表示为 , , 其中、分别为正、逆反应的速率常数,则以物质的分压表示的反应Ⅱ的平衡常数(用、表示),另lgk与的关系如图所示,①、②、③、④四条直线中,表示的是(填序号),温度时,图中A、B、C、D点的纵坐标分别为、、、 , 达到平衡时,测得的转化率为60%,且体系中 , 则 , 以物质的分压表示的反应I的平衡常数。(用含的代数式表示,已知:lg5=0.7) 18. 两分子酯在碱的作用下失去一分子醇生成β-羰基酯的反应称为酯缩合反应,也称为Claisen缩合反应。其反应机理如下:
18. 两分子酯在碱的作用下失去一分子醇生成β-羰基酯的反应称为酯缩合反应,也称为Claisen缩合反应。其反应机理如下:
Claisen缩合在有机合成中应用广泛,有机物M(
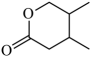 )的合成路线如图所示:
)的合成路线如图所示: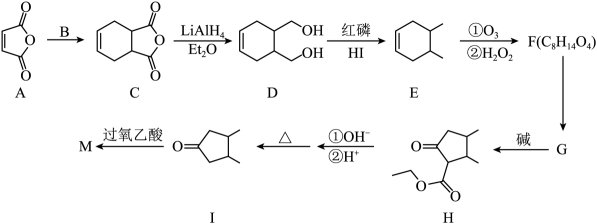
已知:
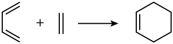
请回答下列问题:
(1)、B的名称为 , D中官能团的名称为。(2)、A→C的反应类型为 , F的结构简式为。(3)、G→H的反应方程式为。(4)、符合下列条件的C的同分异构体有种,其中核磁共振氢谱峰面积比为2:2:2:1:1的结构简式为。①遇溶液显紫色;②能发生水解反应;③能发生银镜反应。
(5)、结合上述合成路线,设计以乙醇和丁二酸(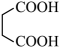 )为原料(其他无机试剂任选),合成
)为原料(其他无机试剂任选),合成 的路线。
的路线。