广东省江门市2023年中考一模化学试题
试卷更新日期:2023-05-23 类型:中考模拟
一、单选题
-
1. 下列各物质的化学式对应的俗名不正确的是( )A、NaOH 烧碱 B、Na2CO3 纯碱、苏打 C、NaHCO3 小苏打 D、CaCO3 熟石灰2. 下列物质与其对应的用途中,叙述错误的是( )A、浓硫酸——干燥CO2气体 B、小苏打——用作焙制糕点的发酵粉 C、纯碱——用于玻璃、洗涤剂的生产 D、氢氧化钠——用于改良酸性土壤3. 生活中一些常见物质的 pH 如下:厕所清洁剂 pH=1、食盐水 pH=7、肥皂水 pH=10、炉具清洁剂 pH=12,其中碱性最强的是( )A、厕所清洁剂 B、食盐水 C、肥皂水 D、炉具清洁剂4. 下列溶液在空气中敞口放置后,溶液质量因发生化学反应而减小的是( )A、石灰水 B、浓硫酸 C、浓盐酸 D、烧碱溶液5. 稀释浓硫酸并进行硫酸性质实验的下列操作,正确的是( )A、
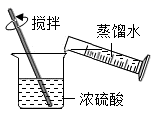 稀释浓硫酸
B、
稀释浓硫酸
B、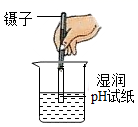 测稀硫酸的pH
C、
测稀硫酸的pH
C、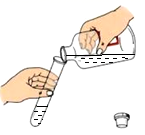 倾倒稀硫酸
D、
倾倒稀硫酸
D、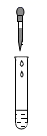 滴加稀硫酸
6. 氢溴酸是一种可溶性酸,与盐酸化学性质相似,其化学式为HBr,医药工业用其合成镇静剂和麻醉剂等医药用品,下列叙述正确的是( )A、HBr溶液能使无色酚酞变红 B、HBr溶液不能清除铁锈 C、HBr溶液和铁反应生成FeBr3 D、HBr溶液与石灰水能反应7. 下列说法正确的是( )A、霉变的花生煮熟食用 B、用甲醛浸泡水产品保鲜 C、食用新鲜的蔬菜水果 D、缺铁会引起骨质疏松8. 合成材料的应用与发展,大大方便了人类的生活。下列物品是用有机合成材料制作的是( )A、塑料桶 B、纯羊毛衫 C、铅笔芯 D、青铜铸像9. 现有一瓶某温度下接近饱和的硝酸钾溶液 ,欲将其转化为饱和溶液,下列措施不正确的是 ( )A、降低温度 B、蒸发一定量水,在恢复到原温度 C、温度不变时增加溶质 D、升高温度10. 将下列各组物质分别混合后同时加入水中,能得到无色透明溶液的组别是( )A、FeCl3、KNO3、NaOH B、AgNO3、NaNO3、CaCl2 C、CuSO4、Na2SO4、NaOH D、Na2CO3、Na2SO4、KCl11. 中和反应在生产、生活中有着广泛的应用。下列做法不是利用中和反应原理的是( )A、用氧化铜与稀硫酸反应制硫酸铜 B、用含氢氧化镁的药物治疗胃酸过多症 C、用氨水处理污水中的硫酸 D、将肥皂水涂抹在蚊虫叮咬处以减轻痛痒12. 下列试剂中,能将稀盐酸、氯化钠溶液、澄清石灰水一步鉴别出来的是( )A、稀硫酸 B、碳酸钠溶液 C、二氧化碳 D、无色酚酞溶液13. 下列除杂方法正确的是( )
滴加稀硫酸
6. 氢溴酸是一种可溶性酸,与盐酸化学性质相似,其化学式为HBr,医药工业用其合成镇静剂和麻醉剂等医药用品,下列叙述正确的是( )A、HBr溶液能使无色酚酞变红 B、HBr溶液不能清除铁锈 C、HBr溶液和铁反应生成FeBr3 D、HBr溶液与石灰水能反应7. 下列说法正确的是( )A、霉变的花生煮熟食用 B、用甲醛浸泡水产品保鲜 C、食用新鲜的蔬菜水果 D、缺铁会引起骨质疏松8. 合成材料的应用与发展,大大方便了人类的生活。下列物品是用有机合成材料制作的是( )A、塑料桶 B、纯羊毛衫 C、铅笔芯 D、青铜铸像9. 现有一瓶某温度下接近饱和的硝酸钾溶液 ,欲将其转化为饱和溶液,下列措施不正确的是 ( )A、降低温度 B、蒸发一定量水,在恢复到原温度 C、温度不变时增加溶质 D、升高温度10. 将下列各组物质分别混合后同时加入水中,能得到无色透明溶液的组别是( )A、FeCl3、KNO3、NaOH B、AgNO3、NaNO3、CaCl2 C、CuSO4、Na2SO4、NaOH D、Na2CO3、Na2SO4、KCl11. 中和反应在生产、生活中有着广泛的应用。下列做法不是利用中和反应原理的是( )A、用氧化铜与稀硫酸反应制硫酸铜 B、用含氢氧化镁的药物治疗胃酸过多症 C、用氨水处理污水中的硫酸 D、将肥皂水涂抹在蚊虫叮咬处以减轻痛痒12. 下列试剂中,能将稀盐酸、氯化钠溶液、澄清石灰水一步鉴别出来的是( )A、稀硫酸 B、碳酸钠溶液 C、二氧化碳 D、无色酚酞溶液13. 下列除杂方法正确的是( )选项
物质(括号内为杂质)
方法
A
K2CO3溶液(K2SO4)
加BaCl2溶液,过滤
B
N2(O2)
将气体通过灼热的铜网
C
NaOH溶液(Na2CO3)
加入稀硫酸
D
ZnSO4溶液(CuSO4)
加入过量的铁粉,过滤
A、A B、B C、C D、D14. 忘盖瓶塞的氢氧化钠溶液可能变质。下表中分析与设计错误的是( )选项
问题
分析与设计
A
为何变质
2NaOH + CO2 = Na2CO3 + H2O
B
是否变质
取样,加入足量稀盐酸,观察是否产生气泡
C
是否全部变质
取样,加入足量氯化钙溶液,观察产生沉淀多少
D
如何除去杂质
取样,加入适量氢氧化钙溶液,过滤
A、A B、B C、C D、D15. 下列各组物质不能实现如图所示的转化关系的是( )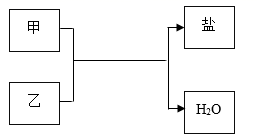
选项
甲
乙
A
Fe2O3
稀硫酸
B
SO3
NaOH溶液
C
稀盐酸
Ca(OH)2溶液
D
稀盐酸
AgNO3溶液
A、A B、B C、C D、D二、填空题
-
16. 新冠疫情期间突然闹出来的“粮荒”,为世界粮食安全敲响了警钟,近日,袁隆平院士团队研究的海水稻,再次在我国青海高盐碱地区试种(高盐碱地土壤内水分pH超过8.5)。(1)、如果试种成功,将来人们有望吃到西部海水稻大米,大米提供的主要营养素是。(2)、由于海水稻生长在碱性土壤,与普通大米相比钠的含量较高,钠元素是人类所需的元素(填“常量”或“微量”)。(3)、为变废为宝,不断改良这种盐碱地,常在土地中施加(填“硫磺粉”或“熟石灰”)。(4)、水稻等农作物生长期间常施加一些肥料,下列物质属于复合肥料的是(填序号)。
a.KNO3
b.CO(NH2)2
c.K2SO4
d.Ca3(PO4)2
三、综合
-
17. 下图是A、B两种物质的溶解度曲线,根据图示回答下列问题:
 (1)、t1oC时,A,B两种物质的溶解度是AB(填“>”、“<”或“=”,下同)。(2)、将t3oC的A,B两种物质的饱和溶液各200g,降温至t1oC,析出晶体的质量关系是AB。(3)、t2oC时,100g水中溶解50gA刚好饱和,那么50g水中溶解g,B也刚好达饱和,此时溶液的质量分数是(精确到0.1%)。(4)、解释生活中的现象:
(1)、t1oC时,A,B两种物质的溶解度是AB(填“>”、“<”或“=”,下同)。(2)、将t3oC的A,B两种物质的饱和溶液各200g,降温至t1oC,析出晶体的质量关系是AB。(3)、t2oC时,100g水中溶解50gA刚好饱和,那么50g水中溶解g,B也刚好达饱和,此时溶液的质量分数是(精确到0.1%)。(4)、解释生活中的现象:①如果用稀硫酸除去铁锈的化学方程式为。其基本类型为反应。
②工厂废气处理时,用石灰浆吸收SO2(性质与CO2相似)的化学反应方程是。
③实验室中含有盐酸的废水倒入下水道会造成铸铁管道腐蚀,其理由为:(用化学方程式解释)。
18. 实验室对含有MgCl2的粗盐进行提纯,步骤如图: (1)、步骤①中,称量5.0g粗盐需补充的主要仪器是。(2)、步骤②中,玻璃棒的作用是;步骤④中玻璃棒的作用是。(3)、步骤③中,滴加过量NaOH溶液除去MgCl2 , 反应的化学方程式是。(4)、步骤⑤中,为中和过量的NaOH,应滴加的“试剂a”是____(填字母)。A、稀盐酸 B、稀硫酸 C、稀硝酸(5)、步骤⑥的操作名称是 , 当时,停止加热;玻璃棒的作用是。(6)、甲同学所得的产率与其他同学比较明显偏低,下列哪些情况导致产率明显偏小____。A、过滤后,滤液还是浑浊的就蒸发 B、蒸发时有一些液滴溅出 C、提纯后的精盐尚未完全干燥就称其质量19. 咸宁市某校2018年实验操作模拟考试的一个考题是:用碳酸钠溶液鉴别稀盐酸、食盐水和澄清石灰水。(1)、(进行实验)
(1)、步骤①中,称量5.0g粗盐需补充的主要仪器是。(2)、步骤②中,玻璃棒的作用是;步骤④中玻璃棒的作用是。(3)、步骤③中,滴加过量NaOH溶液除去MgCl2 , 反应的化学方程式是。(4)、步骤⑤中,为中和过量的NaOH,应滴加的“试剂a”是____(填字母)。A、稀盐酸 B、稀硫酸 C、稀硝酸(5)、步骤⑥的操作名称是 , 当时,停止加热;玻璃棒的作用是。(6)、甲同学所得的产率与其他同学比较明显偏低,下列哪些情况导致产率明显偏小____。A、过滤后,滤液还是浑浊的就蒸发 B、蒸发时有一些液滴溅出 C、提纯后的精盐尚未完全干燥就称其质量19. 咸宁市某校2018年实验操作模拟考试的一个考题是:用碳酸钠溶液鉴别稀盐酸、食盐水和澄清石灰水。(1)、(进行实验)实验步骤
实验现象
实验结论
分别用a、b、c三支试管取样,各加入一定量碳酸钠溶液
a中有气泡产生
a中物质是稀盐酸
b中无明显现象
b中物质是食盐水
c中
c中物质是澄清石灰水
写出a试管中发生反应的化学方程式。把c试管反应后的物质进行过滤,得到滤液。
(2)、(提出问题)滤液中溶质的成分是什么?猜想一:Na2CO3和NaOH;猜想二:NaOH;猜想三:。提示:Ca(OH)2微溶于水。
(3)、(实验过程)为证明猜想一是否正确,进行了如下实验:实验步骤
实验现象
实验结论
取一定量滤液于试管中,加入一种盐溶液(写溶质化学式)。
有白色沉淀
猜想一正确
写出上述有白色沉淀生成的化学方程式。
同学们还对a试管反应后废液的酸碱性感兴趣,决定用pH试纸测定其pH值
用pH试纸测定a试管反应后废液酸碱性的过程
测定结果
在白瓷板上放一小片pH试纸,用玻璃棒蘸取。
pH<7(废液显酸性)
(4)、(反思与交流)a试管中的废液显酸性,从环保、经济、操作简便等方面考虑,应向废液加入(写化学式)后再排放20. 仓库中有一包氮肥,有可能含有碳酸氢铵、氯化铵、硫酸铵、硝酸铵、尿素,其包装标签模糊不清,有同学进行了以下探究: (1)、操作③用玻璃棒搅拌的目的是。(2)、请完成下表(已知AgCl和BaSO4是难溶于水和酸的白色固体):
(1)、操作③用玻璃棒搅拌的目的是。(2)、请完成下表(已知AgCl和BaSO4是难溶于水和酸的白色固体):假设和现象
判断和化学方程式
a
若现象I为无氨味。
则样品中不含(填名称)。
b
由操作②现象判断。
该样品一定含有(离子符号)。
c
若现象Ⅲ为白色沉淀,现象Ⅳ为无沉淀。
则样品中含有(写名称),该反应的化学方程式为。
d
若现象Ⅲ为“无沉淀”,现象Ⅳ为白色沉淀。
则样品中含有(写化学式),该反应的化学方程式为。
(3)、若现象Ⅲ、Ⅳ都无现象,则该氮肥可能是(写化学式)。21. 某化学实验室用稀硫酸处理含有氢氧化钠的废水。现取废水样品80g倒入烧杯中,加入几滴无色酚酞溶液,然后逐滴加入9.8%的稀硫酸,反应过程中溶液的pH变化如图所示。 (1)、当恰好完全反应时,溶液的颜色变化是。(2)、求废水中氢氧化钠的质量分数(写出计算过程)。(3)、往上述80g废水中逐渐加入稀硫酸至过量请在答题卡中画出Na2SO4质量随加入稀硫酸质量变化的曲线。
(1)、当恰好完全反应时,溶液的颜色变化是。(2)、求废水中氢氧化钠的质量分数(写出计算过程)。(3)、往上述80g废水中逐渐加入稀硫酸至过量请在答题卡中画出Na2SO4质量随加入稀硫酸质量变化的曲线。
-