山东省青岛市市北区2022-2023学年九年级下学期开学考试化学试题
试卷更新日期:2023-05-11 类型:开学考试
一、单选题
-
1. 下列变化属于化学变化的是( )A、石蜡熔化 B、丹桂飘香 C、玻璃破碎 D、火上浇油
-
2. “航天点亮梦想”。搭载神舟飞船的火箭常用液氢作燃料,液氢的化学式是( )A、H2 B、CH4 C、CO D、NH3
-
3. 地壳中含量最多的金属元素是()
A、氧 B、硅 C、铝 D、铁 -
4. 节约用水是保护水资源的有效途径。适合张贴在学校水龙头旁的标识是( )A、
 B、
B、 C、
C、 D、
D、
-
5. 下列实验操作正确的是( )A、
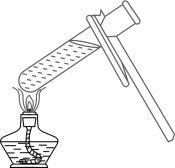 加热液体
B、
加热液体
B、 检查气密性
C、
检查气密性
C、 点燃酒精灯
D、
点燃酒精灯
D、 氧气验满
氧气验满
-
6. 自热食品的发热包中含有CaO,它属于( )A、酸 B、碱 C、盐 D、氧化物
-
7. 下列物质由离子构成的是( )A、氮气 B、硝酸钠 C、二氧化碳 D、金刚石
-
8. 室温时,下列液体的pH小于7的是( )A、白醋 B、蒸馏水 C、食盐水 D、肥皂水
-
9. 下列有关水的说法正确的是( )A、水是取之不尽、用之不竭的资源 B、自来水厂净水过程中,必须有蒸馏的步骤 C、硬水中加入肥皂水并振荡后,会出现大量浮渣 D、为节约水资源,提倡直接用工业废水浇灌农田
-
10. 防治空气污染,保护生态环境。下列做法不合理的是( )A、开发和使用清洁能源 B、车辆尾气净化后排放 C、工业废气排放到高空 D、管理和控制工地扬尘
-
11. 从微观角度可以认识化学变化的实质。下图所示化学反应的类型为( )
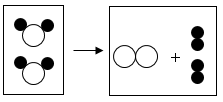
“
 ”和“
”和“ ”表示不同元素的原子A、化合反应 B、分解反应 C、氧化反应 D、复分解反应
”表示不同元素的原子A、化合反应 B、分解反应 C、氧化反应 D、复分解反应 -
12. 很多成语、俗语、诗词中蕴含着丰富的科学道理。下列用化学观点解释错误的是( )A、“众人拾柴火焰高”--指可燃物越多,燃烧放出的热量越多 B、“遥知不是雪,为有暗香来”--分子在不断运动 C、“冰,水为之,而寒于水”-物质的状态不同,化学性质不同 D、“人要实,火要虚”-增加可燃物与氧气的接触面积,可燃物燃烧得更旺
-
13. 高铁酸钾(K2FeO4)是一种高效多功能的新型绿色消毒剂,主要用于饮用水处理。请根据其化学式推算出其中铁元素的化合价为( )A、+2 B、+3 C、+4 D、+6
-
14. 北京冬奥会火种灯使用化合物X作燃料,其燃烧反应方程式为。推断X的化学式是( )A、C3H8 B、C3H6 C、C2H6O2 D、C3H8O3
-
15. 把一根洁净的铁钉放入稀硫酸中,下列叙述正确的是( )
①在铁钉表面产生气泡;②溶液由无色逐渐变为浅绿色;③铁钉的质量增加;④溶液的质量增加。
A、②③ B、①②③ C、①②④ D、①③ -
16. 逻辑推理是一种重要的化学思维方法。下列推理正确的是( )A、同种元素的原子具有相同的质子数,所以具有相同质子数的原子属于同种元素 B、H2O和H2O2的组成元素相同,所以它们的化学性质相同 C、离子是带电荷的粒子,所以带电荷的粒子一定是离子 D、氧化物中都含有氧元素,所以含有氧元素的化合物都是氧化物
-
17. 下列物质的性质与用途具有对应关系的是( )A、石墨能导电,可用于制作铅笔芯 B、二氧化碳是无色气体,可用作保护气 C、氧气不易溶于水,可用于抢救病人 D、浓硫酸具有吸水性,可用于干燥氧气
-
18. 下列物质露置于空气中一段时间,质量会增加的是( )A、浓盐酸 B、大理石 C、浓硫酸 D、氢氧化钠固体
-
19. 下列有关测定氢氧化钠溶液pH的实验操作或描述,你认为正确的是()A、用镊子夹取pH试纸直接伸入氢氧化钠溶液中测量 B、先用蒸馏水将pH试纸润湿,再用滴管吸取氢氧化钠溶液滴到pH试纸上测量 C、用洁净干燥的玻璃棒蘸取氢氧化钠溶液滴到pH试纸上,再与标准比色卡对照 D、用pH试纸测得该氢氧化钠溶液的
-
20. 归纳和推理是重要的科学思维方法,下列说法合理的是( )A、催化剂的质量在化学反应前后不变,因此在反应前后质量不变的物质一定是催化剂 B、洗涤剂通过乳化作用去除油污,因此去除油污的原理都是利用乳化作用 C、溶液具有均一性和稳定性,因此均一、稳定的液体一定是溶液 D、酸与碱作用生成盐和水的反应叫中和反应,但生成盐和水的反应不一定是中和反应
-
21. 下表中所用药品或方法能达到实验目的的是( )
选项
实验目的
所用药品或方法
A
除去CaCl2溶液中混有的HCl
加入过量的Ca(OH)2溶液
B
除去NaOH溶液中混有的Na2CO3
加入适量的稀盐酸
C
鉴别盐酸和NaCl溶液
取样,分别滴加石蕊溶液
D
CaO和CaCO3鉴别
取样,分别在样品表面滴加适量的水
A、A B、B C、C D、D -
22. 常温下取稀盐酸与氢氧化钠反应后的溶液进行实验,下列能说明稀盐酸和氢氧化钠恰好完全反应的是( )A、加入碳酸钙粉末,有气泡产生 B、加入AgNO3溶液,有白色沉淀产生 C、加入酚酞溶液,溶液显红色 D、测定溶液的pH,pH=7
二、填空题
-
23. 从下列选项中选择适当的物质填空(填字母序号)。
A.氯化钠 B.明矾 C.酒精 D.氮气 E.熟石灰
(1)、可用于净水的是。(2)、可用作燃料的是。(3)、可用作食品保鲜保护气的是。(4)、可用于配制生理盐水的是。(5)、可用于改良酸性土壤的是。 -
24. 近年来我国航天事业迅速发展,彰显了我国科技力量的日益强大。(1)、某种火箭推进剂发生化学反应的微观示意图如下,该反应的产物有N2和(用化学式填空)。
 (2)、“天宫课堂”地面分课堂上,某同学提问“空间站的氧气是怎么来的?”,太空教师叶光富解答是通过电解水得到,该反应的化学方程式是。太空教师王亚平将泡腾片塞入蓝色水球中,产生很多小气泡,还闻到阵阵香气。“闻到香气”说明分子在。航天员用过的水净化后可循环使用,其中利用活性炭的性可除去水中的异味和色素等。
(2)、“天宫课堂”地面分课堂上,某同学提问“空间站的氧气是怎么来的?”,太空教师叶光富解答是通过电解水得到,该反应的化学方程式是。太空教师王亚平将泡腾片塞入蓝色水球中,产生很多小气泡,还闻到阵阵香气。“闻到香气”说明分子在。航天员用过的水净化后可循环使用,其中利用活性炭的性可除去水中的异味和色素等。
三、科普阅读题
-
25. 气候变化是人类面临的巨大挑战,世界各国以全球协约的方式减排温室气体。中国政府提出在2060年前实现“碳中和”。“碳中和”是指通过植树造林、节能减排等形式,抵消人类生产生活产生的二氧化碳等温室气体排放,实现正负抵消,达到相对“零排放”。影响二氧化碳排放的主要因素是人类消耗的化石能源急剧增加,排入大气中的二氧化碳增多。我国近年部分行业二氧化碳年排放量如图所示:

“碳捕获和碳封存”也可以减少二氧化碳排放,“碳封存”可从大气中分离出二氧化碳将其压缩液化泵入地下长期储存。
依据文章内容,回答下列问题:
(1)、“碳中和”战略的实施有利于控制。(2)、“零排放”是指人类通过先进的科学技术手段,不再向自然界中排放CO2。此说法(填“正确”或“不正确”)。(3)、工业行业大类中,行业CO2年排放量最多。(4)、石油化工行业中天然气(主要成分是CH4)完全燃烧的化学方程式为。(5)、“碳封存”可将CO2压缩至地下储存,其原因是(从微观角度解释)。 -
26. 元素周期表是学习化学的重要工具。下表为元素周期表中部分元素的相关信息,请利用下表回答相关问题:
 (1)、氯元素的原子序数是 , 它属于(填“金属”或“非金属”)元素。表中Na元素位于元素周期表中的第周期。(2)、与元素的化学性质关系最密切的是原子的。(3)、移动通信即将进入5G时代,铊将得到广泛应用。下图是元素周期表中铊的信息,下列有关铊元素说法错误的是____;
(1)、氯元素的原子序数是 , 它属于(填“金属”或“非金属”)元素。表中Na元素位于元素周期表中的第周期。(2)、与元素的化学性质关系最密切的是原子的。(3)、移动通信即将进入5G时代,铊将得到广泛应用。下图是元素周期表中铊的信息,下列有关铊元素说法错误的是____; A、铊元素属于金属元素 B、铊元素的原子核内有81个质子 C、铊元素的原子实际质量是204.4 D、铊元素的原子核外电子数为81
A、铊元素属于金属元素 B、铊元素的原子核内有81个质子 C、铊元素的原子实际质量是204.4 D、铊元素的原子核外电子数为81
四、综合题
-
27. 制取气体是初中化学实验的重要内容,根据要求回答下列问题:
 (1)、写出标有序号的仪器名称:①。(2)、实验室利用大理石和稀盐酸反应制取二氧化碳,可选择的发生装置是(填字母序号,下同)。(3)、若要得到干燥的氧气,所选择装置的连接顺序为:B→→。(4)、某气体只能用C装置收集,则该气体可能具有的性质为。
(1)、写出标有序号的仪器名称:①。(2)、实验室利用大理石和稀盐酸反应制取二氧化碳,可选择的发生装置是(填字母序号,下同)。(3)、若要得到干燥的氧气,所选择装置的连接顺序为:B→→。(4)、某气体只能用C装置收集,则该气体可能具有的性质为。a.能与水反应 b.能与空气中的某些成分发生反应 c.密度与空气接近
(5)、用图乙装置进行铁丝在氧气里燃烧的实验,可观察到的现象是 , 该反应的化学方程式为。 -
28. 为认识酸和碱的性质,某化学学习小组进行了如下实验。
 (1)、20℃时,配制80 g溶质质量分数为10%的NaOH溶液。
(1)、20℃时,配制80 g溶质质量分数为10%的NaOH溶液。①用图中仪器完成实验,还缺少的玻璃仪器是(填名称),玻璃棒在配制实验中的作用是。
②配制该溶液需要g水。用量筒量取水时,俯视读数会导致所配溶液的溶质质量分数10%。(填“大于”或“小于”)
(2)、向1~4号小试管中分别滴加少量稀盐酸。
①中溶液变为红色(填“试管1”或“试管2”)。
②试管3中可观察到 , 试管4中无明显现象。
(3)、借助传感器对稀NaOH溶液与稀盐酸的中和反应进行研究,实验装置如图1,三颈烧瓶中盛放溶液X,用恒压漏斗匀速滴加另一种溶液。

①甲同学用pH传感器测得三颈烧瓶内溶液pH的变化如题图2,判断溶液X是(填“NaOH溶液”或“稀盐酸”),实验进行到60 s时溶液中的溶质为(填化学式)。
②乙同学用温度传感器测得三颈烧瓶内温度变化如图3(实验过程中热量散失忽略不计),据此可得出反应过程中能量的结论(填“吸收”或“释放”)。
-
29. 归纳总结是学习化学的重要方法,小明同学用思维导图的形式总结了NaOH的四条化学性质如图(即NaOH与四类物质能够发生化学反应)。请回答:
 (1)、反应①中若把酚酞溶液滴加到氢氧化钠溶液中,观察到的现象是。(2)、写出一个符合反应②的化学方程式。(3)、反应③可以选用的盐是 (填字母序号),可观察到的现象是。
(1)、反应①中若把酚酞溶液滴加到氢氧化钠溶液中,观察到的现象是。(2)、写出一个符合反应②的化学方程式。(3)、反应③可以选用的盐是 (填字母序号),可观察到的现象是。A.NaNO3 B.CuSO4 C.NaCl D.KNO3
(4)、二氧化碳和一氧化碳都是非金属氧化物,二氧化碳能和氢氧化钠反应,一氧化碳却不能,造成此性质差异的微观原因是。
五、计算题
-
30. 化学兴趣小组的同学为了测定某石灰石样品中碳酸钙的含量,进行了如下实验:取12.5g石灰石样品于烧杯中,逐渐加入稀盐酸(杂质不与稀盐酸反应),产生二氧化碳的质量与所加稀盐酸的质量关系如图所示。请计算:
 (1)、生成二氧化碳的质量是。(2)、该石灰石样品中碳酸钙的质量分数为多少?
(1)、生成二氧化碳的质量是。(2)、该石灰石样品中碳酸钙的质量分数为多少?
