高中化学(人教2019)选择性必修二期末知识点复习8 金属晶体与离子晶体
试卷更新日期:2023-05-10 类型:复习试卷
一、单选题
-
1. 下列说法正确的是A、除稀有气体外,第二周期元素随着核电荷数递增,元素的最高正价从+1递增到+7 B、H2O的热稳定性高于H2S是因为水分子间存在氢键 C、共价化合物只含共价键,离子化合物只含离子键 D、共价键的键长等于成键原子之间的核间距2. 铜的某种氧化物的晶胞结构如图所示。下列说法错误的是( )
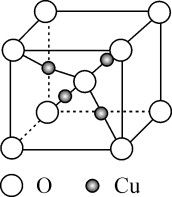 A、位于元素周期表区 B、该晶胞中的配位数为4 C、该物质的化学式为 D、O位于围成的四面体的体心3. 储氢合金LaNi5、LaCo5、CeCo5等结构和CaCu5相同。CaCu5合金由图甲、乙两个原子层交替密堆积而成,丙是CaCu5的晶体结构。
A、位于元素周期表区 B、该晶胞中的配位数为4 C、该物质的化学式为 D、O位于围成的四面体的体心3. 储氢合金LaNi5、LaCo5、CeCo5等结构和CaCu5相同。CaCu5合金由图甲、乙两个原子层交替密堆积而成,丙是CaCu5的晶体结构。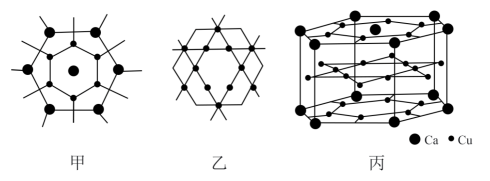
下列说法正确的是( )
A、CaCu5晶体类型为离子晶体 B、晶体中Ca原子与6个Cu原子配位 C、CaCu5晶体的一个晶胞中Cu原子数为15 D、LaNi5晶胞体积为9×10-23cm-3 , 储氢后形成LaNi5H4.5的合金,氢进入晶胞空隙,体积不变,氢在合金中的密度约为0.083g•cm-34. 碱金属氯化物是典型的离子化合物,NaCl和CsCl的晶胞结构如图所示。其中的碱金属离子能够与冠醚形成超分子。
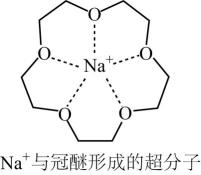
下列说法错误的是( )
A、NaCl晶胞中a为Na+ B、CsCl晶体中Cs+周围紧邻8个Cl- C、碱金属离子与冠醚通过离子键形成超分子 D、不同空穴尺寸的冠醚可以对不同碱金属离子进行识别5. 根据下表数据判断错误的是( )物质
NaCl
熔点
920
801
1291
190
2073
1723
A、表格中的物质涉及三种晶体类型 B、含铝的化合物不一定是离子晶体 C、和的熔点差异是由于键长不同 D、不同族元素的氧化物可形成相同类型的晶体6. 下列叙述正确的是( )A、共价键的方向性使金刚石晶体有脆性,延展性较差 B、三氟氨硼烷()分子中,N和B的杂化方式不同 C、能与HF形成氢键,所以会溶于氢氟酸 D、金属能导电是因为金属在电场作用下先释放自由电子再定向运动7. 某钙钛矿型氧化物的晶胞结构如图所示,其中A为镧系金属离子,B为过渡金属离子,C为氧离子。下列说法正确的是( ) A、镧系元素位于元素周期表中IB族 B、该化合物的化学式为 C、1个基态氧原子有2个未成对电子 D、1个A离子周围最近的A离子有12个8. 下列说法正确的是( )A、甲酸的酸性比乙酸弱 B、[Cu(NH3)4]2+的空间构型为四面体结构 C、NaCl晶胞与CsCl晶胞中阳离子的配位数相同 D、金刚石为三维骨架结构,由共价键形成的碳原子环中,最小的环上有6个碳原子9. 铁氮化合物(FexNy)在磁记录材料领域有着广泛的应用前景。某FexNy的晶胞如图−1所示,晶胞边长为z pm,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物,Fe(x−n) CunNy。FexNy转化为两种Cu替代型产物的能量变化如图−2所示。下列说法错误的是( )
A、镧系元素位于元素周期表中IB族 B、该化合物的化学式为 C、1个基态氧原子有2个未成对电子 D、1个A离子周围最近的A离子有12个8. 下列说法正确的是( )A、甲酸的酸性比乙酸弱 B、[Cu(NH3)4]2+的空间构型为四面体结构 C、NaCl晶胞与CsCl晶胞中阳离子的配位数相同 D、金刚石为三维骨架结构,由共价键形成的碳原子环中,最小的环上有6个碳原子9. 铁氮化合物(FexNy)在磁记录材料领域有着广泛的应用前景。某FexNy的晶胞如图−1所示,晶胞边长为z pm,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物,Fe(x−n) CunNy。FexNy转化为两种Cu替代型产物的能量变化如图−2所示。下列说法错误的是( )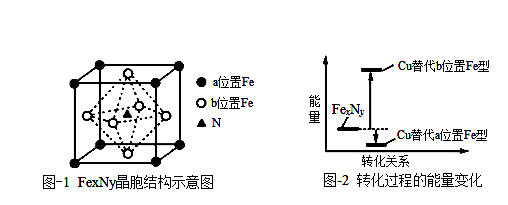 A、该铁氮化合物的化学式为Fe4N B、晶体中与每个N距离最近且等距离的N为6个 C、两个b位置Fe的最近距离为Z pm D、其中更稳定的Cu替代型产物的化学式为FeCu3N10. 下列关于晶体的描述正确的是( )A、分子晶体中一定含有共价键 B、共价晶体中,共价键的键能越大、键长越短,熔点越高 C、金属晶体的导电性和导热性都是通过自由电子的定向移动实现的 D、某晶体溶于水可电离出自由移动的离子,该晶体一定是离子晶体11. 下列物质属于离子晶体的是( )A、长方体形玻璃 B、NaNO3固体 C、水晶 D、钻石12. 下列说法中,正确的是( )A、原子晶体在熔融态时,共价键被破坏 B、金属晶体的熔点一定比分子晶体的高 C、干冰升华时,分子内共价键会发生断裂 D、分子晶体中,分子间作用力越大,对应的物质越稳定13. 检验灼热的碳投入浓硫酸中产生的气体的成分,实验步骤如下:
A、该铁氮化合物的化学式为Fe4N B、晶体中与每个N距离最近且等距离的N为6个 C、两个b位置Fe的最近距离为Z pm D、其中更稳定的Cu替代型产物的化学式为FeCu3N10. 下列关于晶体的描述正确的是( )A、分子晶体中一定含有共价键 B、共价晶体中,共价键的键能越大、键长越短,熔点越高 C、金属晶体的导电性和导热性都是通过自由电子的定向移动实现的 D、某晶体溶于水可电离出自由移动的离子,该晶体一定是离子晶体11. 下列物质属于离子晶体的是( )A、长方体形玻璃 B、NaNO3固体 C、水晶 D、钻石12. 下列说法中,正确的是( )A、原子晶体在熔融态时,共价键被破坏 B、金属晶体的熔点一定比分子晶体的高 C、干冰升华时,分子内共价键会发生断裂 D、分子晶体中,分子间作用力越大,对应的物质越稳定13. 检验灼热的碳投入浓硫酸中产生的气体的成分,实验步骤如下:步骤1:先将该气体通入品红溶液中,观察现象;
步骤2:将步骤1中的气体通入酸性高锰酸钾溶液后再通过品红溶液,观察现象;
步骤3:再将步骤2中的气体通入澄清石灰水中,观察现象。
下列说法错误的是( )
A、步骤1中品红溶液褪色,说明产生气体中含 B、步骤2的目的是除去并证明已除尽 C、步骤3持续时间过长现象会消失,原因是生成了配合物 D、一种碳-铁合金结构如图所示 , 该合金化学式是FeC
14. 辉铜矿(主要成分)可以用于制铜,化学反应方程式为 , 制得的粗铜(含等杂质)可通过电解法进行精炼,下列相关说法正确的是( )
, 该合金化学式是FeC
14. 辉铜矿(主要成分)可以用于制铜,化学反应方程式为 , 制得的粗铜(含等杂质)可通过电解法进行精炼,下列相关说法正确的是( ) A、转化为基态 , 得到的电子填充在轨道上 B、S元素的电负性大于O元素的电负性 C、电解精炼铜时,粗铜应与电源的负极相连 D、如图所示的晶胞中,黑球表示的是15. 下列说法中正确的是( )A、含离子键,在熔融状态下能导电 B、轨道上的电子一定比轨道能量高 C、价电子越多的金属元素的金属性越强 D、第四周期元素的基态原子中,未成对电子数最多的是16. 有关晶体的结构如图所示,下列说法中错误的是( )
A、转化为基态 , 得到的电子填充在轨道上 B、S元素的电负性大于O元素的电负性 C、电解精炼铜时,粗铜应与电源的负极相连 D、如图所示的晶胞中,黑球表示的是15. 下列说法中正确的是( )A、含离子键,在熔融状态下能导电 B、轨道上的电子一定比轨道能量高 C、价电子越多的金属元素的金属性越强 D、第四周期元素的基态原子中,未成对电子数最多的是16. 有关晶体的结构如图所示,下列说法中错误的是( ) A、在晶体中,距最近的有6个,距最近且等距的共12个 B、在晶体中,每个晶胞平均占有4个 , 的配位数是4 C、在金刚石晶体中,每个碳原子被12个六元环共同占有,每个六元环最多有4个碳原子共面 D、该气态团簇分子的分子式为或 , 其晶体不导电17. 下列说法不正确的是( )A、HBr分子中存在极性共价键 B、KOH晶体中既有离子键又有共价键 C、NaCl晶体溶于水时有离子键的断裂 D、NH3分子中每个原子最外电子层都具有8电子稳定结构18. 下列说法正确的是( )A、HCl气体和蔗糖溶于水时,都破坏了共价键 B、H2O、H2S、H2Se的相对分子质量依次增大,熔点依次增大 C、NaOH和K2SO4的化学键类型和晶体类型相同 D、干冰容易升华,是由于干冰中的共价键强度较弱19. 下列有关性质的比较中,不正确的是( )A、离子半径: B、沸点: C、晶格能: D、共价键的健能:20. 下列叙述不正确的是( )A、氯化钠晶胞中阴阳离子的配位数都为6 B、由非金属元素构成的化合物都是共价化合物 C、区分晶体和非晶体最可靠的科学方法是X-射线衍射实验 D、干冰晶胞中,每个分子周围距离最近且相等的分子有12个21. 下表所列物质晶体的类型全部正确的一组是( )
A、在晶体中,距最近的有6个,距最近且等距的共12个 B、在晶体中,每个晶胞平均占有4个 , 的配位数是4 C、在金刚石晶体中,每个碳原子被12个六元环共同占有,每个六元环最多有4个碳原子共面 D、该气态团簇分子的分子式为或 , 其晶体不导电17. 下列说法不正确的是( )A、HBr分子中存在极性共价键 B、KOH晶体中既有离子键又有共价键 C、NaCl晶体溶于水时有离子键的断裂 D、NH3分子中每个原子最外电子层都具有8电子稳定结构18. 下列说法正确的是( )A、HCl气体和蔗糖溶于水时,都破坏了共价键 B、H2O、H2S、H2Se的相对分子质量依次增大,熔点依次增大 C、NaOH和K2SO4的化学键类型和晶体类型相同 D、干冰容易升华,是由于干冰中的共价键强度较弱19. 下列有关性质的比较中,不正确的是( )A、离子半径: B、沸点: C、晶格能: D、共价键的健能:20. 下列叙述不正确的是( )A、氯化钠晶胞中阴阳离子的配位数都为6 B、由非金属元素构成的化合物都是共价化合物 C、区分晶体和非晶体最可靠的科学方法是X-射线衍射实验 D、干冰晶胞中,每个分子周围距离最近且相等的分子有12个21. 下表所列物质晶体的类型全部正确的一组是( )原子晶体
离子晶体
分子晶体
A
二氧化硅
硫酸
He
B
碳酸氢铵
C
金刚石
烧碱
白磷
D
铜
KOH
碘晶体
A、A B、B C、C D、D22. 有关晶体或晶胞结构如下图所示。下列说法错误的是( )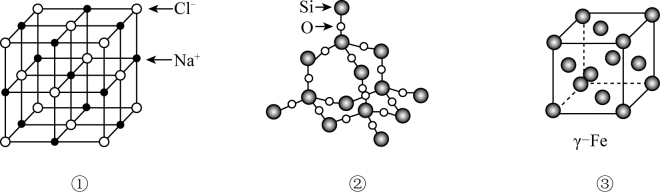 A、晶胞①中Na+的配位数为8 B、晶体②中Si和Si-O个数比为1:4 C、晶胞③中原子堆积方式为面心立方最密堆积 D、三种晶体中微粒间作用力均不相同23. 经研究证明,在固态时由空间结构分别为正四面体和正八面体的两种离子构成,下列关于的推断正确的是( )A、固体为分子晶体 B、晶体由和构成,且离子数之比为1:1 C、晶体由和构成,且离子数之比为1:1 D、晶体具有良好的导电性24. 纳米材料是当今材料科学研究的前沿,其研究成果广泛应用于催化及军事科学中。将纳米材料分散到液体分散剂中,所得混合物可能具有的性质是( )A、能全部透过半透膜 B、有丁达尔效应 C、所得液体不可以全部透过滤纸 D、所得物质一定是溶液25. 纳米材料是21世纪最有前途的新型材料之一,世界各国对这一新型材料给予了极大的关注。纳米粒子是指直径为1 ~ 100 nm的超细粒子(1 nm=10-9 m)。由于表面效应和体积效应,其常有奇特的光、电、磁、热等性质,可开发为新型功能材料,有关纳米粒子的叙述中错误的是( )A、因纳米粒子半径太小,故不能将其制成胶体 B、一定条件下,纳米粒子可催化水的分解 C、一定条件下,纳米TiO2陶瓷可任意弯曲,可塑性好 D、纳米粒子半径小,表面活性高26. 下列关于纳米材料基本构成微粒的叙述中,错误的是( )A、三维空间尺寸必须都处于纳米级 B、既不是微观粒子,也不是宏观物质 C、是原子排列成的纳米数量级原子团 D、是长程无序的一种结构状态
A、晶胞①中Na+的配位数为8 B、晶体②中Si和Si-O个数比为1:4 C、晶胞③中原子堆积方式为面心立方最密堆积 D、三种晶体中微粒间作用力均不相同23. 经研究证明,在固态时由空间结构分别为正四面体和正八面体的两种离子构成,下列关于的推断正确的是( )A、固体为分子晶体 B、晶体由和构成,且离子数之比为1:1 C、晶体由和构成,且离子数之比为1:1 D、晶体具有良好的导电性24. 纳米材料是当今材料科学研究的前沿,其研究成果广泛应用于催化及军事科学中。将纳米材料分散到液体分散剂中,所得混合物可能具有的性质是( )A、能全部透过半透膜 B、有丁达尔效应 C、所得液体不可以全部透过滤纸 D、所得物质一定是溶液25. 纳米材料是21世纪最有前途的新型材料之一,世界各国对这一新型材料给予了极大的关注。纳米粒子是指直径为1 ~ 100 nm的超细粒子(1 nm=10-9 m)。由于表面效应和体积效应,其常有奇特的光、电、磁、热等性质,可开发为新型功能材料,有关纳米粒子的叙述中错误的是( )A、因纳米粒子半径太小,故不能将其制成胶体 B、一定条件下,纳米粒子可催化水的分解 C、一定条件下,纳米TiO2陶瓷可任意弯曲,可塑性好 D、纳米粒子半径小,表面活性高26. 下列关于纳米材料基本构成微粒的叙述中,错误的是( )A、三维空间尺寸必须都处于纳米级 B、既不是微观粒子,也不是宏观物质 C、是原子排列成的纳米数量级原子团 D、是长程无序的一种结构状态二、多选题
-
27. 对晶胞的研究有助于我们了解整个晶体的结构。Cu晶胞的结构如图1所示(晶胞参数为a pm),CuSe晶胞的结构如图2所示,设NA为阿伏加德罗常数的值,下列说法正确的是( )
 A、Cu晶胞的密度为 B、图1中最近的两个Cu之间的距离为 C、填充在形成的正四面体空隙中 D、图2中1个晶胞含14个28. 以Li2O晶胞的某一顶点为原点建立坐标系,沿x、y、z轴的晶胞投影均如图所示。下列说法错误的是( )
A、Cu晶胞的密度为 B、图1中最近的两个Cu之间的距离为 C、填充在形成的正四面体空隙中 D、图2中1个晶胞含14个28. 以Li2O晶胞的某一顶点为原点建立坐标系,沿x、y、z轴的晶胞投影均如图所示。下列说法错误的是( ) A、熔点:Li2O>Na2O>K2O B、Li2O晶体中,O2-的配位数为6 C、Li2O晶体中,与O2-等距且最近的O2-个数为12 D、若Li2O的晶胞参数为anm,则Li+与O2-的最近距离为anm
A、熔点:Li2O>Na2O>K2O B、Li2O晶体中,O2-的配位数为6 C、Li2O晶体中,与O2-等距且最近的O2-个数为12 D、若Li2O的晶胞参数为anm,则Li+与O2-的最近距离为anm三、综合题
-
29. 我国科学家在铁基高温超导体的研究上取得重大突破,发现了该超导体是由Fe、Ba、As三种元素组成,这为进一步理解超导配对机理及其与电荷密度波的关系提供了重要实验证据。
回答下列问题:
(1)、Ba元素属于元素周期表的区元素。(2)、基态Fe原子核外电子排布式为 , 同周期中基态原子未成对电子数比Fe多的有种元素。(3)、As为第四周期第ⅤA族元素,与其同周期且相邻的元素分别为32Ge、34Se,三种元素的基态原子第一电离能由大到小的顺序为 , 原因为。(4)、的晶胞结构如图1所示。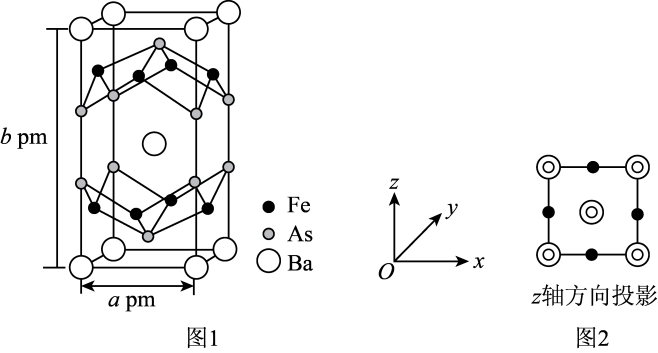
该晶体的化学式为 , 设NA表示阿伏加德罗常数的值,该晶体的密度是(用含a、b、NA的代数式表示)。
30. 我国科学家研发的全球首套千吨级太阳能燃料合成项目被形象地称为“液态阳光"计划。该项目通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢合成甲醇。回答下列问题: (1)、我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为ZnO/ZrO2固溶体。四方ZrO2晶胞如图甲所示。Zr4+ 离子在晶胞中的配位数是 , 晶胞参数为apm、a pm、c pm,该晶体密度为g·cm-3(写出表达式)。在ZrO2中掺杂少量ZnO后形成的催化剂,化学式可表示为ZnxZr1-xOy , 则y=(用x表达)。(2)、过渡金属元素铬(Cr)是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
(1)、我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为ZnO/ZrO2固溶体。四方ZrO2晶胞如图甲所示。Zr4+ 离子在晶胞中的配位数是 , 晶胞参数为apm、a pm、c pm,该晶体密度为g·cm-3(写出表达式)。在ZrO2中掺杂少量ZnO后形成的催化剂,化学式可表示为ZnxZr1-xOy , 则y=(用x表达)。(2)、过渡金属元素铬(Cr)是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
在金属材料中添加AlCr2颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。AlCr2具有体心四方结构,如图乙所示。处于顶角位置的是原子。设Cr和Al原子半径分别为rCr和rAl , 则金属原子空间占有率为%(列出计算表达式)。