山东省东营市河口区2023年中考二模化学试题
试卷更新日期:2023-05-08 类型:中考模拟
一、单选题
-
1. 2023年3月27日是第28个全国中小学生安全教育日,下列标识与安全无关的是A、
 B、
B、 C、
C、 D、
D、 2. 我国提出争取在2030年前实现碳达峰、2060年前实现碳中和。碳中和是指CO2的排放总量和减少总量相当。下列措施中能促进碳中和最直接有效的是A、大力推广使用脱硫煤 B、加快煤的开采与使用,大力发展经济 C、大规模开采可燃冰作为新能源 D、用氨水捕集废气中的CO2 , 将其转化为氮肥3. 宏微结合是化学学科特有的思维方式。下列对宏观事实的微观解释错误的是( )A、水蒸气冷凝变成液态水,体积减小—一温度降低,分子变小 B、气体容易被压缩一一气体分子间隔较大 C、一氧化碳能燃烧,二氧化碳不能燃烧一一不同种分子的性质不同 D、稀盐酸和稀硫酸化学性质相似—一溶液中都含有氢离子4. 贵州茅台酒是中国的国酒,其主要成分是乙醇(C2H5OH)。下列说法正确的是A、乙醇由2个碳原子,6个氢原子,1个氧原子构成 B、乙醇中碳、氢、氧三种元素的质量比为2:6:1 C、乙醇是由碳元素、氢元素、氧元素组成的 D、乙醇中氧元素的质量分数最大5. 化学实验是化学科学发展和化学学习的重要途径。下列实验操作正确的是( )A、分离溶液中的固态物质
2. 我国提出争取在2030年前实现碳达峰、2060年前实现碳中和。碳中和是指CO2的排放总量和减少总量相当。下列措施中能促进碳中和最直接有效的是A、大力推广使用脱硫煤 B、加快煤的开采与使用,大力发展经济 C、大规模开采可燃冰作为新能源 D、用氨水捕集废气中的CO2 , 将其转化为氮肥3. 宏微结合是化学学科特有的思维方式。下列对宏观事实的微观解释错误的是( )A、水蒸气冷凝变成液态水,体积减小—一温度降低,分子变小 B、气体容易被压缩一一气体分子间隔较大 C、一氧化碳能燃烧,二氧化碳不能燃烧一一不同种分子的性质不同 D、稀盐酸和稀硫酸化学性质相似—一溶液中都含有氢离子4. 贵州茅台酒是中国的国酒,其主要成分是乙醇(C2H5OH)。下列说法正确的是A、乙醇由2个碳原子,6个氢原子,1个氧原子构成 B、乙醇中碳、氢、氧三种元素的质量比为2:6:1 C、乙醇是由碳元素、氢元素、氧元素组成的 D、乙醇中氧元素的质量分数最大5. 化学实验是化学科学发展和化学学习的重要途径。下列实验操作正确的是( )A、分离溶液中的固态物质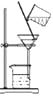 B、稀释浓硫酸
B、稀释浓硫酸 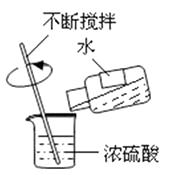 C、配制溶液
C、配制溶液 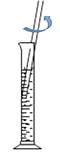 D、测试某溶液的酸碱度
D、测试某溶液的酸碱度  6. 下列化学用语书写正确的是A、2个铁离子:2Fe2+ B、氖气:Ne2 C、金元素:AU D、两个氮分子2N27. 逻辑推理是化学学习中常用的思维方法。下列推理正确的是A、铝的金属活动性比铁强,则铝制品比铁制品更容易锈蚀 B、化合物是由不同元素组成的纯净物,所以由不同种元素组成的纯净物一定是化合物 C、铵态氮肥遇到可溶性碱能释放出氨气,则所有的氮肥遇到可溶性碱能释放出氨气 D、活泼金属能与稀硫酸反应放出气体,则能与稀硫酸反应放出气体的物质一定是活泼金属8. 利津水煎包是东营的地方名吃,其特色在于兼得水煮油煎之妙,色泽金黄,一面焦脆,三面嫩软,皮薄馅大,香而不腻。在水煎包的制作过程中,以下说法正确的个数是
6. 下列化学用语书写正确的是A、2个铁离子:2Fe2+ B、氖气:Ne2 C、金元素:AU D、两个氮分子2N27. 逻辑推理是化学学习中常用的思维方法。下列推理正确的是A、铝的金属活动性比铁强,则铝制品比铁制品更容易锈蚀 B、化合物是由不同元素组成的纯净物,所以由不同种元素组成的纯净物一定是化合物 C、铵态氮肥遇到可溶性碱能释放出氨气,则所有的氮肥遇到可溶性碱能释放出氨气 D、活泼金属能与稀硫酸反应放出气体,则能与稀硫酸反应放出气体的物质一定是活泼金属8. 利津水煎包是东营的地方名吃,其特色在于兼得水煮油煎之妙,色泽金黄,一面焦脆,三面嫩软,皮薄馅大,香而不腻。在水煎包的制作过程中,以下说法正确的个数是①水煎包“香气四溢”,说明分子在不断运动
②水煎包“皮薄馅大”,皮中的糖类是人体的主要供能物质
③木柴燃烧用扇子越扇火焰越旺,是因为为燃料提供了足够的氧气
④往热锅内倒入水会产生大量的“白气”,发生了化学变化
A、1 B、2 C、3 D、49. 某可燃物4.6g 在足量氧气充分燃烧,生成8.8g 二氧化碳和5.4g 水,则该可燃物的组成为A、一定含碳、氢、氧三种元素元素 B、一定含碳、氢元素,可能含氧元素 C、一定含碳、氢元素,不含氧元素 D、所含元素大于三种10. 向一定量Cu(NO3)2和 AgNO3的混合溶液中加入镁粉,充分反应后过滤,得到滤液和滤渣。下列有关说法正确的是A、向滤渣中加入稀硫酸一定产生气泡 B、若滤液为蓝色,则滤渣中一定只有银 C、若向滤液中加入稀盐酸不产生白色沉淀,滤液中一定有Mg(NO3)2和Cu(NO3)2 D、滤液中溶质的成分最多有三种11. 甲烷(CH4)和水反应可以制水煤气,其反应的微观示意图如图,下列叙述正确的是( )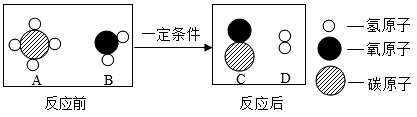 A、甲烷中碳元素的质量分数为20% B、甲烷(CH4)中碳元素化合价为+4价 C、反应前后分子数目不变 D、该反应中,生成C和D的分子个数比为1:312. 下列实验方案合理的是
A、甲烷中碳元素的质量分数为20% B、甲烷(CH4)中碳元素化合价为+4价 C、反应前后分子数目不变 D、该反应中,生成C和D的分子个数比为1:312. 下列实验方案合理的是选项
实验目的
实验方案
A
检验CO2气体
用燃着的木条伸入瓶内,观察火焰是否熄灭
B
除去CO2中的少量HCl气体
先通过足量NaOH溶液,再通过浓硫酸
C
除去NaOH溶液中的Na2CO3
加入过量澄清石灰水,充分反应后过滤
D
鉴别合成纤维和羊毛
取样,分别点燃,闻气味
A、A B、B C、C D、D二、填空题
-
13. 回答问题(1)、中国“天问一号”探测器和首个火星车祝融号成功着陆火星,“天问一号”上应用了新型镁锂合金材料是由西安四方超轻材料有限公司自主研发。回答下列问题:


①祝融号着陆后,展开太阳能板,把太阳能转化为能。
②图1为镁在元素周期表中的部分信息,则镁的相对原子质量为。图2为几种粒子的结构示意图,其中属于同种元素的是(填序号),与镁元素化学性质相似的是(填序号)。
③锂原子(Li)在反应中易失去 1 个电子形成锂离子,写出锂离子的符号。
(2)、酸碱中和反应在日常生活和工农业生产中都有重要的应用。中和反应在生活中有着广泛应用,如胃酸过多的病人可以服用氢氧化镁的药物,此时的原理可以用化学方程式表示为;在农业上也有应用,如pH小于5的土壤常常可以施用适量的来改良;化工生产中产生的废水(溶质以HCl计)小王同学认为可以用消石灰,小李同学认为可以用氢氧化钾,小王同学方案的优点是。
14. 金属和金属化合物在人类的生产、生活中起着重要的作用。(1)、“奋斗者号”载人潜水器的外壳和载人舱由强度高、抗压力强的钛合金制造,钛合金属于____。A、合成材料 B、金属材料 C、天然材料 D、复合材料(2)、工业上通常是在高温条件下,用四氯化钛(TiCl4)与金属镁反应获得钛和氯化镁,该反应的化学方程式为。(3)、下列有关金属的说法错误的是____。A、铁在潮湿空气中易生锈 B、常温下金属均为固态 C、回收利用废金属意义重大 D、合金硬度一般比组成合金的纯金属大15. 化学与人类生活息息相关。根据所学化学知识回答下列问题:(1)、某校食堂周二午餐食谱的部分内容。主食
米饭
副食
清蒸排骨、咸味花生米、红烧鱼
从营养均衡的角度分析,该午餐缺少的一种营养素是。为补充该营养素,建议增加(选填字母序号)。
A.凉拌黄瓜 B.可乐鸡翅 C.酱牛肉 D.炒鸡蛋
(2)、走进厨房,你会发现煤气罐被管道天然气代替了,其主要成分在空气中充分燃烧的化学方程式为。(3)、使用铁强化酱油可预防贫血,铁属于人体所需的(填“常量”或“微量”)元素。(4)、“84”消毒液的有效成分次氯酸钠(NaClO)属于____(填序号)。A、酸 B、碱 C、盐 D、氧化物(5)、中学生应有一定的安全常识。下列说法错误的是____A、室内起火时,立即打开所有门窗通风 B、炒菜油锅内着火,立即盖上锅盖灭火 C、在加油站、加气站使用手机可能引发燃烧、爆炸 D、逃离火灾现场时,可用湿毛巾捂住口鼻,并尽量贴近地面逃离三、综合题
-
16. 化学是认识、改造和应用物质的科学。从海水中提取镁、制“碱”,都体现了人类改造物质的智慧。结合下列流程图(其中部分操作和条件已略去),请回答相关问题:
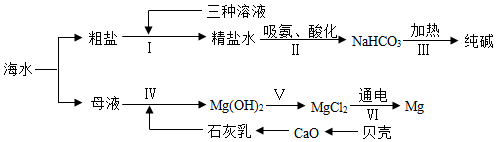 (1)、提纯物质常用转化的方法,就是将杂质转化为沉淀或气体而除去。粗盐中含有氯化镁、硫酸钠、氯化钙等可溶性杂质,通过步骤Ⅰ,再利用过滤操作进行除杂。步骤Ⅰ加入下列三种溶液的先后顺序错误的是____(填字母序号)。
(1)、提纯物质常用转化的方法,就是将杂质转化为沉淀或气体而除去。粗盐中含有氯化镁、硫酸钠、氯化钙等可溶性杂质,通过步骤Ⅰ,再利用过滤操作进行除杂。步骤Ⅰ加入下列三种溶液的先后顺序错误的是____(填字母序号)。①稍过量的Na2CO3溶液 ②稍过量的BaCl2溶液 ③稍过量的NaOH溶液
A、①②③ B、②①③ C、③②① D、③①②(2)、母液中有MgCl2 , 却经历了步骤Ⅳ、Ⅴ的转化过程,其目的是。(3)、为“制碱”工业做出巨大贡献的中国科学家: , 氨厂的原料N2来自空气,分离液态空气是利用空气中各成分的不同。(4)、写出Ⅱ中发生反应的化学方程式为。(5)、若向分离出NaHCO3晶体后的母液(NH4Cl)中加入过量的Ca(OH)2 , 可获的一种可以循环使用的物质,其化学式是。(6)、上述流程图中没有涉及的基本反应类型是。四、填空题
-
17. 如图是 MgCl2、KCl、MgSO4的溶解度曲线,回答问题:
 (1)、P点的意义是。(2)、t2℃时,向40g的MgCl2中加入50g水,充分溶解后,所得溶液的质量为 , 将其升高到t3℃时,所得溶液中溶质和溶液质量最简比为。(3)、将t2℃时KCl和MgSO4的饱和溶液升温至t3℃时,所得溶液中溶质质量分数由大到小的关系是KClMgSO4(填大于或小于)。(4)、下列说法正确的是(填序号)。
(1)、P点的意义是。(2)、t2℃时,向40g的MgCl2中加入50g水,充分溶解后,所得溶液的质量为 , 将其升高到t3℃时,所得溶液中溶质和溶液质量最简比为。(3)、将t2℃时KCl和MgSO4的饱和溶液升温至t3℃时,所得溶液中溶质质量分数由大到小的关系是KClMgSO4(填大于或小于)。(4)、下列说法正确的是(填序号)。①把KCl饱和溶液变成不饱和溶液的措施只有一种
②t2℃时,170gMgCl2的饱和溶液中含有70gMgCl2
③KCl和MgSO4溶液从t2℃降到t1℃时,析出晶体的质量相等
④饱和KCl溶液析出晶体后,溶液中的溶质质量分数可能不变
18. 实验室制取气体需要的一些装置如图1所示,请回答下列问题。
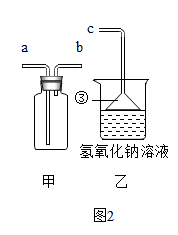 (1)、写出标有序号的仪器名称:① , ②。(2)、实验室制取氧气和二氧化碳的发生装置都可选用B装置的原因是 , 装置中使用分液漏斗的优点是。(3)、使用图一装置,若要得到干燥的氧气,所选择装置的连接顺序为:B→(填字母序号)。(4)、检验二氧化碳是否收集满的操作方法是。(5)、某兴趣小组的同学连接B、G、H装置进行实验。若实验时G装置中蜡烛燃烧更剧烈,H装置中溶液变浑浊,则 B装置中反应的化学方程式为。(6)、二氧化硫气体是一种有刺激性气味的有毒气体,实验室制取SO2气体时需进行尾气处理,二氧化硫的密度比空气大,且会与氢氧化钠溶液反应,用图2甲、乙装置收集并处理尾气的连接顺序为:(填管口abc的先后顺序),乙装置中漏斗的作用为。(7)、科学探究是认识和解决化学问题的重要实践活动。
(1)、写出标有序号的仪器名称:① , ②。(2)、实验室制取氧气和二氧化碳的发生装置都可选用B装置的原因是 , 装置中使用分液漏斗的优点是。(3)、使用图一装置,若要得到干燥的氧气,所选择装置的连接顺序为:B→(填字母序号)。(4)、检验二氧化碳是否收集满的操作方法是。(5)、某兴趣小组的同学连接B、G、H装置进行实验。若实验时G装置中蜡烛燃烧更剧烈,H装置中溶液变浑浊,则 B装置中反应的化学方程式为。(6)、二氧化硫气体是一种有刺激性气味的有毒气体,实验室制取SO2气体时需进行尾气处理,二氧化硫的密度比空气大,且会与氢氧化钠溶液反应,用图2甲、乙装置收集并处理尾气的连接顺序为:(填管口abc的先后顺序),乙装置中漏斗的作用为。(7)、科学探究是认识和解决化学问题的重要实践活动。近年来,自热食品种类繁多。只需将撕去塑料膜的发热包放入凉水中,就能享用美食,很受年轻人的追捧。实验小组同学买来一份自热食品进行以下探究。
【资料】
Ⅰ、发热包中物质的主要成分是生石灰、碳酸钠、铝粒。
Ⅱ、铝能和NaOH溶液反应生成偏铝酸钠(NaAlO2)和氢气,偏铝酸钠溶于水。
小组同学取出发热包,撕去塑料膜,放入适量凉水中,感觉发热,固体迅速膨胀。一段时间后固体变硬结块,写出变硬可能的原因(用化学方程式表示)。在使用发热包过程中,禁止明火的理由是。
五、计算题
-
19. 为了检测石灰石样品中碳酸钙的含量,这几位同学在烧杯中用浓度相同的盐酸与样品充分反应来进行实验测定,(样品中的杂质不溶于水,且不与盐酸反应)测定数据如下:
实验
甲同学
乙同学
丙同学
丁同学
戊同学
取石灰石样品质量(g)
10.0
10.0
10.0
10.0
10.0
加入盐酸的质量(g)
10.0
20.0
30.0
40.0
50.0
烧杯中剩余物质的总质量(g)
19.0
28.0
37.0
46.7
56.7
试回答:
(1)、甲、乙、丙、丁四位同学里面,同学的石灰石样品完全反应;(2)、10.0g石灰石样品最多产生多少克CO2。(3)、求样品中碳酸钙的质量分数(写出计算过程)。
-