吉林省白山市靖宇县2023年中考一模化学试题
试卷更新日期:2023-05-04 类型:中考模拟
一、单选题
-
1. 2021年CCTV中秋晚会主会场设在西昌。下列烘托晚会气氛的场景中蕴含化学变化的是( )A、彩旗飘扬 B、燃放烟花 C、气球升空 D、歌声嘹亮2. 元素周期表是学习化学的工具。发现元素周期律并编制元素周期表的化学家是( )A、拉瓦锡 B、道尔顿 C、门捷列夫 D、阿伏加德罗3. 空气是一种宝贵的自然资源。在空气的成分中,能供给动植物呼吸的是( )A、氮气 B、氧气 C、稀有气体 D、二氧化碳4. 下列图示是同学们在实验考试中的具体操作,正确的是( )A、取用固体
 B、过滤液体
B、过滤液体 C、验满气体
C、验满气体 D、测定溶液的pH
D、测定溶液的pH 5. “等一帘烟雨,候十里春风”,是对二十四节气中“雨水”的形象描述。随着“雨水”之后雨量的增多,空气湿度逐渐增大的原因是( )A、每个水分子体积变大 B、水分子分解加快 C、每个水分子质量增大 D、水分子数目增多6. 生活中一些常见物质的 pH 如下:厕所清洁剂 pH=1、食盐水 pH=7、肥皂水 pH=10、炉具清洁剂 pH=12,其中碱性最强的是( )A、厕所清洁剂 B、食盐水 C、肥皂水 D、炉具清洁剂7. 加热是最常见的反应条件,这一基本实验操作常要使用酒精灯。下列说法中正确的是( )A、若没有火柴或打火机,可用酒精灯引燃另一只酒精灯 B、绝对禁止向燃着的酒精灯里添加酒精,以免失火 C、用酒精灯加热试管里的液体时,要用酒精灯的内焰加热 D、用完酒精灯后,既可用嘴吹灭,又可用灯帽盖灭8. 工业上用CO2和NH3合成尿素【CO(NH2)2】,转化过程如图。下列说法正确的是( )
5. “等一帘烟雨,候十里春风”,是对二十四节气中“雨水”的形象描述。随着“雨水”之后雨量的增多,空气湿度逐渐增大的原因是( )A、每个水分子体积变大 B、水分子分解加快 C、每个水分子质量增大 D、水分子数目增多6. 生活中一些常见物质的 pH 如下:厕所清洁剂 pH=1、食盐水 pH=7、肥皂水 pH=10、炉具清洁剂 pH=12,其中碱性最强的是( )A、厕所清洁剂 B、食盐水 C、肥皂水 D、炉具清洁剂7. 加热是最常见的反应条件,这一基本实验操作常要使用酒精灯。下列说法中正确的是( )A、若没有火柴或打火机,可用酒精灯引燃另一只酒精灯 B、绝对禁止向燃着的酒精灯里添加酒精,以免失火 C、用酒精灯加热试管里的液体时,要用酒精灯的内焰加热 D、用完酒精灯后,既可用嘴吹灭,又可用灯帽盖灭8. 工业上用CO2和NH3合成尿素【CO(NH2)2】,转化过程如图。下列说法正确的是( )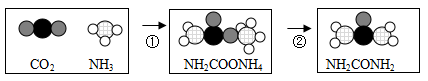 A、反应①是化合反应 B、反应②原子个数减少 C、尿素中氮元素的质量分数为36.7% D、施用尿素主要是为了增强作物抗旱能力9. “民以食为天, 食以安为先”。 下列说法正确的是( )A、霉变大米蒸煮后食用 B、亚硝酸钠可代替食盐 C、味精常用于菜品增鲜 D、福尔马林用于食品防腐10. 下列实验方案设计正确的是( )
A、反应①是化合反应 B、反应②原子个数减少 C、尿素中氮元素的质量分数为36.7% D、施用尿素主要是为了增强作物抗旱能力9. “民以食为天, 食以安为先”。 下列说法正确的是( )A、霉变大米蒸煮后食用 B、亚硝酸钠可代替食盐 C、味精常用于菜品增鲜 D、福尔马林用于食品防腐10. 下列实验方案设计正确的是( )选项
实验目的
实验方案
A
检验某物质中是否含有Na2CO3
加入足量稀盐酸,观察是否产生气泡
B
分离木炭粉和铁粉的混合物
加入足量稀硫酸,过滤、洗涤、干燥
C
除去O2中混有的CO(质量比为1:1)
先通过灼热CuO,再通过足量NaOH溶液,干燥
D
除去CuCl2溶液中混有的NaCl
加入足量NaOH溶液,过滤,向滤渣中加入适量稀盐酸
A、A B、B C、C D、D二、填空题
-
11. 用化学用语填空:(1)、氢元素。(2)、6个氢原子。(3)、6个氢分子。(4)、6个氢离子。12. 下图为元素周期表中部分元素的相关信息,请根据所给信息按要求填空。
 (1)、从上表中可知,碳元素的相对原子质量是。氩原子核内的质子数是。(2)、由原子序数为8和13两种元素组成的化合物是。(填化学式)13. 中国承诺在2030年前实现碳达峰,2060年前实现碳中和,请回答下列问题。(1)、造成温室效应加剧主要是因煤、和天然气等化石燃料燃烧都会产生CO2;(2)、若CO2能合理利用,能与H2在催化剂条件下反应生成甲醇,反应的方程式为 , X的化学式为;(3)、下列做法有利于实现碳中和的是____。A、积极植树造林 B、利用风能实现清洁发电 C、大量使用一次性餐具 D、垃圾焚烧处理14. 水是生命之源。
(1)、从上表中可知,碳元素的相对原子质量是。氩原子核内的质子数是。(2)、由原子序数为8和13两种元素组成的化合物是。(填化学式)13. 中国承诺在2030年前实现碳达峰,2060年前实现碳中和,请回答下列问题。(1)、造成温室效应加剧主要是因煤、和天然气等化石燃料燃烧都会产生CO2;(2)、若CO2能合理利用,能与H2在催化剂条件下反应生成甲醇,反应的方程式为 , X的化学式为;(3)、下列做法有利于实现碳中和的是____。A、积极植树造林 B、利用风能实现清洁发电 C、大量使用一次性餐具 D、垃圾焚烧处理14. 水是生命之源。 (1)、黄河水经沉降、吸附、杀菌消毒等净化过程可得到自来水,自来水属于(填“混合物”或“纯净物”)。(2)、饮用硬度过大的水不利于人体健康,生活中常用检验水是硬水还是软水。(3)、如图是电解水的实验装置图,连接正负两极的玻璃管内产生的气体体积比为。15. 金属及金属材料在生产、生活中应用广泛。(1)、向一定质量的氧化铜中加入一定量的稀硫酸使其完全溶解,得到蓝色溶液。再加入铁粉充分反应,过滤,得到滤渣和滤液。向滤渣中加入稀硫酸,有气泡冒出,则滤液中的溶质是(填化学式)。(2)、早在春秋战国时期,我国就开始生产和使用铁器。炼铁原理是利用一氧化碳与氧化铁在高温条件下反应,该反应的化学方程式为。
(1)、黄河水经沉降、吸附、杀菌消毒等净化过程可得到自来水,自来水属于(填“混合物”或“纯净物”)。(2)、饮用硬度过大的水不利于人体健康,生活中常用检验水是硬水还是软水。(3)、如图是电解水的实验装置图,连接正负两极的玻璃管内产生的气体体积比为。15. 金属及金属材料在生产、生活中应用广泛。(1)、向一定质量的氧化铜中加入一定量的稀硫酸使其完全溶解,得到蓝色溶液。再加入铁粉充分反应,过滤,得到滤渣和滤液。向滤渣中加入稀硫酸,有气泡冒出,则滤液中的溶质是(填化学式)。(2)、早在春秋战国时期,我国就开始生产和使用铁器。炼铁原理是利用一氧化碳与氧化铁在高温条件下反应,该反应的化学方程式为。三、综合题
-
16. 实验小组同学设计了如下实验探究燃烧的条件,请你参与下列实验:
 (1)、实验一中棉球上的酒精燃烧,水不燃烧,由此可得出燃烧的条件之一是。(2)、实验二中木屑先燃烧,煤粉后燃烧,由此可知木屑的着火点比煤粉(填“高”或“低”)。(3)、实验三中升高左侧漏斗使红磷露出水面,红磷不燃烧,原因是。17. 甲、乙两种固体(均不含结晶水)的溶解度曲线如图2所示,请回答下列问题:
(1)、实验一中棉球上的酒精燃烧,水不燃烧,由此可得出燃烧的条件之一是。(2)、实验二中木屑先燃烧,煤粉后燃烧,由此可知木屑的着火点比煤粉(填“高”或“低”)。(3)、实验三中升高左侧漏斗使红磷露出水面,红磷不燃烧,原因是。17. 甲、乙两种固体(均不含结晶水)的溶解度曲线如图2所示,请回答下列问题:
 (1)、t3℃时,乙的溶解度是g。(2)、t3℃时,甲形成的饱和溶液中溶质与溶液的质量比为。(3)、t1℃,把等质量甲,乙两种物质分别放入两只烧杯中,加入100g水,充分搅拌,溶解情况如图1所示,则B烧杯内溶质是(填“甲”或“乙”)。18. 制取气体是初中化学实验的重要内容,根据要求回答下列问题:
(1)、t3℃时,乙的溶解度是g。(2)、t3℃时,甲形成的饱和溶液中溶质与溶液的质量比为。(3)、t1℃,把等质量甲,乙两种物质分别放入两只烧杯中,加入100g水,充分搅拌,溶解情况如图1所示,则B烧杯内溶质是(填“甲”或“乙”)。18. 制取气体是初中化学实验的重要内容,根据要求回答下列问题: (1)、写出标有序号的仪器名称:①。(2)、实验室利用大理石和稀盐酸反应制取二氧化碳,可选择的发生装置是(填字母序号下同)。(3)、某气体只能用C装置收集,则该气体可能具有的性质为。
(1)、写出标有序号的仪器名称:①。(2)、实验室利用大理石和稀盐酸反应制取二氧化碳,可选择的发生装置是(填字母序号下同)。(3)、某气体只能用C装置收集,则该气体可能具有的性质为。a.能与水反应
b.能与空气中的某些成分发生反应
c.密度与空气接近
(4)、某兴趣小组的同学连接B、G、H装置进行实验。若实验时G装置中蜡烛燃烧更剧烈,H装置中溶液变浑浊,则B装置中反应的化学方程式为。19. CuSO4是化学实验中常见试剂。(1)、验证质量守恒定律。步骤1:在锥形瓶中加入适量的CuSO4溶液,塞好橡胶塞。将几根铁钉用砂纸打磨干净,将盛有CuSO4溶液的锥形瓶和铁钉一起放在托盘天平上称量,记录所称质量为m1。
步骤2:将铁钉浸入CuSO4溶液中,塞好橡胶塞。观察实验现象,待反应有明显现象后,将盛有CuSO4溶液和铁钉的锥形瓶一起放在托盘天平上称量,记录所称质量为m2。
①用砂纸将铁钉打磨干净的作用是。
②步骤2中发生反应的化学方程式是。该变化可说明Fe和Cu的金属活动性由强到弱的顺序是。
③若m1=m2 , 可证明参加反应的Fe和CuSO4的质量总和等于。
(2)、探究CuSO4溶液对H2O2分解具有催化作用。①若要证明CuSO4溶液对H2O2分解具有催化作用,除需证明CuSO4在反应前后化学性质和质量不发生改变外,还需证明的是。
②为探究CuSO4在反应前后质量是否发生改变,某同学设计如下实验:
向H2O2溶液中滴入10ga%的CuSO4溶液,待反应完全后,向试管中加入足量的BaCl2溶液,产生沉淀,过滤、洗涤、干燥,称量沉淀物为bg。
上述实验步骤中若缺少“洗涤、干燥”,则通过沉淀物bg计算出溶液中CuSO4的质量(填“大于”“小于”或“等于”)0.1ag。
四、计算题
-
20. 工业上用N2和H2合成NH3是人类科学技术的一项重大突破。NH3与氰酸(HOCN)反应生成尿素【CO(NH2)2】。(1)、尿素为农作物生长提供的主要营养元素为。(2)、尿素可用于去除大气污染物中的NO,其化学反应为。若去除废气中6gNO,理论上所质量分数为10%的尿素溶液的质量是多少?