河南省濮阳市2023年中考一模化学试题
试卷更新日期:2023-04-28 类型:中考模拟
一、单选题
-
1. 下列变化属于化学变化的是( )A、铁杵磨针 B、烧制瓷器 C、石蜡熔化 D、活字印刷2. 河南地处中原,物产丰富,下列特产中富含蛋白质的是( )A、铁棍山药 B、原阳大米 C、黄河鲤鱼 D、新郑大枣3. 下列图示的实验操作正确的是( )A、
 过滤
B、
过滤
B、 称取氯化钠
C、
称取氯化钠
C、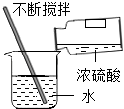 稀释浓硫酸
D、
稀释浓硫酸
D、 测溶液的pH值
4. 下列物质由分子构成的是( )A、金属铜 B、硫酸铜 C、硅 D、蒸馏水5. 下列与水有关的说法正确的是( )A、溶液中的溶剂一定是水 B、活性炭可吸附水中的色素及异味 C、将硬水过滤可以得到软水 D、电解水生成氢气和氧气的质量比为2:16. 分类法是化学学习的重要方法。下列物质分类正确的是( )A、碱:火碱、纯碱 B、合成材料:塑料、蚕丝 C、人体必需的微量元素:铁、锌 D、有机化合物:干冰、乙醇7. 液氢有望取代氢能,成为重要的新一代绿色能源。液氨作为清洁能源的反应原理是。则X的化学式为( )A、H2O B、N2O C、NO D、NO28. 随着新能源汽车的发展,作为锂电池关键材料的镍成为备受关注的金属材料。其相关信息如图所示,下列有关说法错误的是( )
测溶液的pH值
4. 下列物质由分子构成的是( )A、金属铜 B、硫酸铜 C、硅 D、蒸馏水5. 下列与水有关的说法正确的是( )A、溶液中的溶剂一定是水 B、活性炭可吸附水中的色素及异味 C、将硬水过滤可以得到软水 D、电解水生成氢气和氧气的质量比为2:16. 分类法是化学学习的重要方法。下列物质分类正确的是( )A、碱:火碱、纯碱 B、合成材料:塑料、蚕丝 C、人体必需的微量元素:铁、锌 D、有机化合物:干冰、乙醇7. 液氢有望取代氢能,成为重要的新一代绿色能源。液氨作为清洁能源的反应原理是。则X的化学式为( )A、H2O B、N2O C、NO D、NO28. 随着新能源汽车的发展,作为锂电池关键材料的镍成为备受关注的金属材料。其相关信息如图所示,下列有关说法错误的是( ) A、镍原子原子序数为28 B、镍元素相对原子质量是58.69g C、镍属于金属元素 D、镍原子核外有28个电子9. 下列实验方案设计能达到目的的是( )A、加熟石灰研磨区分硫酸铵和氯化铵 B、通过点燃的方法,除去CO2中的CO C、铁丝插入硫酸铜溶液中,验证铁、铜金属活动性 D、将稀盐酸滴入盛有碳酸钠粉末的试管中,验证质量守恒定律10. 科研人员制备了一种新型纳米催化剂,在其表面发生某反应的微观示意图如下图所示。下列说法中错误的是( )
A、镍原子原子序数为28 B、镍元素相对原子质量是58.69g C、镍属于金属元素 D、镍原子核外有28个电子9. 下列实验方案设计能达到目的的是( )A、加熟石灰研磨区分硫酸铵和氯化铵 B、通过点燃的方法,除去CO2中的CO C、铁丝插入硫酸铜溶液中,验证铁、铜金属活动性 D、将稀盐酸滴入盛有碳酸钠粉末的试管中,验证质量守恒定律10. 科研人员制备了一种新型纳米催化剂,在其表面发生某反应的微观示意图如下图所示。下列说法中错误的是( ) A、反应物中碳元素化合价为+4 B、若广泛应用,有利于实现“碳中和” C、该反应中共有2种氧化物 D、该反应的化学方程式为11. 下列有关实验现象描述正确的是( )A、打开浓盐酸瓶塞,瓶口产生大量白烟 B、氢氧化钙溶液长久放置,内壁出现白色物质 C、硫在空气中燃烧,发出明亮的蓝紫色火焰 D、细铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁12. 加入盐酸后,下列转化能一步实现的是( )
A、反应物中碳元素化合价为+4 B、若广泛应用,有利于实现“碳中和” C、该反应中共有2种氧化物 D、该反应的化学方程式为11. 下列有关实验现象描述正确的是( )A、打开浓盐酸瓶塞,瓶口产生大量白烟 B、氢氧化钙溶液长久放置,内壁出现白色物质 C、硫在空气中燃烧,发出明亮的蓝紫色火焰 D、细铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁12. 加入盐酸后,下列转化能一步实现的是( )①Ag→AgCl ②BaCO3→BaCl2 ③Fe2O3→FeCl2 ④Cu(OH)2→CuCl2
A、②④ B、②③ C、①② D、③④13. 下列有关图示正确的是( )A、 电解水
B、
电解水
B、 向一定量稀氢氧化钠溶液中滴入水
C、
向一定量稀氢氧化钠溶液中滴入水
C、 向一定量氯化铜溶液中加入一定量铝
D、
向一定量氯化铜溶液中加入一定量铝
D、 向一定质量的盐酸和氯化钙混合溶液中滴加碳酸钠溶液
14. 取16g氧化铜和氧化铁的混合物,加入一定量的盐酸,恰好完全反应后,溶液中溶质的质量可能是( )A、27g B、32.8g C、32.5g D、30.1g
向一定质量的盐酸和氯化钙混合溶液中滴加碳酸钠溶液
14. 取16g氧化铜和氧化铁的混合物,加入一定量的盐酸,恰好完全反应后,溶液中溶质的质量可能是( )A、27g B、32.8g C、32.5g D、30.1g二、填空题
-
15. 用化学用语填空:空气中含量最高且常用作保护气的是;铁生锈是因为铁与接触发生反应;农业上可作复合肥料的物质是(写出一种)。16. 欲配制80g溶质质量分数为15%的氯化钠溶液,需要称量氯化钠固体的质量为g,量取水时用到的仪器有。若配制的溶液溶质质量分数小于15%,可能的不正确操作是。(写一条即可)17. 请用化学方程式解释下列现象。(1)、铝比铁活泼,但铝比铁更耐腐蚀。。(2)、正常雨水的pH约为5.6。。18. 甲和乙两种固体的溶解度曲线如图所示,请据图回答下列问题:
 (1)、℃时,甲、乙两种物质的饱和溶液中溶质的质量分数相等。(2)、若甲物质中混有少量乙物质,提纯甲的方法为。(3)、t2℃时,向75g甲的饱和溶液中加75g水,所得溶液的溶质质量分数为。
(1)、℃时,甲、乙两种物质的饱和溶液中溶质的质量分数相等。(2)、若甲物质中混有少量乙物质,提纯甲的方法为。(3)、t2℃时,向75g甲的饱和溶液中加75g水,所得溶液的溶质质量分数为。三、综合题
-
19. A、B、C是三种不同类别的物质,且均含有同一种元素,它们之间的转化关系如图。
 (1)、若A,B,C中均含有人体中含量最高的金属元素,B是白色难溶固体,其中金属元素的质量分数是40%,则C物质的一种用途为;C→B转化的化学方程式是。(2)、若B物质的溶液呈蓝色,常用来配制农药波尔多液;A是红色单质。则C→B转化的化学方程式为。20. 在点燃的条件下5.2gC2H2与14.4gO2恰好完全反应,生成13.2gCO2、3.6gH2O和xgCO,则x= , 其反应的化学方程式为。21. 请解释下列现象。(1)、加压时,3000L氧气可装人容积为20L的钢瓶中。(2)、探究燃烧条件的实验如图所示。Y形管中白磷燃烧,红磷没燃烧。红磷没有燃烧的原因是什么?。
(1)、若A,B,C中均含有人体中含量最高的金属元素,B是白色难溶固体,其中金属元素的质量分数是40%,则C物质的一种用途为;C→B转化的化学方程式是。(2)、若B物质的溶液呈蓝色,常用来配制农药波尔多液;A是红色单质。则C→B转化的化学方程式为。20. 在点燃的条件下5.2gC2H2与14.4gO2恰好完全反应,生成13.2gCO2、3.6gH2O和xgCO,则x= , 其反应的化学方程式为。21. 请解释下列现象。(1)、加压时,3000L氧气可装人容积为20L的钢瓶中。(2)、探究燃烧条件的实验如图所示。Y形管中白磷燃烧,红磷没燃烧。红磷没有燃烧的原因是什么?。 22. 实验室可选择下图所示装置来制取气体。
22. 实验室可选择下图所示装置来制取气体。 (1)、写出用装置A制取二氧化碳的化学方程式。(2)、若用装置A制取氧气,请在图中方框内填写对应的药品。(3)、若用装置B干燥氢气,气体应从导管口通入。23. 下图为模拟炼铁原理的装置,请回答下列问题。
(1)、写出用装置A制取二氧化碳的化学方程式。(2)、若用装置A制取氧气,请在图中方框内填写对应的药品。(3)、若用装置B干燥氢气,气体应从导管口通入。23. 下图为模拟炼铁原理的装置,请回答下列问题。 (1)、B装置玻璃管里可观察到什么现象?写出有关反应的化学方程式。(2)、为探究反应后A装置溶液中溶质成分,某同学设计了如下方案:取少量溶液,加入Ba(OH)2溶液,反应后静置,取上层清液滴加酚酞溶液。若溶液变红,溶质为Na2CO3和NaOH,请改正该方案中的不正确之处。24. 将锌粉加入到一定质量Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤,可以得到溶液和固体。(1)、若滤液呈蓝色,则滤渣中一定含有。(2)、写出一定发生的反应化学方程式。25. 酸、碱、盐是初中化学学习的重要内容,它们在生产、生活中有重要的用途。(1)、酸、碱的元素组成中都含有元素;检验某溶液是否呈酸性,可选用的一种试剂是。(2)、某实验小组用氢氧化钠溶液和稀盐酸探究中和反应,用pH计和温度传感器测定并绘制的图像如图所示。
(1)、B装置玻璃管里可观察到什么现象?写出有关反应的化学方程式。(2)、为探究反应后A装置溶液中溶质成分,某同学设计了如下方案:取少量溶液,加入Ba(OH)2溶液,反应后静置,取上层清液滴加酚酞溶液。若溶液变红,溶质为Na2CO3和NaOH,请改正该方案中的不正确之处。24. 将锌粉加入到一定质量Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤,可以得到溶液和固体。(1)、若滤液呈蓝色,则滤渣中一定含有。(2)、写出一定发生的反应化学方程式。25. 酸、碱、盐是初中化学学习的重要内容,它们在生产、生活中有重要的用途。(1)、酸、碱的元素组成中都含有元素;检验某溶液是否呈酸性,可选用的一种试剂是。(2)、某实验小组用氢氧化钠溶液和稀盐酸探究中和反应,用pH计和温度传感器测定并绘制的图像如图所示。
①写出该反应的化学方程式。
②B点对应的溶液中溶质的成分是;该反应属于(填“吸热”或“放热”)反应。
(3)、实验室为了除去粗食盐中所含有CaCl2、MgSO4杂质,设计了如下实验步骤:①将粗盐溶于水;②加入过量的Ba(OH)2溶液;③加入过量的Na2CO3溶液;④过滤;⑤向滤液中加入适量的盐酸;⑥蒸发结晶。加入Ba(OH)2溶液时所发生反应的化学方程式为;步骤③是为了除去溶液中的离子(写离子符号)。
(4)、若取100g溶质质量分数为11.7%的氯化钠溶液,加入足量的硝酸银溶液,充分反应后过滤,可得到氯化银的质量是多少?(写出计算过程,结果精确到0.1g)