广东省云浮市2021-2022学年高二下学期期末教学质量检测化学试题
试卷更新日期:2023-04-17 类型:期末考试
一、单选题
-
1. 在北京冬奥会上,我国使用了多项高科技。下列所使用的材料不属于有机高分子材料的是( )A、火炬“飞扬”使用的高性能树脂 B、御寒服面料使用的新疆长绒棉和驼绒 C、滑雪防护镜使用的聚甲基丙烯酸甲酯 D、颁奖礼仪服饰“瑞雪祥云”使用的保温材料石墨烯2. 中华文化博大精深,蕴含着许多化学知识。下列说法错误的是A、“蜡(主要成分为石蜡)炬成灰泪始干”,“泪”是蜡烛燃烧的产物 B、“强烧之,紫青烟起……云是真硝石也”,此现象涉及电子的跃迁 C、“春蚕到死丝方尽”中,“丝”的主要成分为蛋白质 D、“葡萄美酒夜光杯”中的“美酒”的酿制包含了淀粉的水解过程3. 人们的幸福是靠辛勒劳动创造出来的。下列化学知识解读错误的是
选项
劳动项目
化学知识解读
A
用食醋除去水壶中的水垢
水垢的主要成分——CaCO3是离子晶体
B
用铁锅炒菜
Fe的价层电子排布式为3d54s2
C
用热的碳酸钠溶液清洗油污
油污在碱性条件下水解可以生成丙三醇
D
用乙醇对公共场所杀菌消毒
利用了乙醇的强氧化性
A、A B、B C、C D、D4. 下列物质中,属于含有非极性共价键的分子晶体的是A、Si B、HCl C、N2 D、NH4Cl5. 某有机物M的结构简式如图,其中1、2、3号原子的杂化方式分别为 A、sp3、sp3、sp3 B、sp3、sp3、sp2 C、sp2、sp3、sp2 D、sp3、sp2、sp26. H2O的和H2O2的含有相同的元素,H2O2的分子空间结构如图所示,下列说法正确的是
A、sp3、sp3、sp3 B、sp3、sp3、sp2 C、sp2、sp3、sp2 D、sp3、sp2、sp26. H2O的和H2O2的含有相同的元素,H2O2的分子空间结构如图所示,下列说法正确的是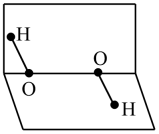 A、H2O2的是非极性分子 B、1molH2O2中含有2molσ键 C、H2O和H3O+的VSEPR模型不同 D、H2O分子之间存在氢键,因此H2O的沸点高于H2S的7. 下列实验方案正确的是A、可用分液漏斗分离甘油和水 B、可用蒸馏法分离正己烷(沸点为69℃)和正庚烷(沸点为98℃) C、可用溴水鉴别乙烯和乙炔 D、只用NaOH溶液可一次性鉴别乙醇、乙酸和乙酸乙酯8. KH2PO4晶体具有优异的非线性光学性能,超大KH2PO4晶体主要应用于大功率固体激光器。关于该物质涉及的元素,下列说法正确的是( )A、电负性:P>O>H B、离子半径大小:K+>P3->O2- C、基态K原子有19种不同运动状态的电子 D、基态P原子的价层电子轨道表示式:
A、H2O2的是非极性分子 B、1molH2O2中含有2molσ键 C、H2O和H3O+的VSEPR模型不同 D、H2O分子之间存在氢键,因此H2O的沸点高于H2S的7. 下列实验方案正确的是A、可用分液漏斗分离甘油和水 B、可用蒸馏法分离正己烷(沸点为69℃)和正庚烷(沸点为98℃) C、可用溴水鉴别乙烯和乙炔 D、只用NaOH溶液可一次性鉴别乙醇、乙酸和乙酸乙酯8. KH2PO4晶体具有优异的非线性光学性能,超大KH2PO4晶体主要应用于大功率固体激光器。关于该物质涉及的元素,下列说法正确的是( )A、电负性:P>O>H B、离子半径大小:K+>P3->O2- C、基态K原子有19种不同运动状态的电子 D、基态P原子的价层电子轨道表示式: 9. 下列有机物分子中属于手性分子的是A、甘氨酸(NH2CH2COOH) B、氯仿(CHCl3) C、乳酸[CH3CH(OH)COOH] D、丙醛(CH3CH2CHO)10. PC(聚碳酸酯)塑料以其独特的高透光率、高折射率、高抗冲性、尺寸稳定性及易加工成型、耐热等特点,被广泛应用在北京冬奥会滑雪运动员护目镜的镜片制作上。PC的结构如图所示,下列说法错误的是
9. 下列有机物分子中属于手性分子的是A、甘氨酸(NH2CH2COOH) B、氯仿(CHCl3) C、乳酸[CH3CH(OH)COOH] D、丙醛(CH3CH2CHO)10. PC(聚碳酸酯)塑料以其独特的高透光率、高折射率、高抗冲性、尺寸稳定性及易加工成型、耐热等特点,被广泛应用在北京冬奥会滑雪运动员护目镜的镜片制作上。PC的结构如图所示,下列说法错误的是 A、PC是纯净物 B、PC是一种缩聚产物 C、PC的一个链节中所有原子不可能共平面 D、PC可水解生成H2CO3和
A、PC是纯净物 B、PC是一种缩聚产物 C、PC的一个链节中所有原子不可能共平面 D、PC可水解生成H2CO3和 11. 下列各组中的反应原理相同的是A、乙醇与浓硫酸共热到140℃、170℃,均能脱去水分子 B、甲苯、乙烯均能使酸性KMnO4溶液褪色 C、向溴水中加入己烯或苯,充分振荡,溴水层均褪色 D、1-溴丙烷分别与KOH水溶液、KOH乙醇溶液共热12. 由徐光宪院士发起院士学子同创的《分子共和国》科普读物生动形象地戏说了BF3、NH3、H2S、O3、CH3COOH、SOCl2等众多“分子共和国”中的明星。下列说法正确的是A、键角:NH3<BF3 B、酸性:CH3COOH>CF3COOH C、SOCl2分子中只存在σ键,不存在π键 D、H2S、O3分子的空间结构均为直线形,且均为非极性分子13. 下列实验装置或操作能达到实验目的的是
11. 下列各组中的反应原理相同的是A、乙醇与浓硫酸共热到140℃、170℃,均能脱去水分子 B、甲苯、乙烯均能使酸性KMnO4溶液褪色 C、向溴水中加入己烯或苯,充分振荡,溴水层均褪色 D、1-溴丙烷分别与KOH水溶液、KOH乙醇溶液共热12. 由徐光宪院士发起院士学子同创的《分子共和国》科普读物生动形象地戏说了BF3、NH3、H2S、O3、CH3COOH、SOCl2等众多“分子共和国”中的明星。下列说法正确的是A、键角:NH3<BF3 B、酸性:CH3COOH>CF3COOH C、SOCl2分子中只存在σ键,不存在π键 D、H2S、O3分子的空间结构均为直线形,且均为非极性分子13. 下列实验装置或操作能达到实验目的的是选项
A
B
C
D
实验装置或操作




实验目的
证明乙炔可使溴水褪色
配制银氨溶液
验证苯与液溴发生取代反应
检验蔗糖的水解产物具有还原性
A、A B、B C、C D、D14. 某有机物M的结构简式为CH3CH(OH)CH2COOH,下列有机物经过一定条件不可以一步生成M的是A、CH3CH=CHCOOH B、CH3CH2CHBrCOOH C、CH3CH(OH)CH2COOCH2CH3 D、 15. 我国科学家在FeS2表面自组装单原子层Cu5纳米团簇构筑双催化剂实现H2O2到·OH的稳定持续活化。FeS2的晶胞结构如图所示。已知:晶胞参数为a pm。下列说法错误的是
15. 我国科学家在FeS2表面自组装单原子层Cu5纳米团簇构筑双催化剂实现H2O2到·OH的稳定持续活化。FeS2的晶胞结构如图所示。已知:晶胞参数为a pm。下列说法错误的是 A、每个晶胞中含有4个Fe2+ B、H2O2和FeS2中都含有非极性键 C、和之间的最短距离为a pm D、Fe2+位于形成的正八面体空隙中16. 有机合成反应需要考虑“原子经济性”,也应尽可能选择反应条件温和、产率高的反应。已知RCHO+R′CH2CHO
A、每个晶胞中含有4个Fe2+ B、H2O2和FeS2中都含有非极性键 C、和之间的最短距离为a pm D、Fe2+位于形成的正八面体空隙中16. 有机合成反应需要考虑“原子经济性”,也应尽可能选择反应条件温和、产率高的反应。已知RCHO+R′CH2CHO 为加成反应。用乙烯制备
为加成反应。用乙烯制备 时,按正确的合成路线依次发生反应的反应类型为 A、加成→氧化→加成 B、加成→氧化→取代 C、加成→氧化→消去 D、加成→加成→氧化
时,按正确的合成路线依次发生反应的反应类型为 A、加成→氧化→加成 B、加成→氧化→取代 C、加成→氧化→消去 D、加成→加成→氧化二、非选择题
-
17. 已知X、Y、Z、M、N是原子序数依次增大的前四周期元素,其中Y是地壳中含量第二的元素,X、Y、Z是核外未成对电子数均为2的非金属元素,ZX3的空间结构为平面三角形,M的价层电子数为6,N与Z同族。请回答下列问题:(1)、X为(填元素名称,下同),Y为 , Z为。(2)、M在元素周期表的位置是 , 基态N原子的价层电子排布式为。(3)、X、Y、Z的第一电离能由大到小的顺序为(填元素符号)。(4)、Z与N的最简单氢化物的稳定性比较: (写化学式),原因为。(5)、YX2的晶体类型为 , 其熔点(填“高于”或“低于”)NX2。18. 湖南省成矿地质条件优越,矿产资源丰富,优质矿产多且分布相对集中,在国内外享有盛誉。在已探明储量的矿种中,钒、锰、锌、锡、磷、硫等的含量在全国均位于前列。
请回答下列问题:
(1)、基态V原子的价层电子轨道表示式为。(2)、锡与氯、溴、碘可以形成四卤化物。熔沸点数据如表所示:SnCl4
SnBr4
SnI4
熔点/℃
-33
31
144.5
沸点/℃
114.1
202
364
SnCl4、SnBr4、SnI4的熔沸点逐渐升高的原因是。
(3)、二麦芽酚锌是锌的一种配位化合物,其结构如图所示。配位化合物中的中心原子配位数是指和中心原子直接成键的原子的数目。二麦芽酚锌中锌的配位数为 , 其中非金属元素的电负性由大到小的顺序是(填元素符号),其中碳原子的杂化类型为。 (4)、MnS的晶胞结构如图所示。
(4)、MnS的晶胞结构如图所示。
①离中心S2-最近且等距离的Mn2+有个,所围成的空间结构为。
②已知NA代表阿伏加德罗常数的值,晶胞参数为apm,则MnS晶胞的密度为(用含NA、a的代数式表示)g•cm-3。
19. 苯乙酮既可用于制香皂和香烟,又可用作纤维素脂和树脂等的溶剂。实验室以苯和乙酸酐为原料制备苯乙酮: , 制备过程中还有CH3COOH+AlCl3→CH3COOAlCl2+HCl↑等副反应发生,实验装置图和相关物质的沸点如表:
, 制备过程中还有CH3COOH+AlCl3→CH3COOAlCl2+HCl↑等副反应发生,实验装置图和相关物质的沸点如表:
物质
苯
苯乙酮
乙酸
乙酸酐
相对分子质量
78
120
60
102
沸点/℃
80.1
202
117.9
139.8
实验步骤如下:
步骤1:苯和适量无水乙酸酐由滴液漏斗滴加,在三颈烧瓶中将30mL(约0.337mol)苯和无水AlCl3粉末充分混合后,再缓慢滴加6mL(约0.064mol)乙酸酐。乙酸酐滴加完后,升温至70~80℃,保温反应一段时间,冷却。
步骤2:冷却后将反应物倒入含盐酸的冰水中,然后分出苯层。苯层依次用水、5%NaOH溶液和水洗涤。
步骤3:向洗涤后的有机相中加入适量无水MgSO4固体,放置一段时间后进行分离。
步骤4:将步骤3中得到的有机相进行蒸馏,经称正得到约5.8g苯乙酮。
回答下列问题:
(1)、仪器a中支管的作用是 , 步骤1中适宜的加热方式为。(2)、干燥管中氯化钙的作用是。(3)、写出步骤2中用NaOH溶液洗涤时除去酸性物质的化学方程式:。(4)、步骤3中分离时用到的玻璃仪器有。(5)、经计算,该反应的产率约为(保留三位有效数字)。20. 有机物物是重要的医药合成中间体,其一种合成路线如图:
已知:
①

 ;
;②I为芳香烃,且同温同压下I对H2的相对密度为46。
回答下列问题:
(1)、I的分子式为 , II的名称为 , II→IV的反应类型为。(2)、IV的结构简式为 , 含有的官能团名称为。(3)、VI→VIII的化学方程式为。(4)、IV有多种同分异构体,同时能满足下列条件的同分异构体有种(不考虑立体异构)。①能发生银镜反应和水解反应
②苯环上有3个取代基
写出其中一种核磁共振氢谱有4组峰且峰面积比为6:2:1:1的结构简式:。
(5)、参照上述合成路线,以甲苯 和为原料合成
和为原料合成 的路线(无机试剂任选)。
的路线(无机试剂任选)。