广西南宁市经济技术开发区2023年中考一模化学试题
试卷更新日期:2023-04-17 类型:中考模拟
一、单选题
-
1. 下列我国古代的发明或技术中,主要原理涉及化学变化的是( )A、水车灌溉 B、烧制陶瓷 C、雕版印刷 D、雕刻石像2. 下列图标,在加油站必须张贴的是( )A、
 B、
B、 C、
C、 D、
D、 3. 下列物质能用作钾肥的是( )A、NH4HCO3 B、K2SO4 C、CaSO4 D、Na3PO44. 下列有关实验基本操作,正确的是( )A、取用固体
3. 下列物质能用作钾肥的是( )A、NH4HCO3 B、K2SO4 C、CaSO4 D、Na3PO44. 下列有关实验基本操作,正确的是( )A、取用固体 B、检查气密性
B、检查气密性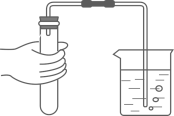 C、过滤
C、过滤 D、测盐酸的pH
D、测盐酸的pH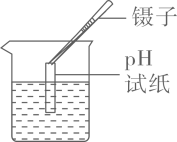 5. 下列气体排放到空气中容易引起酸雨的是( )A、SO2 B、CO2 C、N2 D、CO6. 下列物质的类别属于盐的是( )A、水银 B、干冰 C、醋酸 D、高锰酸钾7. 下列实验现象描述错误的是( )A、一氧化碳在空气中燃烧发出蓝色火焰 B、细铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 C、红磷在空气中燃烧,发出红色的火焰,产生大量白雾 D、木炭在空气中充分燃烧,生成能使澄清石灰水变浑浊的气体8. 月球表面富含钛铁矿,其主要成分是钛酸亚铁(FeTiO3),其中钛元素的化合价为( )A、+1 B、+2 C、+3 D、+49. 下列物质放入水中,能形成溶液的是( )A、蔗糖 B、植物油 C、泥土 D、面粉10. 下列物质的俗名和化学式,对应关系正确的是( )A、干冰H2O B、纯碱NaHCO3 C、烧碱NaOH D、熟石灰CaCO311. 下列有关能源与环境的说法错误的是( )A、积极植树造林,促进达成“碳中和” B、废旧电池回收利用能减少对土壤的污染 C、加高烟囱排放含PM 2.5的烟尘以减少空气污染 D、城市推广使用氢燃料电池客车可减少温室气体排放12. 连花清瘟胶囊可治疗感冒,含有连翘、金银花等十几种中药成分,其中连翘的主要成分之一为连翘苷(化学式为C27H34O11)。下列有关连翘苷的说法正确的是( )A、连翘苷中氢元素的质量分数最大 B、连翘苷由C,H,O三种元素组成 C、连翘苷中氢元素和氧元素的质量比为34:11 D、连翘苷由27个碳原子、34个氢原子和11个氧原子构成13. 把X、Y、Z三种金属分别加入稀盐酸中,Y表面有气泡产生,X、Z无明显变化;再把X放到Z的硝酸盐溶液中,X的表面有固体析出,则三种金属的活动性顺序是( )A、Y>X>Z B、Y>Z>X C、X>Z>Y D、Z>X>Y14. 下列物质存放在烧杯中一段时间后,因发生化学变化使溶液质量变大的是( )A、浓盐酸 B、石灰水 C、浓硫酸 D、烧碱溶液15. a、b、c三种固体物质(不含结晶水)的溶解度曲线如下图所示。下列说法正确的是( )
5. 下列气体排放到空气中容易引起酸雨的是( )A、SO2 B、CO2 C、N2 D、CO6. 下列物质的类别属于盐的是( )A、水银 B、干冰 C、醋酸 D、高锰酸钾7. 下列实验现象描述错误的是( )A、一氧化碳在空气中燃烧发出蓝色火焰 B、细铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 C、红磷在空气中燃烧,发出红色的火焰,产生大量白雾 D、木炭在空气中充分燃烧,生成能使澄清石灰水变浑浊的气体8. 月球表面富含钛铁矿,其主要成分是钛酸亚铁(FeTiO3),其中钛元素的化合价为( )A、+1 B、+2 C、+3 D、+49. 下列物质放入水中,能形成溶液的是( )A、蔗糖 B、植物油 C、泥土 D、面粉10. 下列物质的俗名和化学式,对应关系正确的是( )A、干冰H2O B、纯碱NaHCO3 C、烧碱NaOH D、熟石灰CaCO311. 下列有关能源与环境的说法错误的是( )A、积极植树造林,促进达成“碳中和” B、废旧电池回收利用能减少对土壤的污染 C、加高烟囱排放含PM 2.5的烟尘以减少空气污染 D、城市推广使用氢燃料电池客车可减少温室气体排放12. 连花清瘟胶囊可治疗感冒,含有连翘、金银花等十几种中药成分,其中连翘的主要成分之一为连翘苷(化学式为C27H34O11)。下列有关连翘苷的说法正确的是( )A、连翘苷中氢元素的质量分数最大 B、连翘苷由C,H,O三种元素组成 C、连翘苷中氢元素和氧元素的质量比为34:11 D、连翘苷由27个碳原子、34个氢原子和11个氧原子构成13. 把X、Y、Z三种金属分别加入稀盐酸中,Y表面有气泡产生,X、Z无明显变化;再把X放到Z的硝酸盐溶液中,X的表面有固体析出,则三种金属的活动性顺序是( )A、Y>X>Z B、Y>Z>X C、X>Z>Y D、Z>X>Y14. 下列物质存放在烧杯中一段时间后,因发生化学变化使溶液质量变大的是( )A、浓盐酸 B、石灰水 C、浓硫酸 D、烧碱溶液15. a、b、c三种固体物质(不含结晶水)的溶解度曲线如下图所示。下列说法正确的是( ) A、a、b、c三种物质溶解度的大小:a>b>c B、当a中混有少量b时,可以用蒸发结晶的方法提纯a C、t2℃时,将100ga的饱和溶液降温至t1℃,会有30g的晶体析出 D、t2℃时,分别配制等质量的a、b、c的饱和溶液,所需溶剂的质量大小:a<b<c16. 下列物质之间的转化,不能通过一步反应实现的是( )A、O2→CO→CO2→H2O B、Cu→CuO→CuSO4→CuCl2 C、KCl→KNO3→K2SO4→KOH D、CaO→Ca (OH)2→CaCl2→CaCO317. 下列各组离子在pH=11的无色溶液中,能大量共存的是( )A、Fe2+、Cl-、Na+ B、Ba2+、Na+、 C、K+、H+、 D、Mg2+、Ca2+、18. 将含有CH4和H2的混合气体6g完全燃烧,把产生的气体通入足量的澄清石灰水中,得到20g白色沉淀。则原混合气体中CH4的质量为( )A、1.6g B、2g C、3.2g D、3.6g19. 逻辑推理是一种重要的化学思维方法。下列推理正确的是( )A、H2O和H2O2的组成元素相同,所以它们的化学性质相同 B、碱溶液能使无色酚酞试液变红,则能使无色酚酞试液变红的一定是碱溶液 C、元素的种类是由质子数决定的,则质子数相同的原子一定属于同种元素 D、催化剂在反应前后质量保持不变,则反应前后质量不变的物质一定是催化剂20. 下列实验设计不能达到实验目的的是( )A、验证样品中含有碳酸盐
A、a、b、c三种物质溶解度的大小:a>b>c B、当a中混有少量b时,可以用蒸发结晶的方法提纯a C、t2℃时,将100ga的饱和溶液降温至t1℃,会有30g的晶体析出 D、t2℃时,分别配制等质量的a、b、c的饱和溶液,所需溶剂的质量大小:a<b<c16. 下列物质之间的转化,不能通过一步反应实现的是( )A、O2→CO→CO2→H2O B、Cu→CuO→CuSO4→CuCl2 C、KCl→KNO3→K2SO4→KOH D、CaO→Ca (OH)2→CaCl2→CaCO317. 下列各组离子在pH=11的无色溶液中,能大量共存的是( )A、Fe2+、Cl-、Na+ B、Ba2+、Na+、 C、K+、H+、 D、Mg2+、Ca2+、18. 将含有CH4和H2的混合气体6g完全燃烧,把产生的气体通入足量的澄清石灰水中,得到20g白色沉淀。则原混合气体中CH4的质量为( )A、1.6g B、2g C、3.2g D、3.6g19. 逻辑推理是一种重要的化学思维方法。下列推理正确的是( )A、H2O和H2O2的组成元素相同,所以它们的化学性质相同 B、碱溶液能使无色酚酞试液变红,则能使无色酚酞试液变红的一定是碱溶液 C、元素的种类是由质子数决定的,则质子数相同的原子一定属于同种元素 D、催化剂在反应前后质量保持不变,则反应前后质量不变的物质一定是催化剂20. 下列实验设计不能达到实验目的的是( )A、验证样品中含有碳酸盐 B、证明燃烧所需的两个条件
B、证明燃烧所需的两个条件 C、验证质量守恒定律
C、验证质量守恒定律 D、测定空气中氧气的含量
D、测定空气中氧气的含量
二、填空题
-
21. 从C、H、O、Na、Cl五种元素中选择合适的元素组成,用化学符号填空:(1)、金刚石。(2)、最简单的有机物。(3)、汽水中含有的酸。(4)、配制生理盐水的溶质。(5)、能与血红蛋白结合引起中毒的物质。22. 广西简称“桂”,又称“八桂”,据说这跟广西“桂树成林”有关系。桂花是中国十大名花之一,桂花可制作桂花糕或制作桂花茶,深受人们喜爱。
 (1)、桂花适宜生长在pH为5.5一6.5的土壤中,对于pH为5.5以下的土壤,要种植桂花,可施加对土壤进行改良。(2)、桂花糕味道清香淡雅,其主要成分有糯米粉、面粉、糖、桂花,其中面粉中富含营养素是。(3)、用杂质少的山泉水泡桂花茶,能充分体现茶的色、香、味。生活中可用鉴别山泉水是硬水还是软水。(4)、泡茶时可用茶漏将茶花和水分离,该做法与实验室的操作原理相似;桂花茶泡出的茶汤花香沁人,从微观角度解释,这是因为。23. 化学就在我们身边。(1)、苹果中富含多种物质和维生素,是人们喜爱食用的水果之一。人体缺乏维生素C会引起。(2)、洗碗时加入洗洁精除去油污,这是利用了洗洁精的作用。(3)、饮食过量,胃酸会大量分泌,以致消化不良。为缓减该症状,可服用含有碳酸氢钠的药物治疗,该反应的化学方程式 , 反应的基本类型为。24. 下图是二氧化氯气体和物质氰化氢(HCN)反应的微观示意图。
(1)、桂花适宜生长在pH为5.5一6.5的土壤中,对于pH为5.5以下的土壤,要种植桂花,可施加对土壤进行改良。(2)、桂花糕味道清香淡雅,其主要成分有糯米粉、面粉、糖、桂花,其中面粉中富含营养素是。(3)、用杂质少的山泉水泡桂花茶,能充分体现茶的色、香、味。生活中可用鉴别山泉水是硬水还是软水。(4)、泡茶时可用茶漏将茶花和水分离,该做法与实验室的操作原理相似;桂花茶泡出的茶汤花香沁人,从微观角度解释,这是因为。23. 化学就在我们身边。(1)、苹果中富含多种物质和维生素,是人们喜爱食用的水果之一。人体缺乏维生素C会引起。(2)、洗碗时加入洗洁精除去油污,这是利用了洗洁精的作用。(3)、饮食过量,胃酸会大量分泌,以致消化不良。为缓减该症状,可服用含有碳酸氢钠的药物治疗,该反应的化学方程式 , 反应的基本类型为。24. 下图是二氧化氯气体和物质氰化氢(HCN)反应的微观示意图。 (1)、氰化氢(HCN)含有种元素。(2)、上图所示的反应前后,一定不变的是(用序号填空)。
(1)、氰化氢(HCN)含有种元素。(2)、上图所示的反应前后,一定不变的是(用序号填空)。①原子种类 ②分子种类 ③原子数目 ④原子质量 ⑤元素化合价 ⑥元素种类
(3)、反应前后涉及的物质中,属于氧化物的是(填化学式)。(4)、该反应的化学方程式是。25. 图一是元素周期表中的一部分,图二是三种原子的结构示意图。请回答有关问题: (1)、15号元素属于(选填“金属”或“非金属”)元素,18号元素的相对原子质量是。(2)、Na、Mg、Cl三种原子中,易得到电子的是 , 形成的离子符号是。(3)、钠元素和氟元素组成的化合物的化学式是。(4)、Na、Mg、Cl三种原子在周期表中都排在同一周期,原因是。26. 2022年4月16日,我国“神舟十三号”载人飞船圆满完成长达半年之久的任务,为中国空间站正式建成打下坚实基础。请回答以下问题。(1)、出舱任务。舱外航天服使用的聚氨酯橡胶属于(填“合成”或“金属”)材料,舱外的太阳能电池板是由镍钛合金制成,在低温下被折叠,进入太空运行轨道后,在阳光照射下可自然展开,恢复成原状。以上说明镍钛合金具有良好的(填“导热性”或“延展性”或“抗氧化性”)。(2)、舱内生活。中国空间站废气处理系统保障着宇航员的生命。第一步利用活性炭的性,让呼吸产生的废气进入一个装有活性炭的滤网除去臭气;第二步,再利用含有氢氧化锂(LiOH)的过滤网除去航天员呼出的二氧化碳,生成碳酸锂和水,该反应的化学方程式为。(3)、天宫课堂。航天员介绍,他们呼吸用的氧气是电解水得到的,电解水产生氢气的电极应接在电源的(填“正”或“负”)极。
(1)、15号元素属于(选填“金属”或“非金属”)元素,18号元素的相对原子质量是。(2)、Na、Mg、Cl三种原子中,易得到电子的是 , 形成的离子符号是。(3)、钠元素和氟元素组成的化合物的化学式是。(4)、Na、Mg、Cl三种原子在周期表中都排在同一周期,原因是。26. 2022年4月16日,我国“神舟十三号”载人飞船圆满完成长达半年之久的任务,为中国空间站正式建成打下坚实基础。请回答以下问题。(1)、出舱任务。舱外航天服使用的聚氨酯橡胶属于(填“合成”或“金属”)材料,舱外的太阳能电池板是由镍钛合金制成,在低温下被折叠,进入太空运行轨道后,在阳光照射下可自然展开,恢复成原状。以上说明镍钛合金具有良好的(填“导热性”或“延展性”或“抗氧化性”)。(2)、舱内生活。中国空间站废气处理系统保障着宇航员的生命。第一步利用活性炭的性,让呼吸产生的废气进入一个装有活性炭的滤网除去臭气;第二步,再利用含有氢氧化锂(LiOH)的过滤网除去航天员呼出的二氧化碳,生成碳酸锂和水,该反应的化学方程式为。(3)、天宫课堂。航天员介绍,他们呼吸用的氧气是电解水得到的,电解水产生氢气的电极应接在电源的(填“正”或“负”)极。三、综合题
-
27. 我国制碱工业的先驱一一侯德榜先生发明了“侯氏制碱法”,提高了食盐利用率,降低了纯碱的成本,为世界制碱技术谱写了新的篇章。“侯氏制碱法”的主要原理是以氯化钠、二氧化碳、氨气(NH3)为原料制备碳酸钠,其主要流程如图:

回答下列问题:
(1)、溶解池中用搅拌器搅拌的目的是。(2)、分离器中分离出NaHCO3固体的实验基本操作名称是。(3)、煅烧炉中发生反应的化学方程式为。(4)、为提高生产效率,在炭化塔中应综合考虑该生产的条件是(填字母序号)。a.高温 b.低温 c.常温 d.高压 e.低压 f.常压
(5)、为了使碳化塔中的反应能顺利进行,工业生产过程中是先通入氨气,形成氨的氯化钠饱和溶液之后,再通入二氧化碳气体的。这样做的原因是。28. 下图是实验室制取气体的装置图,请回答下列问题: (1)、仪器①的名称是。(2)、实验室制取二氧化碳可选用的发生装置和收集装置是(填字母序号)。(3)、用B装置制备氧气的化学方程式是。(4)、用E装置收集氧气,不纯的原因可能有(写一点即可)。(5)、可用向下排空气法收集氢气的原因是。(6)、若用F装置收集氢气,请将集气瓶内的导管补画完整。(7)、如图G向烧杯中倒入二氧化碳,观察到的实验现象为。29. 钢铁是现代工业的筋骨,保护金属资源,防止金属腐蚀已成为科学研究和技术领域中的重大问题。科技小组以“铁锈蚀”为主题开展如下项目式学习。(1)、【任务一】探究铁锈蚀的条件
(1)、仪器①的名称是。(2)、实验室制取二氧化碳可选用的发生装置和收集装置是(填字母序号)。(3)、用B装置制备氧气的化学方程式是。(4)、用E装置收集氧气,不纯的原因可能有(写一点即可)。(5)、可用向下排空气法收集氢气的原因是。(6)、若用F装置收集氢气,请将集气瓶内的导管补画完整。(7)、如图G向烧杯中倒入二氧化碳,观察到的实验现象为。29. 钢铁是现代工业的筋骨,保护金属资源,防止金属腐蚀已成为科学研究和技术领域中的重大问题。科技小组以“铁锈蚀”为主题开展如下项目式学习。(1)、【任务一】探究铁锈蚀的条件取三枚相同的洁净无锈铁钉分别放入试管,进行图1实验,一周后观察实验现象。



对比A、B、C试管中实验现象,说明铁锈蚀主要是铁与空气中的发生化学反应。
(2)、铁锈蚀后应及时除锈的原因是。(3)、【任务二】探究影响铁锈蚀的因素小组设计了图2装置,检查气密性,将5g铁粉和2g碳粉加入三颈烧瓶,连接压强传感器、数据采集器,采集数据,绘制出压强随时间变化的曲线如图3。T1时刻利用注射器加入2mL饱和NaCl溶液,再将一只装有稀盐酸的注射器插到烧瓶上。
据图3,对比AB段和BC段说明 , t3时刻压强突然变大的原因是。
(4)、【任务三】探究盐酸除锈向试管A中(含生锈铁钉)加入过量稀盐酸,浸泡。可观察到铁锈逐渐消失,铁钉表面有气泡产生,溶液呈黄色,一段时间后溶液由黄色逐渐变为浅绿色,得到溶液A。
铁锈消失是因为Fe2O3与盐酸发生了反应,该反应的化学方程式为;溶液A中一定含有的溶质是。
(5)、【分析总结】为防止铁制品锈蚀,应保持铁制品表面。
四、计算题
-
30. 甲、乙、丙三位同学对氯化镁样品(仅含氯化钠杂质)进行如下检测:各取5.0g样品溶于一定量的水中得到25.0g溶液,再分别加入不同质量,溶质质量分数为10%的氢氧化钠溶液,反应得到沉淀的实验数据如下表
甲
乙
丙
加入氢氧化钠溶液质量(g)
35.0
40.0
45.0
反应得到沉淀的质量(g)
2.5
2.9
2.9
试回答下列问题:
(1)、上述实验中,同学所用的氢氧化钠溶液一定过量。(2)、求样品中氯化镁的质量分数(写出计算过程,结果精确到0.1%,下同)