山东省潍坊市2023年高三下学期学科核心素养测评化学试题
试卷更新日期:2023-04-13 类型:高考模拟
一、单选题
-
1. 化学与社会、生产、生活密切相关。下列说法错误的是A、久置的红薯变甜,是因为葡萄糖发生了水解 B、电热水器用镁棒防止金属内胆腐蚀,原理是牺牲阳极保护法 C、第五形态的碳单质“碳纳米泡沫”,与石墨烯互为同素异形体 D、用太阳能光催化分解水代替电解水制氢气有利于节能环保2. 下列物质应用错误的是A、溶液用作水果的保鲜剂 B、苯甲酸及其钠盐用作食品防腐剂 C、用作生活用水的消毒剂 D、用热NaOH溶液洗去铁表面沾有的柴油3. 下列实验装置或操作正确的是
 A、用图1装置测定中和反应的反应热 B、用图2装置测定化学反应速率 C、用图3装置分离乙醚和苯 D、用图4装置振荡萃取、静置分层后,打开分液漏斗上方的玻璃塞再进行分液4. 是阿伏加德罗常数的值。下列说法正确的是A、1mol 中含有Si-O键的数目为2 B、25℃、101kPa下,4g 中含有的原子数为2 C、标准状况下,6.72L 与水充分反应转移的电子数目为0.1 D、25℃时,1.0L 的溶液中含有的数目为0.25. 某种天然沸石的化学式为 , 其中元素X、Y、Z、R、W原子序数依次增大,且占据四个不同周期。Y在地壳中含量最高,在该化合物中R显示其最高价态,基态W原子的核外电子恰好填满10个原子轨道。下列说法错误的是A、简单离子半径: B、第一电离能: C、最简单氢化物稳定性: D、氯化物熔点:6. 下列实验操作能达到实验目的的是A、向溶液中加入硝酸酸化的氯化钡溶液,检验溶液中的 B、向沸水中逐滴加入饱和氯化铁溶液并继续加热搅拌制备氢氧化铁胶体 C、除去NaCl固体中的少量 , 将固体溶解后蒸发结晶、趁热过滤、洗涤干燥 D、将固体溶解于盛有适量蒸馏水的烧杯中,经转移、洗涤、定容和摇匀,配制一定浓度的溶液7. 7-ACCA是合成头孢克罗的关键中间体,其结构如图所示。下列说法正确的是
A、用图1装置测定中和反应的反应热 B、用图2装置测定化学反应速率 C、用图3装置分离乙醚和苯 D、用图4装置振荡萃取、静置分层后,打开分液漏斗上方的玻璃塞再进行分液4. 是阿伏加德罗常数的值。下列说法正确的是A、1mol 中含有Si-O键的数目为2 B、25℃、101kPa下,4g 中含有的原子数为2 C、标准状况下,6.72L 与水充分反应转移的电子数目为0.1 D、25℃时,1.0L 的溶液中含有的数目为0.25. 某种天然沸石的化学式为 , 其中元素X、Y、Z、R、W原子序数依次增大,且占据四个不同周期。Y在地壳中含量最高,在该化合物中R显示其最高价态,基态W原子的核外电子恰好填满10个原子轨道。下列说法错误的是A、简单离子半径: B、第一电离能: C、最简单氢化物稳定性: D、氯化物熔点:6. 下列实验操作能达到实验目的的是A、向溶液中加入硝酸酸化的氯化钡溶液,检验溶液中的 B、向沸水中逐滴加入饱和氯化铁溶液并继续加热搅拌制备氢氧化铁胶体 C、除去NaCl固体中的少量 , 将固体溶解后蒸发结晶、趁热过滤、洗涤干燥 D、将固体溶解于盛有适量蒸馏水的烧杯中,经转移、洗涤、定容和摇匀,配制一定浓度的溶液7. 7-ACCA是合成头孢克罗的关键中间体,其结构如图所示。下列说法正确的是 A、该化合物的化学式为 B、分子中有5种不同化学环境的氢原子 C、分子中含有3个手性碳原子 D、不存在分子中含有苯环的同分异构体8. pH计的工作原理(如图所示)是通过测定电池电动势E(即玻璃电极和参比电极的电势差)而确定待测溶液的pH。电池电动势E与待测溶液pH关系为: (E的单位为V,K为常数)。下列说法错误的是
A、该化合物的化学式为 B、分子中有5种不同化学环境的氢原子 C、分子中含有3个手性碳原子 D、不存在分子中含有苯环的同分异构体8. pH计的工作原理(如图所示)是通过测定电池电动势E(即玻璃电极和参比电极的电势差)而确定待测溶液的pH。电池电动势E与待测溶液pH关系为: (E的单位为V,K为常数)。下列说法错误的是 A、计工作时,化学能转化为电能 B、玻璃电极玻璃膜内外的差异会引起电池电动势的变化 C、若玻璃电极电势比参比电极低,玻璃电极反应: D、若测得的标准溶液电池电动势E为 , 可标定常数9. 实验室初步分离苯甲酸乙酯、苯甲酸和环己烷的流程如下:
A、计工作时,化学能转化为电能 B、玻璃电极玻璃膜内外的差异会引起电池电动势的变化 C、若玻璃电极电势比参比电极低,玻璃电极反应: D、若测得的标准溶液电池电动势E为 , 可标定常数9. 实验室初步分离苯甲酸乙酯、苯甲酸和环己烷的流程如下:
已知:苯甲酸乙酯的沸点为212.6℃,“乙醚-环己烷-水共沸物”的沸点为62.1℃。下列说法错误的是
A、操作a和操作b不同 B、操作c为重结晶 C、无水和饱和碳酸钠溶液的作用相同 D、由该流程可以说明苯甲酸和苯甲酸钠在水中的溶解度差别很大10. 《环境科学》刊发了我国科研部门采用零价铁活化过硫酸钠( , 其中S为+6价)去除废水中正五价砷As(V)的研究成果,其反应机理模型如图所示。下列说法错误的是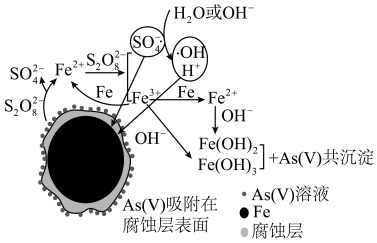 A、反应过程中有非极性键的断裂 B、溶液的pH越小,越有利于去除废水中的正五价砷 C、碱性条件下,硫酸根自由基发生的反应方程式为 D、反应过程中,存在反应11. 根据下列实验目的、操作及现象所得结论错误的是
A、反应过程中有非极性键的断裂 B、溶液的pH越小,越有利于去除废水中的正五价砷 C、碱性条件下,硫酸根自由基发生的反应方程式为 D、反应过程中,存在反应11. 根据下列实验目的、操作及现象所得结论错误的是选项
实验目的
操作及现象
结论
A
验证溶液中存在的水解平衡
向含有酚酞的溶液中加入少量固体,有白色沉淀生成,溶液红色变浅
溶液中存在水解平衡:
B
比较元素的非金属性强弱
向盛有小苏打固体的大试管中加入稀硫酸,有气体生成;将生成的气体通入溶液中,溶液变浑浊
非金属性:
C
检验实验室制得的乙烯中是否有
将生成的气体通入品红溶液中,溶液褪色
有生成
D
比较和的
向盛有溶液的试管中加入足量0.01 溶液,滤出沉淀后,向滤液中加入1 溶液,有白色沉淀生成
A、A B、B C、C D、D12. 我国科学家设计如下图所示“电子转移链”过程,实现了低温条件下氧化高效制。
下列说法错误的是
A、反应Ⅰ为取代反应 B、水解可制取 C、参加反应的 和的物质的量之比为2:1
D、1mol
和的物质的量之比为2:1
D、1mol  最多能与4mol 发生反应
最多能与4mol 发生反应
二、多选题
-
13. 锰及其化合物用途广泛,以菱锰矿(主要成分为 , 还含有铁、镍、钴的碳酸盐以及杂质)为原料生产金属锰和高品位的工艺流程如图所示:
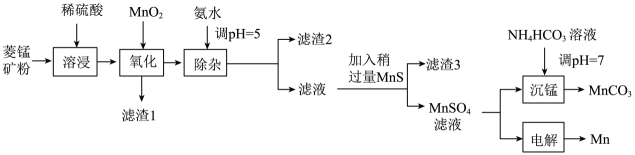
已知25℃时,部分物质的溶度积常数如表所示:
物质
MnS
NiS
CoS
说明:整个流程中Co、Ni均为+2价。下列说法正确的是
A、“氧化”时的主要作用是氧化 B、“滤渣3”的成分为CoS、NiS C、“沉锰”时,为了增强沉淀效果,应将溶液滴加到溶液中 D、“电解”时,以Fe作电极,、溶液为电解液、阳极产物为 , 每生成1mol 转移电子数为614. 我国科学家研究出一种钠离子可充电电池的工作示意图如下,该电池主要依靠钠离子在两极之间移动来工作,工作原理示意图如下:
其中代表没参与反应的-COONa,代表没参与反应的-ONa.下列有关说法错误的是
A、放电时,b极为正极 B、充电时,钠离子由b极向a极移动 C、充电时,阴极发生反应为 D、若电池充满电时a、b两极室质量相等,则放电过程中转移0.3mol电子时,两极质量差为6.9g
15. AgCl()和(砖红色)都是难溶电解质,以对pCl和作图的沉淀平衡曲线如图所示。下列说法正确的是
D、若电池充满电时a、b两极室质量相等,则放电过程中转移0.3mol电子时,两极质量差为6.9g
15. AgCl()和(砖红色)都是难溶电解质,以对pCl和作图的沉淀平衡曲线如图所示。下列说法正确的是 A、阴影区域AgCl和都沉淀 B、 C、向含有AgCl(s)的1.0 KCl溶液中加入 , 白色固体逐渐变为砖红色 D、用硝酸银标准液滴定溶液中的 , 作指示剂的浓度在0.01左右时滴定误差较小
A、阴影区域AgCl和都沉淀 B、 C、向含有AgCl(s)的1.0 KCl溶液中加入 , 白色固体逐渐变为砖红色 D、用硝酸银标准液滴定溶液中的 , 作指示剂的浓度在0.01左右时滴定误差较小三、非选择题
-
16. 有机—无机复合钙钛矿()型材料在太阳能电池及发光二极管等方面具有很好的应用前景,一种复合材料和(立方晶系)的晶胞结构如图所示。

已知:A为间隔的阳离子,例如、等;A'为单一组分钙钛阳离子,例如、、等;B为单一组分钙钛矿中心离子、等,X为单一组分钙钛矿的阴离子,例如、或等卤素离子。
回答下列问题:
(1)、基态Ti原子的价电子排布式为。(2)、H、C、N、O四种元素电负性由大到小的顺序为;第一电离能、、由大到小的顺序为。(3)、中C的杂化方式为;正丁胺()的沸点为77.8℃,正丁醇()的沸点为117.6℃,正丁胺沸点低的原因是。(4)、中Ca的配位数为;A为 , A'为 , B为 , X为 , 晶胞参数为a nm和c nm,该晶体的密度为。17. 三氯化六氨合钴是合成其它一些Co(Ⅲ)配合物的原料,其在水中的溶解度随着温度的升高而增大。实验室用晶体制备的实验步骤如下:i.在锥形瓶中,将溶于水中,加热至沸,加入研细的晶体,溶解得到混合溶液;
ii.将上述混合液倒入三颈烧瓶中,加入活性炭。冷却,利用如图装置先加入浓氨水,再逐滴加入5% 溶液,水浴加热至50~60℃,保持20min;

iii.然后用冰浴冷却至0℃左右,吸滤,把沉淀溶于50mL沸水中,经操作X后,慢慢加入浓盐酸于滤液中,即有大量橙黄色晶体( , )析出;
iv.用冰浴冷却后吸滤,晶体以冷的盐酸洗涤,再用少许乙醇洗涤,吸干。回答下列问题:
(1)、步骤i中,研细晶体所用的仪器名称为 , 无水的作用是。(2)、写出制备三氯化六氨合钴的化学方程式。(3)、步骤i中操作X为。(4)、取0.2000g 样品,配成100mL溶液,取50mL样品溶液于锥形瓶中,加入3滴溶液做指示剂,用0.0600的溶液滴定至终点时,消耗溶液的体积为10.00mL,样品的纯度为。(5)、某兴趣小组为探究的还原性,设计如下实验:实验I:粉红色的溶液在空气中久置,无明显变化。
实验II:向0.1 溶液中滴入2滴酸性溶液,无明显变化。
实验III:按下图装置进行实验,观察到电压表指针偏转。
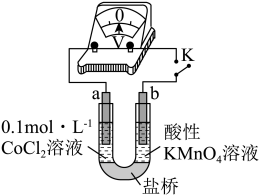
根据实验III得出结论:可以被酸性溶液氧化。
另一名同学设计了实验IV,否定了该结论,请说明实验IV的操作和现象。
18. 氧化铈()是一种应用非常广泛的稀土氧化物。现以氟碳铈矿(含、等)为原料制备氧化铈,其工艺流程如图所示:
已知:
①在空气中易被氧化,易与形成复盐沉淀;
②硫脲(
 )具有还原性,酸性条件下易被氧化为;
)具有还原性,酸性条件下易被氧化为;③在硫酸体系中能被萃取剂[]萃取,而不能。
回答下列问题:
(1)、“氧化焙烧”中氧化的目的是。(2)、步骤①中加入硫脲的目的是将四价铈还原为三价铈,写出硫脲与反应生成的离子方程式。(3)、步骤③反应的离子方程式为。(4)、步骤④萃取时存在反应:。分别在有机层中与水层中存在形式的物质的量浓度之比称为分配比()。取20mL含四价铈总浓度为0.1的酸浸液,向其中加入10mL萃取剂 , 充分振荡,静置,若 , 则水层中。(计算结果保留二位有效数字)。(5)、步骤⑤“反萃取”时双氧水的作用是。(6)、产品是汽车尾气净化催化剂中最重要的助剂,催化机理如图所示。写出过程①发生反应的化学方程式。 19. 化合物J是合成风湿性关节炎药物罗美昔布的一种中间体,其合成路线如下:
19. 化合物J是合成风湿性关节炎药物罗美昔布的一种中间体,其合成路线如下:
已知:
I.

II.

回答下列问题:
(1)、A的化学名称是 , C中官能团的名称是。(2)、C→D的化学方程式为。(3)、H→I的反应类型是 , 化合物E的结构简式。(4)、写出2种同时符合下列条件的化合物B的同分异构体的结构简式。①属于芳香族化合物且有两个六元环
②除苯环外,核磁共振氢谱显示有6组峰,峰面积之比为6:4:2:2:1:1
(5)、写出以甲苯和为主要原料合成化合物H的路线(无机试剂、有机溶剂任选)。20. 甲醇合成丙烯有“一步法”和“两步法”两种合成方式,“一步法”是在催化剂的作用下由甲醇直接合成丙烯;“两步法”则分两步合成,其热化学方程式如下:反应I:甲醇醚化反应(DME)
反应II:含氧化合物制丙烯反应(OTP)
已知部分键能数据如下:
化学键
C-C
C=C
C-H
H-H
O-H
C=O
C-O
键能/
356
615
413
436
462
745
360
回答下列问题:
(1)、“一步法”合成丙烯的热化学方程式为。合成丙烯时有乙烯等副产物,若选择作载气时,保持总压不变,调控甲醇和的不同分压,各产物的选择性如下表所示(其他产物略):分压/MPa
分压/MPa
丙烯选择性/%
乙烯选择性/%
0.10
0
30.9
7.51
0.08
0.02
32.0
7.42
0.04
0.06
34.8
7.03
0.02
0.08
36.7
6.48
0.01
0.09
39.4
5.43
分析表中数据:要合成得到更多的丙烯,应控制甲醇的最佳分压为MPa。
(2)、已知:。温度为500K时,在密闭反应器中加入2mol , 若只发生反应Ⅰ,达平衡状态时,体系中的物质的量分数为(填序号)。A. B. C. D.(3)、“两步法”中,在恒容密闭容器中通入甲醇,初始压强为 , 反应达到平衡时压强为 , 则平衡混合体系中,丙烯的体积分数为(用含、的式子表示,下同),若平衡时甲醇的转化率为60%,则反应II(OTP)的平衡常数。(4)、“两步法”中存在反应Ⅲ: △H,同时也会有芳香烃等副产品,其中丙烯和芳香烃选择性与不同温度下反应I进行的程度的关系如图所示。要提高丙烯的选择性,可采取的措施是 , 当温度高于285℃后,丙烯的选择性降低,其原因是。