江苏省淮安市涟水县2023年中考一模化学试题
试卷更新日期:2023-04-10 类型:中考模拟
一、单选题
-
1. 中华文化博大精深。下列过程中只涉及物理变化的是( )A、粮食酿酒 B、烧制陶瓷 C、甲骨刻字 D、火药爆炸2. 学校采购了一批含75%酒精的免洗手消毒喷雾,存放处应张贴的标志是( )A、
 B、
B、 C、
C、 D、
D、 3. 配制10%的稀硫酸并与碳酸钠粉末反应的部分操作如下,其中操作规范的是( )A、
3. 配制10%的稀硫酸并与碳酸钠粉末反应的部分操作如下,其中操作规范的是( )A、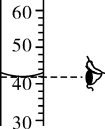 读取浓硫酸的体积
B、
读取浓硫酸的体积
B、 稀释浓硫酸
C、
稀释浓硫酸
C、 加入碳酸钠
D、
加入碳酸钠
D、 倾倒稀硫酸
4. 碳酸氢钠(NaHCO3)是焙制糕点所用发酵粉主要成分之一,下列有关说法正确的是( )A、NaHCO3中的阳离子为Na+ B、NaHCO3中含有3个氧原子 C、NaHCO3中碳元素和氧元素的质量比为1:3 D、NaHCO3也可用于治疗胃酸过多5. 日前,金属材料顶级期刊《Acta材料》刊登我国科学家成功研制用于外太空核反应堆的钼合金。钼元素在元素周期表中的信息如图所示。下列说法错误的是( )
倾倒稀硫酸
4. 碳酸氢钠(NaHCO3)是焙制糕点所用发酵粉主要成分之一,下列有关说法正确的是( )A、NaHCO3中的阳离子为Na+ B、NaHCO3中含有3个氧原子 C、NaHCO3中碳元素和氧元素的质量比为1:3 D、NaHCO3也可用于治疗胃酸过多5. 日前,金属材料顶级期刊《Acta材料》刊登我国科学家成功研制用于外太空核反应堆的钼合金。钼元素在元素周期表中的信息如图所示。下列说法错误的是( ) A、钼原子的核外电子数为42 B、三氧化钼的化学式是MoO3 C、钼的相对原子质量为95.96g D、钼合金比钼硬度大、强度高6. 关于“舌尖上的化学”,下列做法不科学的是( )A、为保鲜海产品,加入少量甲醛溶液浸泡 B、为摄取人体所需蛋白质,可食用适量肉、鱼类食物 C、为减少维生素C流失,炒蔬菜时可以加点食醋调味 D、为延长食品保质期,可在食品包装袋内充入氮气7. 下列物质的性质和用途,有直接联系的是( )A、浓硫酸有腐蚀性,在实验室中可用作干燥剂 B、金刚石无色透明,可用于制作钻头 C、碳酸氢铵受热易分解,可用作化肥 D、熟石灰溶于水呈碱性,可用于中和酸性废水8. 水是构成一切生物体的基本成分,是生命之源。下列说法错误的是( )
A、钼原子的核外电子数为42 B、三氧化钼的化学式是MoO3 C、钼的相对原子质量为95.96g D、钼合金比钼硬度大、强度高6. 关于“舌尖上的化学”,下列做法不科学的是( )A、为保鲜海产品,加入少量甲醛溶液浸泡 B、为摄取人体所需蛋白质,可食用适量肉、鱼类食物 C、为减少维生素C流失,炒蔬菜时可以加点食醋调味 D、为延长食品保质期,可在食品包装袋内充入氮气7. 下列物质的性质和用途,有直接联系的是( )A、浓硫酸有腐蚀性,在实验室中可用作干燥剂 B、金刚石无色透明,可用于制作钻头 C、碳酸氢铵受热易分解,可用作化肥 D、熟石灰溶于水呈碱性,可用于中和酸性废水8. 水是构成一切生物体的基本成分,是生命之源。下列说法错误的是( ) A、a管连接的是电源正极 B、a、b管内气体质量比为1:2 C、“干燥氢气”的目的是除去水蒸气,防止对检验水产生影响 D、如图两个实验均能验证水的组成9. 已知白磷的着火点是40℃,红磷的着火点是240℃。如图实验,三支试管里面充满氮气,初始温度20℃,升温至80℃后,用注射器同时向②③试管中迅速注入足量氧气。下列说法错误的是( )
A、a管连接的是电源正极 B、a、b管内气体质量比为1:2 C、“干燥氢气”的目的是除去水蒸气,防止对检验水产生影响 D、如图两个实验均能验证水的组成9. 已知白磷的着火点是40℃,红磷的着火点是240℃。如图实验,三支试管里面充满氮气,初始温度20℃,升温至80℃后,用注射器同时向②③试管中迅速注入足量氧气。下列说法错误的是( ) A、只有②中有燃烧现象 B、由①②现象说明可燃物达到着火点未必燃烧 C、若继续水浴升温,③中红磷也一定会燃烧 D、该实验能总结出燃烧的条件10. CuCl2是重要的化工原料。工业上常采用将Cu与稀盐酸在持续通入空气的条件下反应,FeCl3具有催化作用。反应原理如图所示。下列说法正确的是( )
A、只有②中有燃烧现象 B、由①②现象说明可燃物达到着火点未必燃烧 C、若继续水浴升温,③中红磷也一定会燃烧 D、该实验能总结出燃烧的条件10. CuCl2是重要的化工原料。工业上常采用将Cu与稀盐酸在持续通入空气的条件下反应,FeCl3具有催化作用。反应原理如图所示。下列说法正确的是( ) A、该实验说明Cu能与稀盐酸发生置换反应 B、参加反应的O2、HCl分子个数比为1:4 C、该反应过程中需要持续添加FeCl3溶液 D、该过程中只有铜、氧元素化合价发生改变
A、该实验说明Cu能与稀盐酸发生置换反应 B、参加反应的O2、HCl分子个数比为1:4 C、该反应过程中需要持续添加FeCl3溶液 D、该过程中只有铜、氧元素化合价发生改变二、填空题
-
11. 高铁酸钠(Na2FeO4)是一种新型净水剂。请用化学用语填空。(1)、高铁酸钠中一种金属元素的符号为。(2)、标出高铁酸钠中铁元素的化合价。(3)、消毒后生成铁离子的符号为。12. 如图所示为某地可持续农业生态系统一一“桑基鱼塘”的模式简图。
 (1)、蚕丝属于(选填“天然”或“合成”)纤维。(2)、桑叶茶中富含Ca、K等元素,其中能预防骨质疏松的是。(3)、塘泥用作肥料,促进桑叶生长茂盛、叶色浓绿,相当于(选填“氮肥”“磷肥”或“钾肥”)的作用。(4)、桑树的光合作用过程中,能量的转化形式为转化为化学能。13. 水是生命之源,是人类生产、生活中不可缺少的重要物质。(1)、化学实验室中经常用到水,如溶液的配制。配制50g溶质质量分数为6%的氯化钠溶液,需要水的体积为mL。(2)、水常用作物质溶解的溶剂。
(1)、蚕丝属于(选填“天然”或“合成”)纤维。(2)、桑叶茶中富含Ca、K等元素,其中能预防骨质疏松的是。(3)、塘泥用作肥料,促进桑叶生长茂盛、叶色浓绿,相当于(选填“氮肥”“磷肥”或“钾肥”)的作用。(4)、桑树的光合作用过程中,能量的转化形式为转化为化学能。13. 水是生命之源,是人类生产、生活中不可缺少的重要物质。(1)、化学实验室中经常用到水,如溶液的配制。配制50g溶质质量分数为6%的氯化钠溶液,需要水的体积为mL。(2)、水常用作物质溶解的溶剂。
①KNO3中混有少量NaCl,提纯KNO3可采用的方法是。
②10℃时,将等质量的KNO3、NaCl固体,分别加入到盛有100g水的两个烧杯中,搅拌,充分溶解,现象如图2所示。烧杯中一定是饱和溶液的是(填“KNO3”或“NaCl”)溶液。
③Ca(OH)2溶解度曲线如图3所示,将A点对应的Ca(OH)2溶液溶质质量分数增大,可采取的具体操作是。
三、科普阅读题
-
14. 阅读下面科普短文,并回答问题。
泡菜品种繁多、风味独特、口感鲜脆。新鲜蔬菜中含有硝酸盐,硝酸盐对人体无直接危害,但转化成亚硝酸盐后,就会对人体产生危害。亚硝酸盐【如亚硝酸钠(NaNO2)】与胃酸(主要成分是盐酸)反应,产生亚硝酸(HNO2)和氯化物(如NaCl)。亚硝酸不稳定,产生的二氧化氮进入血液与血红蛋白结合,会导致人中毒。
如图为室温下,食盐水浓度和泡制时间与芹菜泡制过程中亚硝酸盐含量的关系曲线。

用不同的蔬菜进行测定,亚硝酸盐含量变化趋势与芹菜相似。泡菜发酵过程中,泡制温度较高时,亚硝酸盐含量最大值出现得早,且数值低,这与温度较高有利于乳酸菌的繁殖有关。泡制过程中添加姜汁和维生素C,都能有效地减少亚硝酸盐的生成,现代医学证明,泡菜中的乳酸和乳酸菌对人体健康有益,具有抑制肠道中的腐败菌生长、降低胆固醇等保健作用。但是,有些泡菜盐分或糖分过高,对高血压和糖尿病等慢性病患者不利。另外,泡制过程也会造成某些营养素的流失。
请依据文章回答下列问题:
(1)、亚硝酸钠与盐酸的反应属于(填写基本反应类型)。(2)、室温下,用芹菜制作的泡来,最佳食用时间是____(填字母)。A、泡制2~3天 B、泡制5~6天 C、泡制12天后(3)、下列关于制作泡菜的说法中,不合理的是____(填字母)。A、最好加入一些姜汁 B、最好在较低温度下泡制 C、最好如入一些富含维生素C的水果 D、最佳食用期的泡菜中亚硝酸盐的含量与泡制时的食盐水浓度无关四、综合题
-
15. “5G”改变生活,“中国芯”彰显中国“智”造。芯片的基材主要是高纯硅(Si),如图是一种用石英砂(主要成分为SiO2)制备高纯硅的工艺流程图。
 (1)、已知粗硅的主要成分是硅单质,反应I的化学方程式是。(2)、操作I是。(3)、在实际制备过程中,反应Ⅱ要隔绝空气的原因是(写一条即可)。(4)、上述生产流程中可以循环利用的物质是(填化学式)。16. 在实验室里,利用如图实验装置制取有关气体。
(1)、已知粗硅的主要成分是硅单质,反应I的化学方程式是。(2)、操作I是。(3)、在实际制备过程中,反应Ⅱ要隔绝空气的原因是(写一条即可)。(4)、上述生产流程中可以循环利用的物质是(填化学式)。16. 在实验室里,利用如图实验装置制取有关气体。 (1)、图中仪器a的名称是。(2)、实验室用A、F装置制取氧气,反应的化学方程式为。(3)、B、C、D装置均可用作制取二氧化碳的发生装置,D装置与B、C装置相比,其突出优点是。若选择H装置采用排空气法收集二氧化碳,验满的方法是。(4)、某同学在使用A装置时发现试管固定得太高,该同学应调节如图中的旋钮。(填“①”“②”或“③”)
(1)、图中仪器a的名称是。(2)、实验室用A、F装置制取氧气,反应的化学方程式为。(3)、B、C、D装置均可用作制取二氧化碳的发生装置,D装置与B、C装置相比,其突出优点是。若选择H装置采用排空气法收集二氧化碳,验满的方法是。(4)、某同学在使用A装置时发现试管固定得太高,该同学应调节如图中的旋钮。(填“①”“②”或“③”) 17. 我国高铁创造的中国速度今世界瞩目,某学习小组对高铁建设中的铜铁锈蚀进行探究。
17. 我国高铁创造的中国速度今世界瞩目,某学习小组对高铁建设中的铜铁锈蚀进行探究。【提出问题】铁锈蚀与哪些因素有关。
【设计实验】
(1)、实验一:定性探究铁锈蚀的因素取四枚大小相同的洁净无锈铁钉分别放入试管。进行图1实验,现象如下表。

试管编号
A
B
C
D
一周后铁钉表面现象
有一层铁锈
无明显变化
无明显变化
有较厚铁锈
对比A、B、C试管中实验现象,说明铁锈蚀是与空气中的发生化学反应。
(2)、对比A和D试管中实验现象,说明铁锈蚀快慢与有关;(3)、实验二:定量探究影响铁锈蚀的因素
小组设计了图2装置,检查气密性,将5g铁粉和2g碳粉加入三颈烧瓶,t1时刻加入2mL饱和NaCl溶液后,再将一只装有5mL稀盐酸的注射器插到烧瓶上(此时没有推动注射器活塞),采集数据。
据图3分析,说明铁生锈(填“放热”或“吸热”),t2~t3这段时间反应并未停止但温度却开始降低,原因是。
(4)、据图3、图4分折,稀盐酸注入烧瓶中的时刻是(填“t2”或“t3”或“t4”)。(5)、实验三:测定部分生锈的铁粉中铁的含量连接如图5装置。取部分生锈的铁粉(铁和氧化铁的混合物)0.6g于锥形瓶中,加入足量稀盐酸进行实验。完全反应后,测得生成气体体积为0.2L,已知该条件下氢气密度为0.09g/L,根据以上数据,请计算该固体中铁的质量分数。(写出计算过程)
 (6)、学习小组有同学提出:用这种方法测得的气体体积不够准确,可能会导致测定的铁的质量分数偏大,可能的原因是(填序号)。
(6)、学习小组有同学提出:用这种方法测得的气体体积不够准确,可能会导致测定的铁的质量分数偏大,可能的原因是(填序号)。a.装置的气密性不好 b.铁与盐酸反应放热
c.装置内原来的空气没有排掉 d.没有扣掉加入的盐酸的体积
18. 学习小组同学用如图所示实验探究碱的化学性质。 (1)、小组同学做甲图所示实验时,当溶液恰好由红色变为无色,即停止了滴加稀盐酸,由此可以得出结论。做乙图所示实验时,观察到的实验现象有。丙图烧杯中溶液变浑浊,反应的化学方程式为。(2)、实验后,将甲、乙、丙中的物质均倒入洁净的废液缸,发现废液浑浊且呈红色。同学们很好奇,于是接着进行了下列的拓展学习与探究。
(1)、小组同学做甲图所示实验时,当溶液恰好由红色变为无色,即停止了滴加稀盐酸,由此可以得出结论。做乙图所示实验时,观察到的实验现象有。丙图烧杯中溶液变浑浊,反应的化学方程式为。(2)、实验后,将甲、乙、丙中的物质均倒入洁净的废液缸,发现废液浑浊且呈红色。同学们很好奇,于是接着进行了下列的拓展学习与探究。【拓展问题】
废液呈红色,说明废液显性。使废液变成红色的物质是什么?
【做出猪想】
猜想一:只有Na2CO3
猜想二:只有NaOH
猜想三:NaOH和Ca(OH)2
猜想四:NaOH和Na2CO3
猜想五:NaOH、Ca(OH)2和Na2CO3
你认为以上猜想中,不合理的猜想除了猜想五外,还有。
【查阅资料】CaCl2溶液呈中性。
【验证猜想】
静置一段时间后,取少量废液缸中的上层红色清液于试管中,加入过量CaCl2溶液,观察到 , 由此证明了猜想四成立。
-