河南省驻马店市确山县2023年中考一模化学试题
试卷更新日期:2023-04-07 类型:中考模拟
一、单选题
-
1. 杂交水稻之父袁隆平说“人就像一粒种子,要做一粒好的种子”。水稻种子的主要成分是淀粉,淀粉属于( )A、蛋白质 B、糖类 C、油脂 D、维生素2. 变化观念是化学学科核心素养之一。下列变化中属于化学变化的是( )A、蔗糖溶解 B、高炉炼铁 C、干冰升华 D、火柴梗被折断3. 建设美丽淮安,人人有责。下列做法中,不利于改善环境的是( )A、推广使用一次性餐具 B、禁止燃放烟花爆竹 C、使用可降解塑料制品 D、倡导乘坐公共交通工具出行4. 物质由微观粒子构成,下列都由离子构成的一组物质是( )A、氯化钠、硫酸铜 B、水、干冰 C、金刚石、氧化汞 D、氦气、氢气5. 铜可做导线,说明铜具有良好的( )A、导电性 B、延展性 C、导热性 D、抗腐蚀性6. 水是人类的宝贵自然资源。下列关于水的说法正确的是( )A、把硬水煮沸包含了化学变化 B、部分结冰的蒸馏水属于混合物 C、保持水的化学性质的粒子是氢原子和氧原子 D、硬水中有较多含钙的矿物质,可以多喝硬水补钙7. 下列实验操作正确的是( )A、
 B、
B、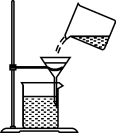 C、
C、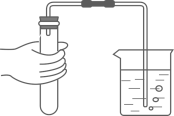 D、
D、 8. 环境问题已成为制约社会发展和进步的严重问题。下列有几种说法:
8. 环境问题已成为制约社会发展和进步的严重问题。下列有几种说法:①臭氧层的主要作用是吸收紫外线
②温室效应将导致全球气候变暖
③酸雨主要是由SO2、NO2等污染物所致
④汽车排放的尾气会造成空气污染。其中正确的是( )
A、①② B、②③ C、①②③ D、①②③④9. 蔬菜、水果富含维生素C(C6H8O6)。下列有关维生素C的说法正确的是( )A、维生紫C中有20个原子 B、碳、氢元素质量比为3:4 C、维生素C中O元素质量分数最大 D、相对分子质量是176g10. 如图是A、B两物质的溶解度曲线,下列信息中正确的是( ) A、图中阴影部分表明A、B两物质的溶液都是饱和溶液 B、t2℃时,A物质溶液的浓度大于B物质溶液的浓度 C、t1℃时,A、B两物质的饱和溶液中溶质质量相等 D、t2℃时等质量的A、B两物质的饱和溶液降温到t1℃时析出溶质的质量A>B11. AgNO3受热分解生成了Ag、NO2和气体X,关于X元素组成说法正确的是( )A、一定含有氮元素 B、一定含有氧元素 C、一定含有银元素 D、一定含有氮、氧元素12. 材料、能源、环境与健康等问题的解决离不开化学知识。下列说法错误的是( )A、塑料、合成纤维和合成橡胶都属于合成材料 B、太阳能、氢能、地热能都属于新能源 C、化石燃料燃烧产生的二氧化碳会导致酸雨 D、合理摄入钙元素,可有效预防佝偻病或骨质疏松症13. 下列图像不能正确反映化学反应原理的是( )A、
A、图中阴影部分表明A、B两物质的溶液都是饱和溶液 B、t2℃时,A物质溶液的浓度大于B物质溶液的浓度 C、t1℃时,A、B两物质的饱和溶液中溶质质量相等 D、t2℃时等质量的A、B两物质的饱和溶液降温到t1℃时析出溶质的质量A>B11. AgNO3受热分解生成了Ag、NO2和气体X,关于X元素组成说法正确的是( )A、一定含有氮元素 B、一定含有氧元素 C、一定含有银元素 D、一定含有氮、氧元素12. 材料、能源、环境与健康等问题的解决离不开化学知识。下列说法错误的是( )A、塑料、合成纤维和合成橡胶都属于合成材料 B、太阳能、氢能、地热能都属于新能源 C、化石燃料燃烧产生的二氧化碳会导致酸雨 D、合理摄入钙元素,可有效预防佝偻病或骨质疏松症13. 下列图像不能正确反映化学反应原理的是( )A、 等质量、等质量分数的稀硫酸与足量镁、铁反应
B、
等质量、等质量分数的稀硫酸与足量镁、铁反应
B、 高锰酸钾受热分解制氧气
C、
高锰酸钾受热分解制氧气
C、 碳酸钙在高温下分解
D、
碳酸钙在高温下分解
D、 向等质量的水中分别加入相同质量的氢氧化钠固体和硝酸铵固体
14. 某金属粉末可能由镁、铝、铁中的一种或多种组成。取该金属粉末样品2.4g,放入一定量稀盐酸中,恰好完全反应,生成0.2g氢气。下列说法正确的是( )A、样品中一定含有镁 B、样品中一定含有镁、铝、铁 C、反应后溶液中溶质质量为9.5g D、反应后溶质可能为MgCl2、AlCl3和FeCl3
向等质量的水中分别加入相同质量的氢氧化钠固体和硝酸铵固体
14. 某金属粉末可能由镁、铝、铁中的一种或多种组成。取该金属粉末样品2.4g,放入一定量稀盐酸中,恰好完全反应,生成0.2g氢气。下列说法正确的是( )A、样品中一定含有镁 B、样品中一定含有镁、铝、铁 C、反应后溶液中溶质质量为9.5g D、反应后溶质可能为MgCl2、AlCl3和FeCl3二、填空题
-
15. 空气中含量多且常用作保护气的是;地壳中含量最高的元素是。16. 中国探月工程“绕、落、回”三步已经圆满收官,“探、登、驻”三大阶段已在路上。在月球上,岩石基本都是岩浆岩,以硅铝矿物(氧化铝和二氧化硅)和铁镁矿物(氧化亚铁和氧化镁)为主。氧化铝中各元素的质量比为 , 标出二氧化硅中硅元素的化合价。17. 金属在生产生活中具有广泛的应用。(1)、下列金属制品中,主要利用金属导热性的是____(填字母)。A、金属硬币 B、铝制导线 C、铜制火锅(2)、波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、生石灰加水配制而成,不能用铁质容器配制波尔多液的原因是(用化学方程式表示)。(3)、铝具有良好的抗腐蚀性能,原因是(用文字阐述)。18. 请按要求书写文字表达式。(1)、产生明亮的蓝紫色火焰的反应。(2)、剧烈燃烧,火星四射,生成黑色固体的反应。19. 某化学兴趣小组的同学设计制备氧气及探究可燃物燃烧条件的实验装置如图所示。实验时,可观察到铜片上的白磷和水中的白磷都燃烧,而红磷未燃烧。锥形瓶中发生的反应的化学方程式为;通过铜片上的白磷燃烧而红磷不燃烧的实验现象,可说明燃烧需要满足的条件之一是。
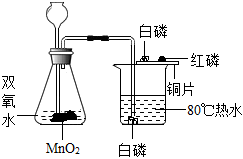 20. 已知A-E均为初中化学常见的物质,C是最常见的溶剂,D广泛用于玻璃、造纸、纺织和洗涤剂的生产等。它们之间的关系如图所示。(“一”表示相互反应,“→”表示反应一步实现,部分反应物和生成物已略去)
20. 已知A-E均为初中化学常见的物质,C是最常见的溶剂,D广泛用于玻璃、造纸、纺织和洗涤剂的生产等。它们之间的关系如图所示。(“一”表示相互反应,“→”表示反应一步实现,部分反应物和生成物已略去)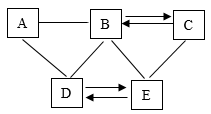 (1)、C的化学式是。(2)、A一B所属的基本反应类型为。(3)、B一D的化学方程式为。E→D的化学方程式为。21. 如图所示为探究可燃物燃烧条件的装置。
(1)、C的化学式是。(2)、A一B所属的基本反应类型为。(3)、B一D的化学方程式为。E→D的化学方程式为。21. 如图所示为探究可燃物燃烧条件的装置。 (1)、甲装置中热水的作用的是什么?(2)、请简述乙装置相对于甲装置的优点。22. 化学与人类生活密不可分。请用所学知识解释下列现象。(1)、用洗洁精可以除去餐具上的油污。(2)、铝的化学性质活泼,为什么铝制品却具有很好的抗腐蚀性能?(用化学方程式表示)。23. 水是地球表面覆盖最多的物质,也是生命活动不可缺少的物质。(1)、电解水过程与水的蒸发过程微观本质上的区别是。(2)、可以用固体高锰酸钾和水配制消毒液。将高锰酸钾和水依次倒入烧杯中,用玻璃棒搅拌,其目的是。24. 如下图是配制80克质量分数为10%的氯化钠溶液的操作过程示意图。试回答:
(1)、甲装置中热水的作用的是什么?(2)、请简述乙装置相对于甲装置的优点。22. 化学与人类生活密不可分。请用所学知识解释下列现象。(1)、用洗洁精可以除去餐具上的油污。(2)、铝的化学性质活泼,为什么铝制品却具有很好的抗腐蚀性能?(用化学方程式表示)。23. 水是地球表面覆盖最多的物质,也是生命活动不可缺少的物质。(1)、电解水过程与水的蒸发过程微观本质上的区别是。(2)、可以用固体高锰酸钾和水配制消毒液。将高锰酸钾和水依次倒入烧杯中,用玻璃棒搅拌,其目的是。24. 如下图是配制80克质量分数为10%的氯化钠溶液的操作过程示意图。试回答: (1)、B操作中应称量氯化钠的质量是 , 放好砝码和游码后,向托盘中加入氯化钠过程中,若指针偏向分度盘的左边,应进行的操作是。(2)、D操作应选用的量筒(从10mL、100mL中选择),量水时量筒必须平放,视线要与量筒凹液面的处保持水平。(3)、E操作的作用是。25. 化学兴趣小组的同学在实验室进行粗盐提纯的实验,并配制一定溶质质量分数的氯化钠溶液。(1)、实验一:粗盐初步提纯
(1)、B操作中应称量氯化钠的质量是 , 放好砝码和游码后,向托盘中加入氯化钠过程中,若指针偏向分度盘的左边,应进行的操作是。(2)、D操作应选用的量筒(从10mL、100mL中选择),量水时量筒必须平放,视线要与量筒凹液面的处保持水平。(3)、E操作的作用是。25. 化学兴趣小组的同学在实验室进行粗盐提纯的实验,并配制一定溶质质量分数的氯化钠溶液。(1)、实验一:粗盐初步提纯
①操作I中玻璃棒的作用是。
②蒸发结晶时,当观察到时,停止加热。
③若产率偏低,写出一条可能的原因。
(2)、实验二:粗盐“再”提纯若“实验一”得到的精盐中,只含有NaCl和MgCl2 , 请设计实验方案除去MgCl2得到纯净的NaCl。(提醒:除杂试剂的量选择适量)
实验方案
化学方程式
结论
。
。
所得固体为NaCl
(3)、实验三:用“实验二”提纯的NaCl配制50g溶质质量分数为6%的氯化钠溶液,配制过程包括如下操作。
①该实验正确的操作顺序是(填字母)。
②如果配制的氯化钠溶液的溶质质量分数大于10%,则可能是量取水时(选填“仰视”或“俯视”)读数导致。
③将已配好的50g质量分数为6%的氯化钠溶液稀释成质量分数为3%的氯化钠溶液,需要再加水的质量是g。