广西贵港市平南县2023年中考一模化学试题
试卷更新日期:2023-04-07 类型:中考模拟
一、单选题
-
1. 下列氧气的性质中,属于化学性质的是( )A、无色无味 B、沸点低 C、能支持燃烧 D、不易溶于水2. 下列措施中,不能防止金属制品锈蚀的是()A、在表面刷漆 B、在表面涂油 C、在表面镀铬 D、用湿布擦拭3. 今年我市关于“禁止燃放烟花爆竹”的规定中,禁止燃放的区域除城区外新增了部分乡镇。下列表示“禁止燃放鞭炮”的图标是( )A、
 B、
B、 C、
C、 D、
D、 4. 2021年,科学家通过“化学/生化”途径,人工合成了淀粉。淀粉属于( )A、糖类 B、油脂 C、蛋白质 D、维生素5. 下列关于空气的说法错误的是( )A、空气是一种混合物 B、空气中氧气的体积分数约为21% C、空气是一种宝贵的资源 D、稀有气体不与任何物质发生化学反应6. 正确的实验操作是化学实验成功的重要保证。下列实验操作正确的是( )A、熄灭酒精灯
4. 2021年,科学家通过“化学/生化”途径,人工合成了淀粉。淀粉属于( )A、糖类 B、油脂 C、蛋白质 D、维生素5. 下列关于空气的说法错误的是( )A、空气是一种混合物 B、空气中氧气的体积分数约为21% C、空气是一种宝贵的资源 D、稀有气体不与任何物质发生化学反应6. 正确的实验操作是化学实验成功的重要保证。下列实验操作正确的是( )A、熄灭酒精灯 B、加热液体
B、加热液体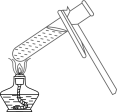 C、量取水时读数
C、量取水时读数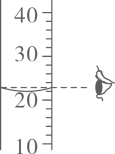 D、称量氯化钠固体
D、称量氯化钠固体 7. 下列做法有利于实现“碳达峰、碳中和”的是( )A、石油炼制 B、焚烧秸秆 C、风能发电 D、一氧化碳作燃料8. 化学与生产、生活、环保等密切相关。下列有关说法错误的是( )A、电池可将化学能转化为电能 B、随意丢弃聚乙烯塑料不产生污染 C、强热使煤焦化属于化学变化 D、维生素D有助于骨骼的生长发育9. 化学与人类健康密切相关。下列说法错误的是( )A、霉变大米洗净、煮熟后可以食用 B、不吃超过保质期的食物 C、食用蔬菜和水果可补充维生素 D、合理摄入油脂有益身体健康10. 合理使用化肥,促进农作物生长,提高粮食产量。下列物质属于复合肥料的是( )A、K2SO4 B、Ca3(PO4)2 C、CO(NH2)2 D、KNO311. 随着科学技术的发展,许多新能源走进了我们的生活。下列能源属于新能源的是( )A、煤 B、太阳能 C、石油 D、天然气12. 氢气燃烧的反应微观示意图如图所示。该反应的基本反应类型是( )
7. 下列做法有利于实现“碳达峰、碳中和”的是( )A、石油炼制 B、焚烧秸秆 C、风能发电 D、一氧化碳作燃料8. 化学与生产、生活、环保等密切相关。下列有关说法错误的是( )A、电池可将化学能转化为电能 B、随意丢弃聚乙烯塑料不产生污染 C、强热使煤焦化属于化学变化 D、维生素D有助于骨骼的生长发育9. 化学与人类健康密切相关。下列说法错误的是( )A、霉变大米洗净、煮熟后可以食用 B、不吃超过保质期的食物 C、食用蔬菜和水果可补充维生素 D、合理摄入油脂有益身体健康10. 合理使用化肥,促进农作物生长,提高粮食产量。下列物质属于复合肥料的是( )A、K2SO4 B、Ca3(PO4)2 C、CO(NH2)2 D、KNO311. 随着科学技术的发展,许多新能源走进了我们的生活。下列能源属于新能源的是( )A、煤 B、太阳能 C、石油 D、天然气12. 氢气燃烧的反应微观示意图如图所示。该反应的基本反应类型是( ) A、分解反应 B、置换反应 C、化合反应 D、复分解反应13. 下列物质不是由分子构成的是( )A、氧气 B、水 C、氯化氢 D、氯化钠14. “84消毒液”是一种含氯消毒剂,可以有效杀死新冠病毒。它的有效成分是次氯酸钠(化学式:NaClO)。次氯酸钠中氯元素的化合价是( )A、-1 B、0 C、+1 D、+715. 推理是学习化学的一种重要方法,必须严谨、科学。下列说法正确的是( )A、单质是由同种元素组成的物质,所以由同种元素组成的纯净物一定是单质 B、酸溶液的pH<7,所以pH<7的溶液一定是酸溶液 C、燃烧都伴有发光、放热现象,所以有发光、放热现象的一定是燃烧 D、中和反应生成盐和水,所以生成盐和水的反应一定是中和反应16. 下列实验方案能达到实验目的的是( )
A、分解反应 B、置换反应 C、化合反应 D、复分解反应13. 下列物质不是由分子构成的是( )A、氧气 B、水 C、氯化氢 D、氯化钠14. “84消毒液”是一种含氯消毒剂,可以有效杀死新冠病毒。它的有效成分是次氯酸钠(化学式:NaClO)。次氯酸钠中氯元素的化合价是( )A、-1 B、0 C、+1 D、+715. 推理是学习化学的一种重要方法,必须严谨、科学。下列说法正确的是( )A、单质是由同种元素组成的物质,所以由同种元素组成的纯净物一定是单质 B、酸溶液的pH<7,所以pH<7的溶液一定是酸溶液 C、燃烧都伴有发光、放热现象,所以有发光、放热现象的一定是燃烧 D、中和反应生成盐和水,所以生成盐和水的反应一定是中和反应16. 下列实验方案能达到实验目的的是( )选项
实验目的
实验方案
A
除去Cu(NO3)2溶液中的AgNO3
加入过量铁粉,过滤
B
分离KCl和MnO2固体
加水溶解,过滤
C
除去NaCl固体中少量的NH4Cl
加入足量Ca(OH)2固体,研磨
D
鉴别羊毛线和棉线
取样,在空气中灼烧,闻气味
A、A B、B C、C D、D17. 下列物质间的转化关系,不能实现的是( )A、H2O2→H2O→H2CO3 B、Mg→MgO→MgSO4 C、KCl→KNO3→K2SO4 D、Cu(OH)2→CuSO4→CuCl218. 已知白磷的着火点约为40℃,红磷的着火点约为240℃。如图实验,三支试管里面充满氮气,初始温度25℃,水浴加热至60℃后,用注射器同时向②③试管中迅速注入足量氧气。下列说法错误的是( ) A、只有②中有燃烧现象 B、若继续水浴升温,则③中一定会燃烧于水浴加热 C、该实验能总结出燃烧的条件 D、由①②现象说明可燃物达着火点未必燃烧19. 向一定量的氢氧化钠溶液中逐滴加入稀硫酸。溶液中氢氧化钠的质量、水的质量、硫酸钠的质量随稀硫酸的质量的变化关系如图所示。下列说法错误的是( )
A、只有②中有燃烧现象 B、若继续水浴升温,则③中一定会燃烧于水浴加热 C、该实验能总结出燃烧的条件 D、由①②现象说明可燃物达着火点未必燃烧19. 向一定量的氢氧化钠溶液中逐滴加入稀硫酸。溶液中氢氧化钠的质量、水的质量、硫酸钠的质量随稀硫酸的质量的变化关系如图所示。下列说法错误的是( ) A、乙代表水的质量,丙代表硫酸钠的质量 B、加入Ng稀硫酸时,两者恰好完全反应 C、a点对应的溶液中含有三种溶质 D、b点对应的溶液中含有的阳离子只有H+、Na+20. 某不纯的Na2CO3粉末中,含有NaCl、CaCO3、CuSO4中的一种或几种杂质。为了探究其成分组成,现取10.6g该粉末,向其中加入100g7.3%的稀盐酸,粉末全部溶解,得到无色溶液,同时生成4g气体。下列说法错误的是( )A、粉末中一定没有CuSO4 B、粉末中可能含有NaCl C、粉末中可能含有CaCO3 D、粉末成分组成有两种可能
A、乙代表水的质量,丙代表硫酸钠的质量 B、加入Ng稀硫酸时,两者恰好完全反应 C、a点对应的溶液中含有三种溶质 D、b点对应的溶液中含有的阳离子只有H+、Na+20. 某不纯的Na2CO3粉末中,含有NaCl、CaCO3、CuSO4中的一种或几种杂质。为了探究其成分组成,现取10.6g该粉末,向其中加入100g7.3%的稀盐酸,粉末全部溶解,得到无色溶液,同时生成4g气体。下列说法错误的是( )A、粉末中一定没有CuSO4 B、粉末中可能含有NaCl C、粉末中可能含有CaCO3 D、粉末成分组成有两种可能二、填空题
-
21. 用化学用语填空。(1)、氮元素。(2)、氖气。(3)、四氧化三铁。(4)、3个硫原子。(5)、5个氢氧根离子。22. 从下列选项中选择适当的物质填空(填字母序号)。
A.食盐 B.明矾 C.石墨 D.氮气 E.熟石灰
(1)、可用于净水的是。(2)、可用作食品保鲜保护气的是。(3)、可用作电极的是。(4)、可用于腌制食品的是。(5)、可用于改良酸性土壤的是。23. 第24届北京冬奥会向全世界展示了“中国智造”。请回答下列问题。(1)、“冰墩墩”的冰晶外壳由塑料制成,塑料属于(填“天然材料”或“合成材料”)。(2)、冬奥会新场馆使用了大量铝合金,铝合金具有(举一例)的优点。场馆内的冰壶机器人,选用以氧化锂(Li2O)为原料制造的锂电池。氧化锂中锂、氧元素的质量比是(填最简比)。(3)、冬奥会运用的5G通信技术是一大科技亮点,5G通信芯片是用氮化镓材料制成的。如图是镓(Ga)原子的结构示意图,镓原子的质子数为 , 镓离子的符号为。 (4)、冬奥火炬“飞扬”采用氢气作燃料,实现零碳排放。关闭火炬的燃气开关,使火炬熄灭,其灭火原理是。24. 人体中各元素的含量如图所示,个体会存在微小差异。请回答下列问题。
(4)、冬奥火炬“飞扬”采用氢气作燃料,实现零碳排放。关闭火炬的燃气开关,使火炬熄灭,其灭火原理是。24. 人体中各元素的含量如图所示,个体会存在微小差异。请回答下列问题。 (1)、含量超过0.01%的元素称为常量元素,11种常量元素中非金属元素共有种;人体缺乏微量元素元素可能会引起贫血。(2)、下列有关化学元素与人体健康的说法正确的是____。A、微量元素是因为对健康的作用微小而命名的 B、铜元素为重金属元素,对人体健康毫无益处 C、人体中常量元素的总质量约占人体总质量的99.95%(3)、下图是硫元素在元素周期表的位置图。硫元素位于第周期,其原子在化学反应中易(填“失去”或“得到”)电子。
(1)、含量超过0.01%的元素称为常量元素,11种常量元素中非金属元素共有种;人体缺乏微量元素元素可能会引起贫血。(2)、下列有关化学元素与人体健康的说法正确的是____。A、微量元素是因为对健康的作用微小而命名的 B、铜元素为重金属元素,对人体健康毫无益处 C、人体中常量元素的总质量约占人体总质量的99.95%(3)、下图是硫元素在元素周期表的位置图。硫元素位于第周期,其原子在化学反应中易(填“失去”或“得到”)电子。 25. 水是一切生命体生存所必需的物质。请回答下列问题。(1)、爱护水资源,人人有责。下列做法正确的是____。(填字母序号)A、水龙头漏水不及时更换 B、生活污水集中处理和排放 C、洗菜水冲厕所 D、农业上合理使用农药和化肥(2)、小新同学从西江取回水样,用自制净水器处理,净水器可以利用(填写物质名称)吸附水样中的异味和色素。(3)、NH4Cl和KNO3在不同温度时的溶解度如下表,请回答下列问题。
25. 水是一切生命体生存所必需的物质。请回答下列问题。(1)、爱护水资源,人人有责。下列做法正确的是____。(填字母序号)A、水龙头漏水不及时更换 B、生活污水集中处理和排放 C、洗菜水冲厕所 D、农业上合理使用农药和化肥(2)、小新同学从西江取回水样,用自制净水器处理,净水器可以利用(填写物质名称)吸附水样中的异味和色素。(3)、NH4Cl和KNO3在不同温度时的溶解度如下表,请回答下列问题。温度/℃
20
30
40
50
60
溶解度/g
NH4Cl
37.2
41.4
45.8
50.4
55.2
KNO3
31.6
45.8
63.9
85.5
110
①40℃时,NH4Cl的溶解度是g。60℃时,向100g水中加入120gKNO3固体,所得溶液的质量是g。
②将等质量的NH4Cl、KNO3饱和溶液分别由50℃降温至20℃,所得NH4Cl溶液中溶质的质量分数(填“<”“=”或“>”)KNO3溶液中溶质的质量分数。
三、科普阅读题
-
26. 请阅读和分析下列材料,回答下列问题。
二氧化硫是有刺激性气味的无色气体;易溶于水,溶于水中时,会形成亚硫酸(H2SO3)。二氧化硫是大气污染物之一,空气中的二氧化硫主要来源于火山的喷发、工业废气的排放以及煤的燃烧。二氧化硫也是食品加工中常用的漂白剂和防腐剂,广泛应用于干制果蔬、面粉、葡萄酒等食品的加工,但必须严格按照国家有关范围和标准使用。
(1)、二氧化硫具有的物理性质是(举一例即可)。它属于(填“单质”“氧化物”“酸”“碱”或“盐”)。(2)、二氧化硫造成大气污染的主要问题是。为了减少其对大气的污染,你认为在生活生产中可采取的有效措施是(举一例即可)。(3)、写出二氧化硫溶于水时所发生反应的化学方程式:。四、综合题
-
27. NaCl是日常生活的必需品,也是重要的化工原料。工业上用粗盐(含有少量Ca2+、Mg2+、等杂质离子)提纯NaCl,其流程如下图所示。请回答下列问题。
 (1)、操作1加水溶解的过程中,为了加快溶解,可以采取的措施是(举一例即可)。操作2的名称是。(2)、在a处添加过量的试剂①饱和Na2CO3溶液、②NaOH溶液、③BaCl2溶液,以除去粗盐中的Ca2+、Mg2+、离子,试剂的添加顺序为:(填序号)。(3)、在溶液I中加入稀盐酸,其目的是。(4)、NaCl是无机化工生产之母,通电电解饱和氯化钠溶液可以得到氢氧化钠、氢气和氯气(Cl2),该反应的化学方程式是。28. 如图是实验室常用的实验装置,据图回答问题。
(1)、操作1加水溶解的过程中,为了加快溶解,可以采取的措施是(举一例即可)。操作2的名称是。(2)、在a处添加过量的试剂①饱和Na2CO3溶液、②NaOH溶液、③BaCl2溶液,以除去粗盐中的Ca2+、Mg2+、离子,试剂的添加顺序为:(填序号)。(3)、在溶液I中加入稀盐酸,其目的是。(4)、NaCl是无机化工生产之母,通电电解饱和氯化钠溶液可以得到氢氧化钠、氢气和氯气(Cl2),该反应的化学方程式是。28. 如图是实验室常用的实验装置,据图回答问题。 (1)、A图中标号a的仪器名称是。(2)、实验室若用装置AF制取并收集氧气,其反应的化学方程式是 , 证明已集满的现象是;A图中棉花的作用是。(3)、实验室若用大理石和稀盐酸制取二氧化碳,可选用E为收集装置,选用的主要理由是。将净化后的二氧化碳通入紫色石蕊试液中(如图G),可观察到试管中溶液逐渐变色,据此得出的结论是。29. 为了深度学习探究初中酸碱盐的内容,某化学小组根据酸碱盐之间的转化关系开展项目式学习。
(1)、A图中标号a的仪器名称是。(2)、实验室若用装置AF制取并收集氧气,其反应的化学方程式是 , 证明已集满的现象是;A图中棉花的作用是。(3)、实验室若用大理石和稀盐酸制取二氧化碳,可选用E为收集装置,选用的主要理由是。将净化后的二氧化碳通入紫色石蕊试液中(如图G),可观察到试管中溶液逐渐变色,据此得出的结论是。29. 为了深度学习探究初中酸碱盐的内容,某化学小组根据酸碱盐之间的转化关系开展项目式学习。 (1)、任务一:探究中和反应。
(1)、任务一:探究中和反应。如图甲所示,将稀盐酸逐滴滴到烧杯中,当看到烧杯中的溶液恰好由色变为无色时,即停止了滴加稀盐酸。烧杯中所发生反应的化学方程式为。
(2)、任务二:探究酸碱盐之间的反应。如图乙和丙所示,实验探究碱的化学性质。图乙中向下推注射器的活塞后,可观察到的现象是。
(3)、将图甲、乙、丙中实验后得到的无色溶液均倾倒入一只洁净的废液缸中,发现废液缸中的废液呈红色且明显变浑浊。小组同学对废液缸中的废液继续进行探究。【交流讨论】
①废液缸中的废液呈红色,说明废液显性(填“酸”“碱”或“中”)。
②废液缸中的废液明显变浑浊,说明倾倒前丙的溶液中含有(填化学式)。
(4)、【提出问题】使废液呈现红色的物质是什么?【做出猜想】猜想一:NaOH;猜想二:NaOH和Ca(OH)2;猜想三:NaOH和Na2CO3
【查阅资料】BaCl2溶液呈中性。
【实验探究】
实验操作
实验现象
实验结论
取少量废液缸中的上层红色清液于试管中,加入过量BaCl2溶液,静置
有白色沉淀生成,溶液仍呈红色
猜想成立
(5)、【拓展延伸】废液缸中的废液里所含有的阴离子是(填写离子符号)。小组同学在老师的指导下对废液进行无害化处理,避免了污染环境。五、计算题
-
30. 某学习小组的同学为了测定某黄铜(铜锌合金)中铜的含量,取该黄铜样品50g放入大烧杯中,再将300g稀硫酸分3次加入烧杯中,每次充分反应后,分别测得剩余固体的质量记录如下。
加入次数
第1次
第2次
第3次
加入稀硫酸的质量/g
100
100
100
充分反应后剩余固体的质量/g
43.5
m
34
请根据实验数据计算,并回答下列问题。
(1)、m的值为。(2)、该黄铜样品中铜的质量分数为。(3)、计算所用稀硫酸的溶质质量分数。(写出计算过程,结果精确到0.1%)
-