广东省茂名市茂南区2023年中考一模化学试题
试卷更新日期:2023-04-07 类型:中考模拟
一、单选题
-
1. 春节是我国的传统节日,有着悠久的文化历史,下列春节习俗包含有化学变化的是( )A、贴春联 B、剪窗花 C、穿新衣 D、放鞭炮2. 化学实验室存放浓硫酸的药品柜上应贴的标志是是( )A、
 B、
B、 C、
C、 D、
D、 3. 下列物质属于氧化物的是( )A、金刚石 B、干冰 C、烧碱 D、空气4. 下列化学用语表示正确的是( )A、磷元素:P B、水: C、镁离子: D、2个氯原子:Cl25. 规范操作是实验成功的基础。下列操作正确的是( )A、放置滴管
3. 下列物质属于氧化物的是( )A、金刚石 B、干冰 C、烧碱 D、空气4. 下列化学用语表示正确的是( )A、磷元素:P B、水: C、镁离子: D、2个氯原子:Cl25. 规范操作是实验成功的基础。下列操作正确的是( )A、放置滴管 B、添加酒精
B、添加酒精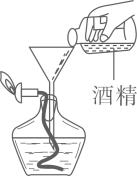 C、稀释浓硫酸
C、稀释浓硫酸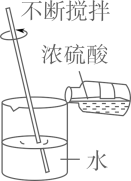 D、量筒读数
D、量筒读数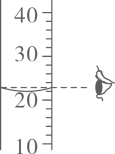 6. 我国北斗三号全球卫星导航系统正式开通,北斗卫星天线金属丝的主要成分有高纯度银,银元素在元素周期表中的信息及银原子结构示意图如图所示,下列说法错误的是( )
6. 我国北斗三号全球卫星导航系统正式开通,北斗卫星天线金属丝的主要成分有高纯度银,银元素在元素周期表中的信息及银原子结构示意图如图所示,下列说法错误的是( ) A、原子的质子数为42 B、银元素的相对原子质量是95.94g C、银原子核外电子排布图中x为12 D、铝原子在化学变化中易失去电子7. 化学与生活密切相关,下列说法错误的是( )A、用稀有气体制成多种用途的由光源 B、为节约和环保,分类回收生活垃圾 C、生活中常采用煮沸的方法降低水的硬度 D、在窗内放一盆水能防止煤气中毒8. 小明妈妈为他迎接中考制定了如下食谱:
A、原子的质子数为42 B、银元素的相对原子质量是95.94g C、银原子核外电子排布图中x为12 D、铝原子在化学变化中易失去电子7. 化学与生活密切相关,下列说法错误的是( )A、用稀有气体制成多种用途的由光源 B、为节约和环保,分类回收生活垃圾 C、生活中常采用煮沸的方法降低水的硬度 D、在窗内放一盆水能防止煤气中毒8. 小明妈妈为他迎接中考制定了如下食谱:主食
米饭
配菜
红烧肉、三杯鸡、鱼头豆腐汤
为使营养均衡,你觉得最好还要补充( )
A、牛肉 B、河虾 C、青菜 D、雪糕9. “证据推理与模型认知”是化学学科核心素养的重要组成部分。下列推断合理的是( )A、因为蜡烛燃烧生成和 , 所以蜡烛组成里一定含有碳元素和氢元素 B、离子是带电的粒子,则带电的粒子一定是离子 C、溶液是均一、稳定的,所以均一、稳定的液体一定是溶液 D、洗涤剂去油污是利用了乳化作用,汽油去油污也是利用了乳化作用10. 对下列事实的解释错误的是( )选项
事实
解释
A
闻到花香
分子在不断运动
B
盐酸能导电
溶液中含有自由移动的离子
C
水银温度计受热时示数上升
温度升高,汞原子体积变大
D
氧气与氢气化学性质不同
分子种类不同,物质化学性质不同
A、A B、B C、C D、D11. 如图为某化学反应的微观模拟示意图,下列有关该反应的说法中,错误的是( ) A、甲物质为氨气,其化学式为NH3 B、图示中x的值为2 C、参加反应的甲、乙两物质的质量比为17:24 D、该反应属于置换反应12. 甲、乙两种固体物质的溶解度曲线如图所示,下列说法错误的是( )
A、甲物质为氨气,其化学式为NH3 B、图示中x的值为2 C、参加反应的甲、乙两物质的质量比为17:24 D、该反应属于置换反应12. 甲、乙两种固体物质的溶解度曲线如图所示,下列说法错误的是( ) A、t2℃时,甲与乙的溶解度均为40g B、t3℃时,若将甲溶液由N点转变为M点状态,可采取添加溶质的方法 C、t1℃时,30g固体甲溶解在50g水中形成不饱和溶液 D、将t3℃时乙的饱和溶液降温至t2℃,有晶体析出13. 控制变量法实验探究重要方法。利用如图所示的实验能实现探究目的是( )
A、t2℃时,甲与乙的溶解度均为40g B、t3℃时,若将甲溶液由N点转变为M点状态,可采取添加溶质的方法 C、t1℃时,30g固体甲溶解在50g水中形成不饱和溶液 D、将t3℃时乙的饱和溶液降温至t2℃,有晶体析出13. 控制变量法实验探究重要方法。利用如图所示的实验能实现探究目的是( ) A、甲中①②对比可探究铁的锈蚀与植物油是否有关 B、甲中①③对比可探究铁的锈蚀与水是否有关 C、乙中铜片上的白磷与红磷实验,可探究可燃物的燃烧是否需要与氧气接触 D、乙中铜片上的白磷与热水中的白磷实验,可探究可燃物的燃烧是否需要达到着火点。14. 下列物质的鉴别与除杂的实验方案设计正确的是( )
A、甲中①②对比可探究铁的锈蚀与植物油是否有关 B、甲中①③对比可探究铁的锈蚀与水是否有关 C、乙中铜片上的白磷与红磷实验,可探究可燃物的燃烧是否需要与氧气接触 D、乙中铜片上的白磷与热水中的白磷实验,可探究可燃物的燃烧是否需要达到着火点。14. 下列物质的鉴别与除杂的实验方案设计正确的是( )选项
实验目的
实验方案
A
鉴别CH4和H2
分别点燃,观察火焰颜色
B
除去CuCl2溶液中少量的FeCl2
加入过量的Fe粉,过滤
C
鉴别硫酸铵固体和氢氧化钠固体
取样后,加水溶解,测溶液温度
D
除去CO2中少量的CO
点燃
A、A B、B C、C D、D15. 识别图像有利于发展科学思维。下列图像与反应过程的变化趋势对应正确的有( )A、 足量的铁片和镁条分别与等质量分数的稀盐酸反应
B、
足量的铁片和镁条分别与等质量分数的稀盐酸反应
B、 加热一定质量的高锰酸钾
C、
加热一定质量的高锰酸钾
C、 用两份等质量、等浓度的过氧化氢溶液制取氧气
D、
用两份等质量、等浓度的过氧化氢溶液制取氧气
D、 足量红磷在密闭容器中燃烧
足量红磷在密闭容器中燃烧
二、填空题
-
16. 高铁是“中国制造”一张耀眼的名片,它带领中国走向世界。请回答下列问题:(1)、高铁列车的车体建设需要消耗大量的铝合金,铝合金具有很多优良性能,例如:铝合金的硬度比纯铝 (填“大”或“小”);铝合金耐腐蚀,其原因是铝在空气中形成一层致密的(写化学式)薄膜。(2)、高铁列车与电路连接的石墨电刷主要利用的石墨性质是____。(填字母序号)A、稳定性 B、润滑性 C、还原性 D、导电性(3)、高铁酸钠()是高铁上常用的一种“绿色环保高效”的消毒剂,中铁元素的化合价为。(4)、近年来,我国高铁建设需要大量的钢铁。如图为模拟炼铁的装置,写出a中发生反应的化学方程式 , 写出尾气处理的一种方法。

三、综合题
-
17. 溶液在日常生活、工农业生产中具有广泛的用途。
 (1)、I.水是一种常见的溶剂,生活中处处离不开水。
(1)、I.水是一种常见的溶剂,生活中处处离不开水。自来水厂利用活性炭的性来除去天然水中的色素和异味。
(2)、用如图1所示装置电解水时,a管与b管所产生的气体的体积比约为 , 这个实验证明了水是由组成的。(3)、爱护水资源,人人有责。写出一条生活中节约用水的措施:。(4)、II. 农业上常用溶质质量分数为16%的NaCl溶液选种,实验室配制100g该溶液的过程如上面图2所示。图2中正确的操作顺序为____(填字母).
A、④②①⑤③ B、①②③④⑤ C、①②④③⑤ D、④⑤②③①(5)、②中需称量NaCl的质量为g,配制该溶液需要用的量筒量取水(填“50mL”、“100mL”或“200mL”)。(6)、配制好的溶液装瓶时洒落,将导致溶质质量分数 (填“偏高”、“偏低”或“不变”)。18. 具备基本化学实验技能是学习化学的基础和保证。小明和小华完成以下两组实验,相关实验装置如图所示。 (1)、I组:和的实验室制取
(1)、I组:和的实验室制取仪器a的名称是。
(2)、小明想用同一套装置分别制取和 , 应选用发生装置和收集装置(在A-E中选,填字母)。其中,制取H2的化学方程式为。(3)、小华选用装置A和F装置制取并测定生成氧气的体积,反应的化学方程式为 , 若测定出来的气体体积明显小于理论值,则可能的原因有 (填字母)。a.装置漏气
b.反应一开始产生气体就通入F中
c.收集气体前F装置中植物油上方原本有空气
(4)、II组:比较铁和铜的活动性小华分别取铁钉和铜片于A、B两支试管中,分别加入5mL的稀硫酸,能得出铁的活动性比钢强的实验现象是。
(5)、小明取铁钉于试管中,加入溶液(填化学式),也能比较铁和钢的活动性。19. 碳化钙的化学式为CaC2 , 是一种灰色块状固体,将其投入水中,它会迅速与水反应产生可燃烧的乙炔(C2H2)气体,反应完毕后,水底会沉积一种白色固体。实验小组决定对反应后水底沉积的白色固体进行探究。(1)、【提出问题】白色固体是什么物质?经交流讨论,小组一数认为肯定不是氧化钙。小组得出这一结论的理由是(用化学方程式表示)。
(2)、【查阅资料】①氢氧化钙微溶于水。②生产碳化钙的原料是碳酸钙,所以碳化钙中常有没反应完全的碳酸钙。
【做出猜想】经过讨论,小组对白色固体的成分提出如下几种猜想:
猜想I:Ca(OH)2;猜想II:CaCO3;猜想III:。
(3)、【实验探究】实验操作
实验现象
a、取少量白色固体放入烧杯中,加入蒸馏水,振荡静置,取上层澄清溶液于试管中,通入CO2
溶液变浑浊
b、另取少量白色固体放入烧杯中,加入足量稀盐酸
无气泡产生
操作a中通入CO2时,发生反应的化学方程式为。
(4)、【实验结论】结合操作a、b的实验现象分析,得出猜想成立。(5)、【反思拓展】乙炔在纯氧中完全燃烧时,火焰明亮井并产生高温,燃烧产物为和(填化学式)。但若在空气中点燃乙炔,则火焰不够明亮并有大量的黑烟产生,从燃烧的角度看,这是由于而造成的。20. 金属冶炼厂的粉尘中混有一定量的氧化铜、氧化锌以及能造成污染的硫。对粉尘收集并进行适当处理,还可得到纯净的化工产品,主要流程如下。 (1)、反应器Ⅰ中生成的可导致的环境问题是。(2)、反应器Ⅱ中发生的反应有 (写其中一条化学方程式)。(3)、反应器Ⅲ中,加入过量锌的目的是: , 滤渣b的成分是和(填化学式)。(4)、“系列操作”包含:蒸发浓缩→→过滤。过滤需要用到的玻璃仪器有烧杯、玻璃棒、 , 玻璃棒的作用为。
(1)、反应器Ⅰ中生成的可导致的环境问题是。(2)、反应器Ⅱ中发生的反应有 (写其中一条化学方程式)。(3)、反应器Ⅲ中,加入过量锌的目的是: , 滤渣b的成分是和(填化学式)。(4)、“系列操作”包含:蒸发浓缩→→过滤。过滤需要用到的玻璃仪器有烧杯、玻璃棒、 , 玻璃棒的作用为。四、计算题
-
21. 100g的稀盐酸与含杂质的石灰石10g恰好完全反应(杂质不溶于水且不与盐酸反应,也不与生成物反应),测得烧杯中物质总质量的变化如图所示。
 (1)、生成气体的质量为g。(2)、计算100g稀盐酸中溶质的质量分数(写出计算过程)。
(1)、生成气体的质量为g。(2)、计算100g稀盐酸中溶质的质量分数(写出计算过程)。
-